科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2018-10-25
2018年10月19日,绿色萤光蛋白(Green fluorescent protein,GFP)发现者,2008年诺贝尔化学奖得主下村修(Osamu Shimomura,1928-2018)因病逝世,享年90岁 。
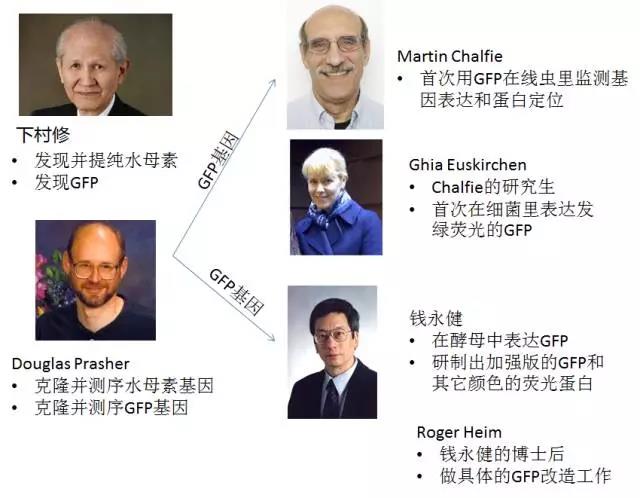
GFP的发现和普及过程跌宕起伏,涉及四个实验室和六个关键人物,其中三人——下村修、马丁·沙尔菲、钱永健——因此获得2008年诺贝尔化学奖,但有一位关键人物一度放弃了GFP。对于这一段历史,每个人都能得到不一样的启示。这个故事值得我们一遍又一遍地重温和回味。

“科学有时很残酷。对于Douglas Prasher来说,在卖车行打一份一小时挣10美元的工,与获得诺贝尔奖及其带来的荣耀和120万美金,只有一线之差。”——Dr. Marc Zimmer, “Illuminating Disease: AnIntroduction to Green Fluorescent Proteins”
每年六七月份,在美国西北太平洋海岸边,都会出现成千上万的水晶水母。它们直径不超过10厘米,没有头,没有有毒的触角,全身都是透明的,在海水中摇曳着。当受到惊扰的时候,它们会在伞型身体的下缘发出一束束绿光。夏天一过它们又全都消失。日出日落,潮涨潮退,年复一年,周而复始,好像从远古到永远,都不会改变。
直到二十世纪六十年代初的一个夏天,几个长杆捞网突然划破海面的平静,开始一网一网地捕捞水晶水母。
在此后的三十多年里,水晶水母(学名叫维多利亚多管发光水母)的绿色萤光的奥秘被一点一点发现。
绿色萤光蛋白(GFP)的发现和应用成为生命科学革命性的里程碑, 而以GFP及其它荧光蛋白为基础的现代分子成像技术成为生物医药科研的不可缺少的工具, 被誉为二十一世纪的显微镜。GFP的光辉照亮了世界的每个角落,彻底改变了人类对疾病的认知过程。
GFP的发现和普及过程跌宕起伏,涉及四个实验室和六个关键人物,其中三人因此获得诺贝尔化学奖。GFP的历史在以前多有介绍,包括饶毅老师于2008年发表的博客,其中描述最为翔实的是Marc Zimmer教授于2015年出版的新书。绿色萤光蛋白的故事仍值得我们一遍又一遍地重温和回味。
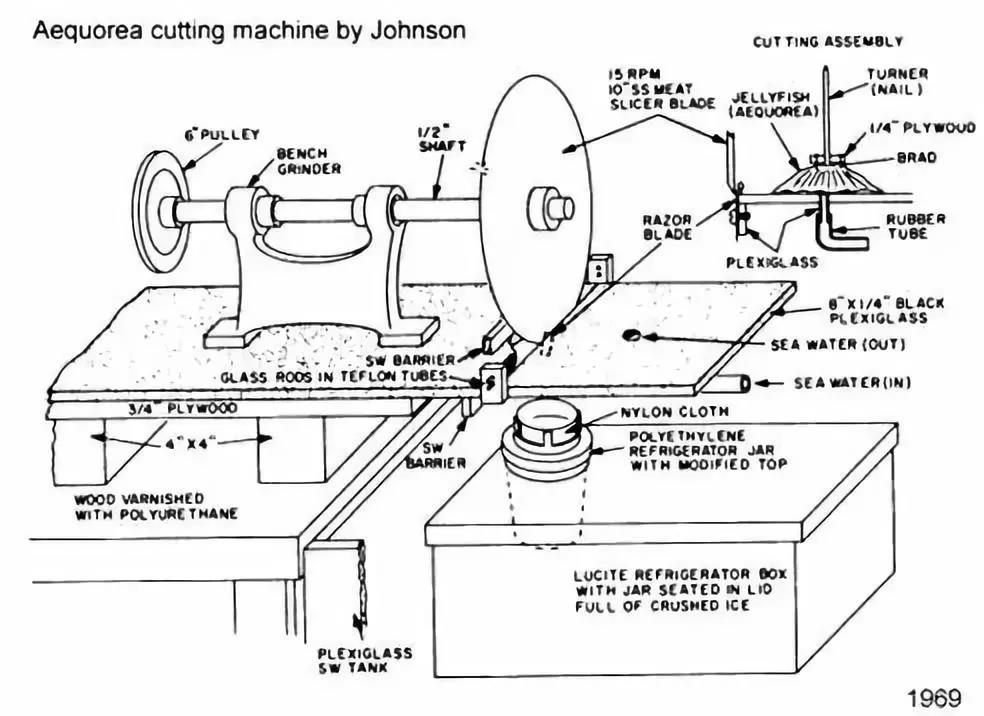
那些长杆捞网的主人是在美工作的日裔学者下村修(Osamu Shimomura)和他的实验室老板Frank Johnson,及实验室其他成员。
下村修出生于1928年,从小在日本和中国长大。当第二颗原子弹爆炸在长崎时,当时年仅16岁的下村修正在附近的军工厂工作。他目睹了闪光和巨大的蘑菇状烟云。他在黑色的雨中跑回家,到家时身上的白衬衣已变成灰色。
下村修在1960年应邀并凭借着福布莱特奖学金到美国普林斯顿大学做访问学者。他先在普林斯顿大学工作22年,后又在伍兹霍尔海洋研究所做科研。他一直对生物发光感兴趣。为什么水晶水母可以发绿光是他孜孜不倦不舍不弃想要回答的问题。
在将近20年的时间里,每年夏季他和家人从东海岸一路开车到西海岸,在华盛顿大学的“星期五港”实验室外的栈桥上大批大批地捕捞水晶水母。回到实验室,他又忙着把水母的伞盖下缘切下来,不厌其烦地分离和分析各种成分。剪切,挤压,过滤,搅拌,沉淀……
几十次实验和数万只水母之后,下村修终于弄清楚了绿色荧光的奥秘:
水母有两个发光蛋白,第一个他命名为水母素(aequorin),是一个荧光素酶,在碰到钙离子时会发出蓝光。第二个就是绿色荧光蛋白或GFP。水母素发出的蓝光作为能量会传给GFP,激发出绿色荧光。但GFP的含量在水母中远低于水母素,从水母中提取GFP更加耗时耗力。
水母素的发现导致了两篇重要的论文发表。水母素被作为钙离子的传感器注射到藤壶的肌肉细胞和乌贼的神经细胞里,当肌肉收缩时或是神经细胞放电时,科研人员第一次在细胞里清楚地看到了明亮的蓝色闪光。
科学界意识到了发光蛋白的可能应用,但每一篇论文虽然只需要几毫克的水母素,却需要几万只水母来提炼。这种昂贵的技术注定无法普及。
下村修当时只对水母素蛋白感兴趣,而并不在意GFP。他提出了一个假说:GFP蛋白仅靠它自己不能发荧光,需要水母体内的酶加工才会变成荧光蛋白。
如果这个假说成立,GFP在生物科研中用处就不大了, 因为它在其它生物个体中无法独立发光。但遗憾的是,该假说当时被普遍接受, 对以后GFP的研发有着深远的负面影响。再加上GFP蛋白提取困难,在随后的20多年里,GFP的科研几乎没有任何进展。
故事中的第二个人物是比下村修小23岁的Douglas Prasher博士。Prasher在乔治亚大学的MiltonCormier实验室作博士后时候,和其他成员成功地从水母中找到并克隆了水母素的基因,并用该基因在大肠杆菌了表达了水母素蛋白。
这是一个不小的成就。同从水母中提取蛋白相比,用细菌表达制备蛋白要方便、省时、省力和便宜得多,也人道得多。任何实验室想要用水母素作为钙离子的传感器,都可以直接用细菌生产或以合理的价格购买。水母素的来源不再是一个瓶颈,直到今天它仍在实验中被广泛用来检测钙离子。
后来Prasher也在伍兹霍尔海洋研究所建立了自己的实验室。他开始把目光投向了无人问津的GFP。他产生了一个独特的想法,如果下村修的假说不成立呢?
也许GFP本身就能发荧光,并不需要水母的其它蛋白处理加工。如果这样,GFP就可以通过基因拼接的方式被附着在任何蛋白的末端。而目标蛋白在活细胞内甚至是活的个体内的一切生理状态下的活动都能被看得清清楚楚,就像时时刻刻有一盏探照灯照着它。
而那时候人们还没有任何手段追踪蛋白在活细胞或活体里的动态变化。验证这一想法的第一步就是克隆GFP的基因。基因是蛋白的源程序。有了基因,后续工作就容易地多。
Prasher把自己的这些想法和计划组织起来,作为科研基金的申请交了上去。但Prasher的假说与占主导地位的理论背道而驰,因而他不断碰壁,申请一次次的被拒绝。但功夫不负有心人,终于Prasher从美国癌症协会获得了20万美金的科研基金来支持这个项目。
从80年代初起,Prasher也开始一次次地在初夏前往西海岸“星期五港”实验室,大批大批地捞水晶水母。但Prasher与下村修两者的差异是,下村修感兴趣的是蛋白,而Prasher搜寻的是GFP的基因。
由于在当时的条件下,很多现在普及的分子生物学的手段还没有被发明,Prasher的工作量与下村修相比只多不少。
在将近3年的时间里,Prasher先从约7万只水母中提取足够的RNA建立水晶水母的基因库(cDNA library),再用同位素标记的探针杂交的方法来大海捞针。一遍遍地尝试,一遍遍地失败,再尝试,再失败。直到他拿到了完整的GFP基因。他将GFP基因转到了大肠杆菌里表达,又提取了GFP蛋白。
但残酷的结果使他坠入了绝望的深渊:GFP并不能发绿荧光!看来下村修的理论是对的。他本来就有些动摇的自信心遭到致命一击。
Prasher是一个孤独的科学家,他不擅于和同行交流。
他和下村修在一个研究所共事多年,研究的课题紧密相关,但两人只有一次谈话的场合,还是在远离研究所的一次会议上。在他苦闷的时候,在他的实验走到瓶颈的时候,他无人可以倾诉,可以交流。这时候他的20万科研基金已经用完了,再申请又被拒绝。他心灰意冷,彻底放弃了GFP。
但在Prasher彻底告别GFP之前,他还是把克隆GFP基因的过程和结果写成一篇论文,于1992年发表。
在文中,他承认了GFP本身并不发荧光,下村修的理论是对的。这可能是历史上最悲壮的一篇论文。在看似无边的黑暗和疲倦中,Prasher不知道他与绿色的曙光有多么接近。
Prasher的这篇论文引起了两位同行的注意:哥伦比亚大学的生物学家Martin Chalfie和加州大学圣地亚哥分校的钱永健 (Roger Tsien)教授。两个教授都发电子信件向Prasher索要GFP基因。Prasher毫不犹豫地无条件给两个实验室寄去了。

Chalfie是研究线虫的专家。线虫约一毫米长,经常被用作模型来研究动物的发育过程和初级神经系统。它的一大优势就是全身上下是透明的,这是验证荧光蛋白标记技术最理想的动物模型。
Chalfie得到GFP的DNA后把它交给在实验室里工作的研究生Ghia Euskirchen。Euskirchen发现Prasher的GFP基因并不齐整,在首尾各多了一些碱基,因此它表达的蛋白并不是天然的GFP蛋白,而是抻长版的GFP,前后都有些多余的氨基酸残基。
原来Prasher在把GFP基因插到表达质粒上时,用了当时的通行方法,用两个限制性内切酶切出来含有GFP基因的DNA片段,再接到质粒上。限制酶方法方便但不精确。
为了精确地把GFP基因插到表达质粒上,Euskirchen使用了刚发明不久还没有普及的PCR技术。对于基因剪拼来说,限制酶方法是用斧头砍,接缝的地方总是多一块或少一块,而PCR方法则是激光刀,可以把一个基因准确地切割下来,一个碱基不多,一个碱基不少。她把GFP基因严丝合缝地插入到质粒里。
令她大吃一惊的是,表达该质粒的细菌在培养的时候就是绿色的,在荧光显微镜下观察竟然发出明亮的绿荧光。Euskirchen成为世界上第一个在大肠杆菌中看到GFP荧光的人。
至此下村修的理论被证明是错误的。GFP不需要其它酶加工。它的三个氨基酸构成光核或发色团,而蛋白的其余部分折叠成一个桶状,将发色团围在中间,就象一个有灯罩的台灯一样。而Prasher的GFP蛋白由于首尾多了一些氨基酸,在细菌中不能形成正确的桶状构象,就发不了荧光。
Chalfie的团队迅速地用GFP标记了线虫的对接触敏感的蛋白,观察到它在线虫体内神经细胞的表达。这一成果1994年发表在《科学》杂志上[8]。Prasher由于提供了基因,被列为论文的最后作者。那期《科学》的封面就是一张在黑色的背景中发绿色荧光的线虫的照片。
文章的发表引起了世界性的轰动。千千万万个学者为这张照片而痴迷。用GFP作为工具监测活的生物个体里的基因表达和蛋白变化为解决无数个生命不解之谜提供了钥匙。

钱永健差不多同一时间得到Prasher的GFP基因,但却没有立刻开展这个项目。
钱永健是钱学森的表侄,在美国出生,16岁就获得西屋科学奖。他是化学方面的专家,他的实验室缺乏有生物背景的人。钱在等他刚招的生物博士后Roger Heim来做这个项目。在Heim还没有加入钱的实验室之前,钱永健就听说了Chalfie的实验室在GFP上取得的突破。他们决定另辟蹊径,在酵母里表达了GFP。
另外他们以GFP为基础,产生了一系列的突变蛋白,产生包括蓝色,黄色和青色等不同颜色的荧光[9]。这样在同一实验中,两或三个不同的蛋白可同时被跟踪监测。
他们还在GFP蛋白里置换了一系列的氨基酸,大大提高了GFP的稳定性和发光强度。在今天生物医学研究中大部分被使用的GFP都是钱的实验室研制出的加强版GFP。
如果说Chalfie的那篇《科学》论文是向世界宣告一个工具的诞生,那钱的工作就是使这个工具更好用,更方便。洪水之门一下子被打开了,使用荧光蛋白技术的论文呈几何级数增长。今天发表的生物医药领域科研成果有一半以上都用到这一技术。
2008年10月,瑞典皇家学院宣布诺贝尔化学奖将被授予对GFP的发现和应用有突出贡献的三位科学家:下村修,Chalfie,和钱永健。而也起了关键作用的Prasher却遗憾地与诺贝尔奖失之交臂。
更令人感慨的是,Prasher此时已不再从事与科学有关的工作。当记者找到他时,他正在阿拉巴马州的一家丰田车车行打工,开班车接送客人,挣着最低工资。
原来在放弃了GFP项目不久,Prasher离开了伍兹霍尔海洋研究所,在阿拉巴马州找到一份政府科研的工作。但不幸的是,由于政府撤销了对该科研项目的投资,Prasher失去了这份工作。他又不想离开那个城市,但那里的科研工作机会实在有限。为了养家糊口,Prasher无奈放弃了科学,找到了这份临时工。
Chalfie和钱在记者采访时和后来的诺贝尔奖演讲时都强调了Prasher的关键作用。钱永健邀请并资助了Prasher一家去瑞典参加诺贝尔奖颁奖典礼。之后,Prasher又重返科研,在钱的实验室里工作。
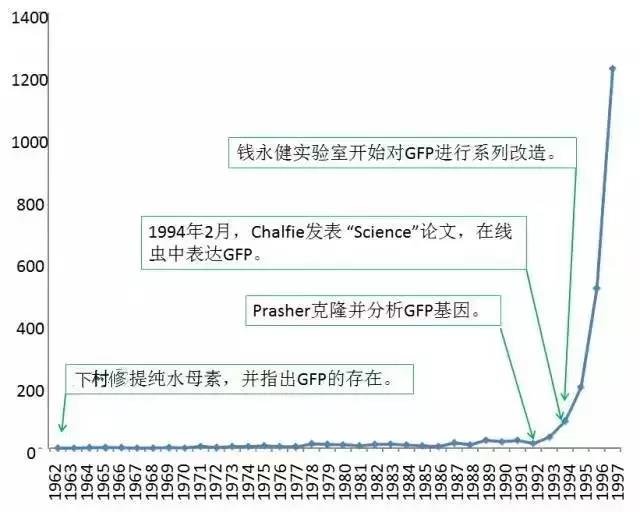
图说:通过GoogleScholar检索出的每年发表的提到GFP的论文数。
GFP的故事令我感慨万千。对这一段历史,也许每个人得到的启示都不一样,可以探讨的话题很多。
IQ和EQ与成功的关系;细节决定成败的含义;每一个突破性成果的背后的研究生,博士后,和实验员的贡献;科学权威的理论对科学发展的影响;当代科研基金的评奖机制能否孕育出革命性的成果;运气在科研中的作用(从80年代末起,每年夏天的水晶水母潮竟然神秘地消失了);对前沿技术(比如90年代初的PCR)的早期使用所获得的巨大优势……
但我今天只想谈谈两个话题:科学与技术,贡献和荣誉。
2015年10月23日,华尔街时报刊登了一篇随笔,题目为“基础科学之谜”。作者Matt Ridley是资深的生物学家和畅销书作者。
他在文中的主要观点是纵观人类历史,技术的发展是复杂的,和科学的进步关系并不大。往往是新技术的出现才带来了科学的突破,而不是像人们普遍认为的那样,科学的发展引发了技术的革新。
文中指出,是先有了蒸汽机,才建立起热动力学;先有了X射线晶体技术,才发现了DNA的双螺旋结构。文章的一个推论是政府耗巨资支持基础科研是没有必要的。
我认为Ridley的观点有些以偏概全。就拿生物医药来说,也许在早期,这种现象确实普遍存在:先发现了阿斯匹林,几十年后其机理才逐渐浮出水面。
但在今天,从生物机理(科学)到确定药靶再到新药研发和使用(技术)是占主导地位的模式,而GFP的历史更是一个典型的例子。
下村修在一次又一次地提取水母中的发光蛋白时,他只想去解决生命的奥秘之一。但一旦GFP的机理被弄清楚了,GFP蛋白标记技术就水到渠成呼之欲出。Chalfie的论文完成了由科学到技术蜕变的第一步,而钱永健的实验室和销售加强版GFP基因的公司则完成了第二步:新兴技术的成熟化和产业化。
再举一个例子。PCR技术虽然是1983年问世的,但真正使其推广的关键是能够耐高温的TaqDNA聚合酶。这种酶是在六、七十年代搞基础研究的生物学家在探索黄石公园的温泉中生长的细菌时发现的。一个技术的诞生和成熟过程可能来源于几十年来科学的积累:PCR技术诞生就是建立在DNA复制过程理论基础上,而其推广则离不开Taq酶的发现。
GFP的历史还告诉我们,科学和技术之间不能简单地归纳为线性的单向关系,科学和技术之间有着非常复杂的动态作用过程。由于GFP的发现(科学),才有了荧光蛋白标记技术,许多过去无法回答的生物问题才能迎刃而解(科学),包括许多疾病的分子机理,这又进一步促进了新药的研发(技术)。科学产生技术,技术推动科学,科学再产生新的技术,如此循环反复。
咱们再来谈一下贡献和荣誉。在今天,任何科研项目的成功都要依靠团队的合作,而且这个趋势只会愈演愈烈。据华尔街时报报道,拥有几千个作者的论文也已不足为奇。在这种时代的背景下,对任何一个科研成果来分析比较每位参与者的贡献将会越来越困难。
在GFP的发现和推广的过程中,下村修是开拓者,Prasher起到承前启后的作用,Chalfie证实了自己的远见,钱永健善于改进,而 Euskirchen和Heim拥有一流的实验设计和执行能力。
要想从中挑出三个人授予诺贝尔奖是一个很艰难的抉择。我相信诺贝尔奖评委是想努力做到公平的,他们为此认真调查了一年才做出的决定。但由于每单项奖每年授予人数不能超过三个人,诺贝尔奖的评选结果注定有其不公平性。诺贝尔奖既是给个人的荣誉,更是对某个科研领域的肯定。
Prasher在GFP技术的发展中起到了关键作用,但功亏一篑,痛失诺贝尔奖。他在大众的眼里被媒体塑造成悲剧的角色。当我们在为他叹息的时候,我们有没有想到我们是可以改变这一结局的?
每一个做出贡献的人都应该是我们的偶像,不管有没有得到诺贝尔奖或其它荣誉。得到诺奖的人值得我们敬仰和歌颂,没有得到的人更需要鲜花和喝彩。社会、媒介和政府都有责任,让那些应该得诺奖而没有得到的人享受同样的荣耀和待遇。
从古至今,人类凭借着自强不息的精神,对知识的好奇心,对真理的渴望,不断推动科学和技术的交替进步,促进社会的发展。在漫漫的科技历史长河中,既有牛顿和爱因斯坦这样灿若星辰照亮世界的天才人物,也有Prasher在黑暗中踯躅而行的寂寥身影。他们都是英雄。
来源:微信公众号“赛先生”
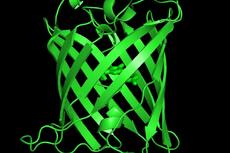
荧光蛋白的发色团及β桶结构
诺奖得主Martin Chalfie:让绿色荧光蛋白点亮生物学研究之光

2008年诺贝尔化学奖获得者下村脩去世

【分析】细胞膜表面特定蛋白上的聚糖成像策略

【纳米】高度有序的荧光蛋白纳米阵列:生物启发的人工光捕获系统
【大师讲堂】诺奖得主Martin Chalfie:绿色荧光蛋白的发展历程

【论文精选】基于绿色荧光蛋白的冷鲜猪肉中大肠杆菌预测模型的构建
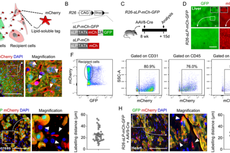
科学家建立基于膜透过荧光蛋白的邻近细胞标记技术
【大师讲堂】诺奖得主Martin Chalfie:绿色荧光蛋白的发展历程
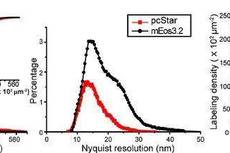
光激活定位显微技术和新型光转换荧光蛋白pcStar用于活细胞动态超分辨成像