科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-03-27
药明康德AI/报道
就在几个月前,DeepMind推出了AlphaFold系统,这个被称为生物界“AlphaGo”的系统能够预测并生成蛋白质3D结构。而近日,来自MIT的研究人员开发了一个新的研究模型,能够直接预测氨基酸链片段是如何决定蛋白质功能的。这一发现可以帮助研究人员设计和测试新的蛋白质,从而用于药物研发和生物学研究。
我们都知道,蛋白质是维持我们生命所必需的庞大而复杂的物质。蛋白质具体能完成什么样的功能,主要取决于它独特的三维结构。因此了解蛋白质的结构,对于预测其对某些药物的反应来说,是一个非常重要的环节。
▲每一个蛋白质都拥有错综复杂的三维结构(图片来源:123RF)
然而,尽管有了数十年的研究和多种成像技术的辅助,我们仍然只了解到了无数蛋白质结构中的很小一部分,还有很多未知结构的蛋白质功能尚未揭晓。针对这一情况,来自MIT的研究人员开发出了一种方法,“学习”了蛋白质序列中每个氨基酸位置上容易计算的表征。随后,研究人员将这些表征输入机器学习模型,让模型直接预测单个氨基酸片段的功能,而无需任何蛋白质结构的数据。
首先,研究人员使用了来自蛋白质结构分类数据库(SCOP)的约22000种蛋白质,将这些蛋白质按照结构和氨基酸序列的相似性进行分类,并对机器学习模型进行训练。对于每一对蛋白质,研究人员都会根据其SCOP类别计算出一个结构相似性评分。然后,研究人员将随机的蛋白质结构对及其氨基酸序列输入机器学习模型,通过编码器将它们转换成数值表示出来,称为嵌入(embedding)。每个嵌入都包含了一对氨基酸序列的相似性信息。
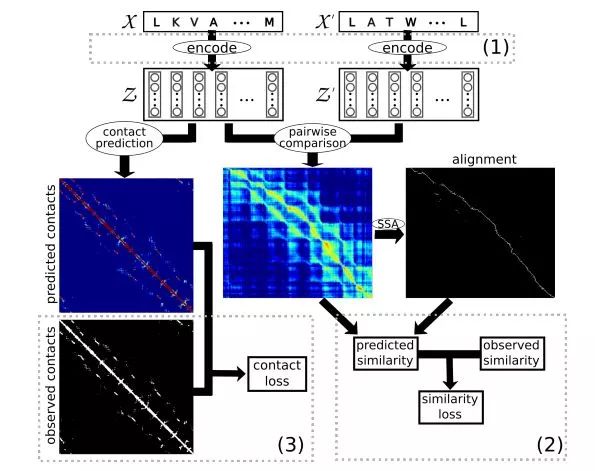
▲该模型的示意图(图片来源:arxiv.org)
该模型将两个嵌入对齐,然后计算出相似度评分,以预测其代表的蛋白质三维结构的相似性。然后,计算机会将这一评分与真实的SCOP相似性评分进行比较,并向编码器发送反馈信号。如果模型的预测分数与真实分数相差较远,则会进行一定的调整。
同时,该模型预测了每次嵌入的“接触图”(contact map),即每个氨基酸与该蛋白质中其他氨基酸的距离,并将其预测的接触图与来自SCOP的已知接触图进行比较,然后向编码器发送反馈信号。这一步骤有助于模型更好地明确氨基酸在蛋白质结构中的确切位置,从而进一步了解每个氨基酸的功能。
对于某个氨基酸链,该模型可以为三维结构中的每个氨基酸位置生成一个嵌入。然后,机器学习模型可以使用这些序列嵌入,根据其预测的三维结构接触图,来准确预测每个氨基酸的功能。在一个应用实例中,研究人员使用该模型预测有哪些蛋白质可以通过细胞膜,其预测结果比现有的先进模型还要更加准确。
接下来,研究人员计划将该模型应用到更多的预测任务中,例如弄清楚哪些序列片段可以与小分子结合,这对于药物研发工作来说是至关重要的。研究人员表示,这项研究最终将可以应用于人类健康和药物基因组学,因为它有助于检测破坏蛋白质结构的有害突变。
参考资料:
[1] Bepler, et al., (2019). Learning protein sequence embeddings using information from structure. ICLR 2019, arXiv:1902.08661
[2] MIT CSAIL’s AI predicts a protein’s function from chains of amino acids. Retrieved March 26, 2019, from https://venturebeat.com/2019/03/22/mit-csails-ai-predicts-a-proteins-function-from-chains-of-amino-acids/
[3] Model learns how individual amino acids determine protein function. Retrieved March 26, 2019, from http://news.mit.edu/2019/machine-learning-amino-acids-protein-function-0322
来源:global_academia 学术经纬
原文链接:http://mp.weixin.qq.com/s?__biz=MzI5MDQzNjY2OA==&mid=2247491967&idx=3&sn=356d00ebffb05a59fb5f597c4a326021&chksm=ec1d422cdb6acb3a2ac76f9e565c22bd9afaebffe95cd397487a82753f4280e7d6b300d34568&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
速度提高100万倍,哈佛医学院大神提出可预测蛋白质结构的新型深度模型
神经科学:协同工作的大脑
苹果WWDC 2017干货亮点全在这里
氨基酸的检查
血清支链氨基酸/芳香族氨基酸比值
氨基酸自养生物
科学家利用大连相干光源揭示电喷雾离子化过程中氨基酸侧链电荷影响蛋白质结构的分子机制

用突变基因,解码蛋白质结构
血清支链氨基酸/芳香族氨基酸比值
必需氨基酸检查