科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-27
来源:CBG资讯
第一作者:杨国辉
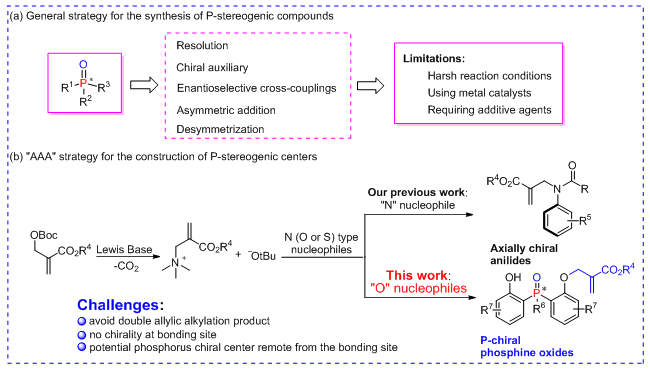
图1(来源:Chem. Sci.)
有机路易斯碱催化的基于MBH加成物的不对称烯丙基烷基化反应(AAA)是用于手性化合物合成的非常简单、高效的方法,但其主要被用于碳中心手性化合物的构筑。南开大学化学学院程津培、李鑫课题组在前期发展的基于MBH加成物的不对称烯丙基烷基化策略(AAA)合成手性苯胺化合物的基础上(J. Am. Chem. Soc. 2018, 140, 12836-12843),进一步挖掘AAA反应在合成非碳中心手性化合物的潜力,实现了基于去对称化策略的AAA 反应合成手性磷化合物(图2)。该反应具有较广泛的底物普适性,立体选择性较好。进行放大量实验产物的对映选择性可以很好地保持。对产物进一步转化,可以合成新的催化剂,并完成了其在不对称催化中的初步探索。
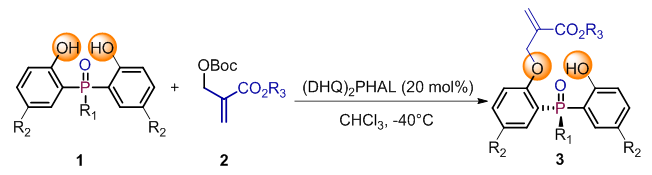
图2(来源:Chem. Sci.)
课题组研究人员通过对底物基础参数与立体选择性之间的线性自由能关系分析方法,发现产物的选择性受芳环上R2取代基团的电子和位阻影响。此外,与磷中心相连的R1基团的大小也对立体选择性控制有很大贡献。通过理论计算,提出了合理的过渡态模型,得到了与实验相吻合的对映选择性,并合理解释了线性自用能关系分析中获得的相关信息(图3、图4)。
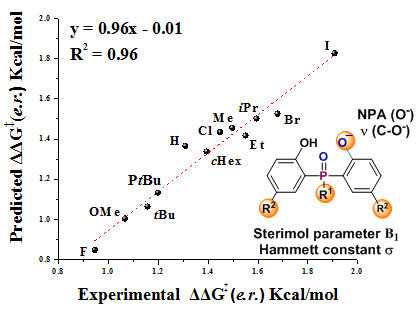
图3 (来源:Chem. Sci.)
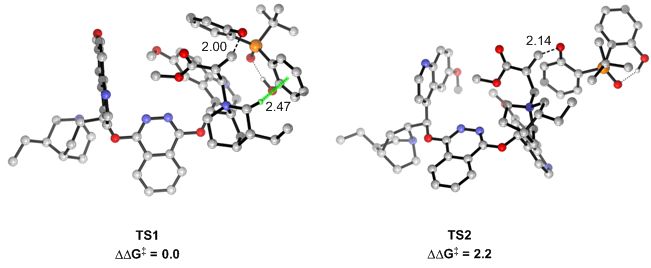
图4 (来源:Chem. Sci.)
来源:BeanGoNews CBG资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzI4ODQ0NjUwMg==&mid=2247494909&idx=2&sn=7acc0a775ebbd709aed1cd8faa67a8f5&chksm=ec3cedb4db4b64a2b48d2fb94a054015b10062b077d096fc093ae0f035d211063fa660da121b&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
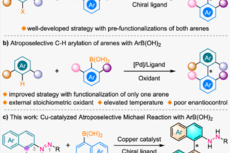
JACS:旧配体新手性!谭斌团队利用BINOL配体高效构筑轴手性联芳基化合物
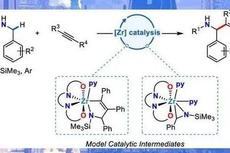
JACS:锆催化炔烃的氢化氨基烷基化反应合成烯丙基胺
遗传学:巨型基因组研究提供了关于人类疾病和遗传多样性的新知识
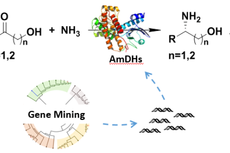
胺脱氢酶合成手性胺醇化合物研究取得进展

Angew:Ir催化酰胺烯醇的不对称烯丙基烷基化反应
苹果WWDC 2017干货亮点全在这里

不对称氢化帮助构建环状手性季碳化合物
动物学: 侦察蚁能够引导搬运食物的同窝蚂蚁回家
化学:以分子为基础的隐形墨水
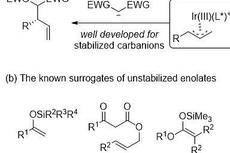
烯基叠氮参与的高对映选择性烯丙基烷基化反应