科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-15
来源:BioArt
发育过程中的基因表达需要将细胞核划分为精确的亚核区域,活跃的常染色质集中在细胞核的中间区域而核周围是基因表达沉默的异染色质区域【1】。已知的一些与lamin A突变相关的退行性疾病表明染色质正确地结合在细胞核周围的区域对于细胞的完整性非常关键【2】。H3K9甲基化(H3K9me)是异染色质的特征之一,能够介导转录抑制和染色质定位在核膜内侧【3】。在线虫的胚胎期,染色质结构域蛋白(chromodomain protein)CEC-4能够通过H3K9me将异染色质锚定在核膜上,随后在分化的组织中异染色质隔离信号途径(heterochromatin-sequestering pathway)被诱导表达。但是异染色质的空间隔离是如何建立的还不很清楚。
为了进一步对该问题进行解析,2019年5月23日,来自瑞士巴塞尔大学的Susan M.Gasser研究组在Nature发文,题为Active chromatin marks drive spatial sequestration of heterochromatin in C. elegans nuclei,为异染色质的空间隔离的调控通路提供了非常新颖的思路。

为了找到异染色质空间隔离调控的关键因子,Gasser研究组首先建立了RNAi筛选的品系库,以缺少H3K9me锚定因子CEC-4蛋白作为筛选背景,通过观察异染色质报告因子gwIs4在备选基因敲低的情况下的变化,作者们对已有的品系库中97个备选的异染色质与核膜分离调控因子进行筛选。挑选备选基因的标准主要基于这些因子在具有核内膜的定位或者是具有修饰组蛋白的功能。他们使用的异染色质报告因子gwIs4是已知的在核内膜上具有稳定分布特点,并且具有抑制性的组蛋白标记H3K9me2、H3K9me3和H3K27me3,但是缺少H3K4me3标记【4】(图1)。
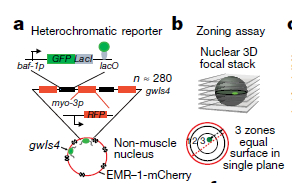
图1 异染色质报告因子构建模式图以及报告因子为止分布统计示意图,异染色质的信号落在每一部分的几率均是33%
通过RNAi的筛选,作者们发现了两个重要的基因mrg-1和akap-1参与到异染色质分布的调控中(图2)。并且作者们发现MRG-1在分化的肠细胞中促进异染色质锚定的功能不依赖于CEC-4-H3K9me。MRG-1是酵母Eaf3和人类MRG15染色质域蛋白的同源蛋白【5】。与前人的研究相一致的是【6】,MRG-1的分布集中在常染色质上,与H3K36me2/me3标记的染色质相关,而与H3K27me3和H3K9me3标记的染色质负相关(图3)。因此,以上的结果说明MRG-1对于异染色质结构的影响是间接的。而且他们还发现分化后的肠细胞核中异染色质的位置形成需要常染色质的H3K36me2/me3修饰。
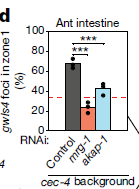
图2 RNAi筛选得到异染色质分布的重要调控因子
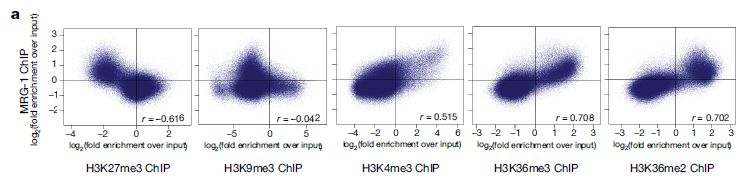
图3 MRG-1结合位点与组蛋白修饰的ChIP-seq结果
作者们发现在线虫卵中mrg-1的敲除引起异染色质解折叠以及去抑制(即不能正确定位),但是强烈的CEC-4-H3K9me锚定信号仍可以阻止异染色质的去定位,因此这其中必有其它因子参与异染色质的空间定位。为挖掘MRG-1调控异染色质空间分布过程中其它因子,研究人员提出设想:这些因子在mrg-1突变体中发生了表达改变。因此,研究人员首先利用RNA-seq发现411基因显著上调、24个基因显著下调,并推测辅助MRG-1发挥调控的因子可能就在其中。
通过分析前人的研究,作者们发现,在很多物种中MRG-1的同源蛋白都参与到组蛋白乙酰化的酶复合体中。作者们通过筛选乙酰化相关的酶RNAi的品系中发现cbp-3对于异染色质的定位非常重要。CBP-3是CBP-1的截短形式,是线虫中CBP/p300的同源蛋白。作者们发现在MRG-1敲除或者是CBP-1过表达的情况下CBP-1通过属于bZIP转录因子家族的C/EBPs的ATF-8招募到异染色质的区域。
总的来说,Gasser研究组展示了MRG-1蛋白虽然定位在常染色质上,但是间接地对异染色质的空间分隔起到了非常重要的作用,并且发现与基因激活相关的H3K27ac乙酰转移酶CBP/p300对于异染色质的正确的分布也非常关键。这提示我们,异染色质的异常定位以及由此引发的一些疾病很有可能与CBP的水平异常相关。
原文链接:
https://www.nature.com/articles/s41586-019-1243-y
参考文献
1. Solovei, I., Thanisch, K. & Feodorova, Y. How to rule the nucleus: divide et impera. Current opinion in cell biology 40, 47-59, doi:10.1016/j.ceb.2016.02.014 (2016).
2. Perovanovic, J. et al. Laminopathies disrupt epigenomic developmental programs and cell fate. Science translational medicine 8, 335ra358, doi:10.1126/scitranslmed.aad4991 (2016).
3. Mattout, A., Cabianca, D. S. & Gasser, S. M. Chromatin states and nuclear organization in development--a view from the nuclear lamina. Genome biology 16, 174, doi:10.1186/s13059-015-0747-5 (2015).
4. Towbin, B. D. et al. Step-wise methylation of histone H3K9 positions heterochromatin at the nuclear periphery. Cell 150, 934-947, doi:10.1016/j.cell.2012.06.051 (2012).
5. Doyon, Y., Selleck, W., Lane, W. S., Tan, S. & Cote, J. Structural and functional conservation of the NuA4 histone acetyltransferase complex from yeast to humans. Molecular and cellular biology 24, 1884-1896, doi:10.1128/mcb.24.5.1884-1896.2004 (2004).
6. Filion, G. J. et al. Systematic protein location mapping reveals five principal chromatin types in Drosophila cells. Cell 143, 212-224, doi:10.1016/j.cell.2010.09.009 (2010).
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652471293&idx=4&sn=bdec0331cf9c444d29af7706d495c12c&chksm=84e2ec49b395655fa65ad5d42eac1656f5874b0e196cb3621524020e0effa1a09bbe7e0f505e&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
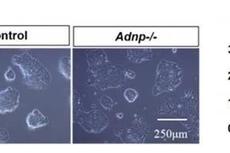
水生所揭示ADNP维持胚胎干细胞干性的染色质调控机制

Nature背靠背:组蛋白H1调控染色质结构
红细胞染色质小体

新突破! 二维实验系统成功应用于四维材料研究
关于举办“环境友好的农林害虫生态调控与生物防治技术高级研修班”通知
环境友好的农林害虫生态调控与生物防治技术——2017高级研修班总结

Nature: 核小体构象变化与异染色质相分离

Nature: 沈晓骅团队发现U1 snRNP调控非编码RNA结合染色质的新机制

浙江大学揭示染色质水平调控拟南芥缺磷响应的分子机制
X染色质