科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-10-16
来源:BioArt
原标题:Molecular Cell:蒋玉辉团队揭示四氢生物蝶呤合成途径代谢酶在肿瘤发展中的作用机制
GTP环化水解酶 (GTP cyclohydrolase I),6-丙酮酰四氢生物蝶呤合成酶 (6-pyruvoyltetrahydropterin synthase,PTPS) 以及墨蝶呤还原酶 (sepiapterin reductase) 负责四氢生物蝶呤(tetrahydrobiopterin,BH4)的从头合成。
生物体BH4合成缺陷往往伴随着这些酶的的功能异常。BH4可作为一氧化氮合成酶(nitric oxide synthases,NOS)活化所需的辅酶因子。NOS包括三个同工酶nNOS、iNOS和eNOS,它们能够催化L-精氨酸产生L-瓜氨酸和一氧化氮。
一氧化氮除了作为神经递质的作用外,还通过介导蛋白S-亚硝基化 (S-Nitrosylation) 参与细胞信号通路的调节。蛋白S-亚硝基化会在多个方面影响蛋白质状态,包括蛋白质稳定性、活性以及蛋白质-蛋白质相互作用。以往BH4合成代谢通路在肿瘤发展中的功能及其相关机制鲜有报道。
2019年10月15日,来自上海交通大学附属上海市第一人民医院的蒋玉辉教授研究团队在Molecular Cell杂志上在线发表了题为PTPS Facilitates Compartmentalized LTBP1 S-Nitrosylation and Promotes Tumor Growth under Hypoxia的文章,其对PTPS在早期大肠癌进展中的作用做了诠释。

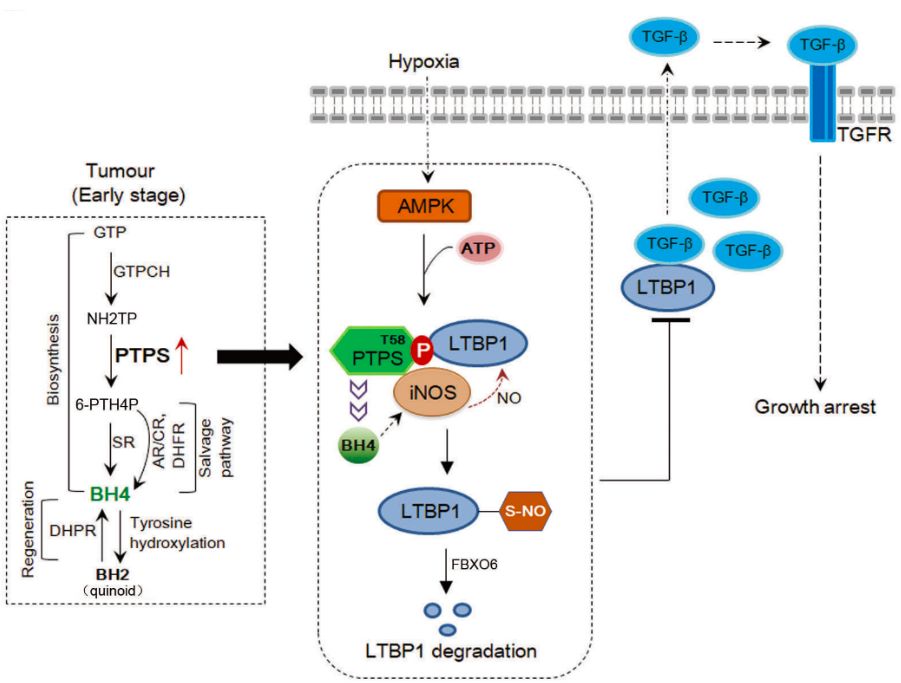
该项研究发现PTPS蛋白表达水平在早期大肠癌中明显升高。功能上,PTPS缺失以及酶活突变明显抑制了肿瘤细胞在低氧(hypoxia)条件下的生长,然而PTPS缺失对细胞造成的效应并不能有效地通过补充外源性BH4来缓解;这暗示着PTPS在介导BH4产生之外还通过未知的方式参与了细胞生长调节。
分子机制研究表明,低氧条件下AMPK介导了PTPS-Thr58磷酸化;此磷酸化促进了PTPS与LTBP1的结合,并且PTPS与LTBP1相互作用进一步促进了iNOS与LTBP1的结合。在iNOS-PTPS-LTBP1复合物中,PTPS介导的BH4产生促进了iNOS的活化即NO的产生,从而有效促进了LTBP1 S-亚硝基化以及导致相关蛋白酶体介导的LTBP1蛋白降解。护送TGF-β的分泌是LTBP1的主要生物学功能。
因此PTPS/iNOS介导的LTBP1下调最终可抑制了低氧条件下TGF-β的分泌以及TGF-β诱导的细胞生长抑制,从而维持了低氧条件下肿瘤细胞的生长。
以往已有研究报道大肠癌发展过程中伴随着TGF-β信号通路的抑制,比如TGF-βRI/TGF-βRII 和Smad4功能的丢失。然而,在失去TGF-β应答能力的肿瘤细胞中往往还存在着TGF-β分泌的功能。考虑到肿瘤的异质性,具有TGF-β分泌功能的肿瘤细胞会影响到TGF-β信号通路完整的肿瘤细胞以及微环境中基质细胞及免疫细胞等的功能。因此,该研究发现的PTPS抑制TGF-β分泌的功能也进一步整体上反映了TGF-β信号通路抑制对于早期大肠癌发展的必要性。
代谢物可以直接参与大分子修饰的化学反应,并且越来越多的证据表明代谢酶的不同状态可以灵活地调节代谢物的可用性。该研究发现了通过BH4生物合成途径调节LTBP1-TGF-β信号的潜在分子机制,并突出了PTPS对肿瘤生长的特殊作用。该研究确定的PTPS如何调节LTBP1的稳定性揭示了一种新的机制,即BH4生物合成相关的代谢酶在环境的刺激下,巧妙地发挥非代谢的病理生理作用。该研究将为开发肿瘤治疗的新策略提供有价值的理论基础。
据悉,上海交通大学医学院,癌基因及相关基因国家重点实验室,上海市第一人民医院蒋玉辉教授,复旦大学附属中山医院陈涛博士为本文共同通讯作者。助理研究员赵琴博士为本文第一作者。该研究得到了华东师范大学廖鲁剑教授和李大力教授的支持。
原文链接:
https://doi.org/10.1016/j.molcel.2019.09.018
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652476578&idx=2&sn=90a2d9531a75c99f05937aee1f27d0de&chksm=84e20716b3958e00697cef79b7666054b19054968c0f6d12c4a74dd32e219051f9ae66e4611c&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
中国抗癌协会肿瘤介入学专业委员会换届会议召开




发光纳米颗粒可以更快更精准地检测癌症

高广辉教授:什么是循环肿瘤细胞?为什么它能实现肿瘤早期发现、实时监测肿瘤治疗效果?
胸腔积液肿瘤细胞学检查

附属仁济医院团队发现死亡肿瘤细胞或助肿瘤"卷土重来"
胸腔积液肿瘤细胞学检查
Nat Commun:中性粒细胞或会促进肿瘤细胞死亡
中国抗癌协会肿瘤护理专业委员会在津成立



中国科大揭示肿瘤细胞代谢重编程与周期调控新机制

基于稀土纳米材料实现肿瘤细胞检测!