科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-10-30
来源:MedSci梅斯
导语:国家药品监督管理局(NMPA)已批准PD-L1单抗Tecentriq(atezolizumab)联合抗血管内皮生长因子(VEGF)单抗Avastin(贝伐单抗),用于未接受过全身性治疗、不可切除的肝细胞癌(HCC)患者。罗氏宣布,国家药品监督管理局(NMPA)已批准PD-L1单抗Tecentriq(atezolizumab)联合抗血管内皮生长因子(VEGF)单抗Avastin(贝伐单抗),用于未接受过全身性治疗、不可切除的肝细胞癌(HCC)患者。
图片来源:https://www.biospace.com/article/genentech-s-avastin-tecentriq-combination-gets-greenlight-for-liver-cancer/
罗氏首席医学博士Levi Garraway说:“全世界上近一半的肝细胞癌患者在中国,这项批准标志着中国肝细胞癌治疗的重大进展。”
中国临床肿瘤学会(CSCO)肝癌专家委员会主席秦叔逵教授说:“在中国,原发性肝癌是第四常见的恶性肿瘤,大多数中晚期患者诊断时已经不能选择手术或其他局部疗法,因此迫切需要新的治疗药物。IMbrave150研究表明,Tecentriq和Avastin联合使用可以显着改善患者的预后。该组合现在中国获批,为中国肝癌患者提供了新的选择。”
肝癌是中国最常见的癌症之一,每年诊断近40万例,约368,000例死亡,相当于每天超过1000例死亡。中国肝癌患者的平均5年生存率仅约15%。
该批准是基于III期IMbrave150研究的结果,在194名中国患者中的研究结果显示与索拉非尼相比,Tecentriq联合Avastin将死亡风险(总体生存率,OS)降低了56%,将疾病恶化或死亡的风险(无进展生存期,PFS)降低了40%。并且Tecentriq和Avastin具有良好的耐受性,毒性易于控制。
IMbrave150全球研究结果表明,与索拉非尼相比,Tecentriq与Avastin组合可使死亡风险(OS)降低42%,并将疾病恶化或死亡风险(PFS)降低41%。这些结果已于2020年5月14日发表在《新英格兰医学杂志》上。
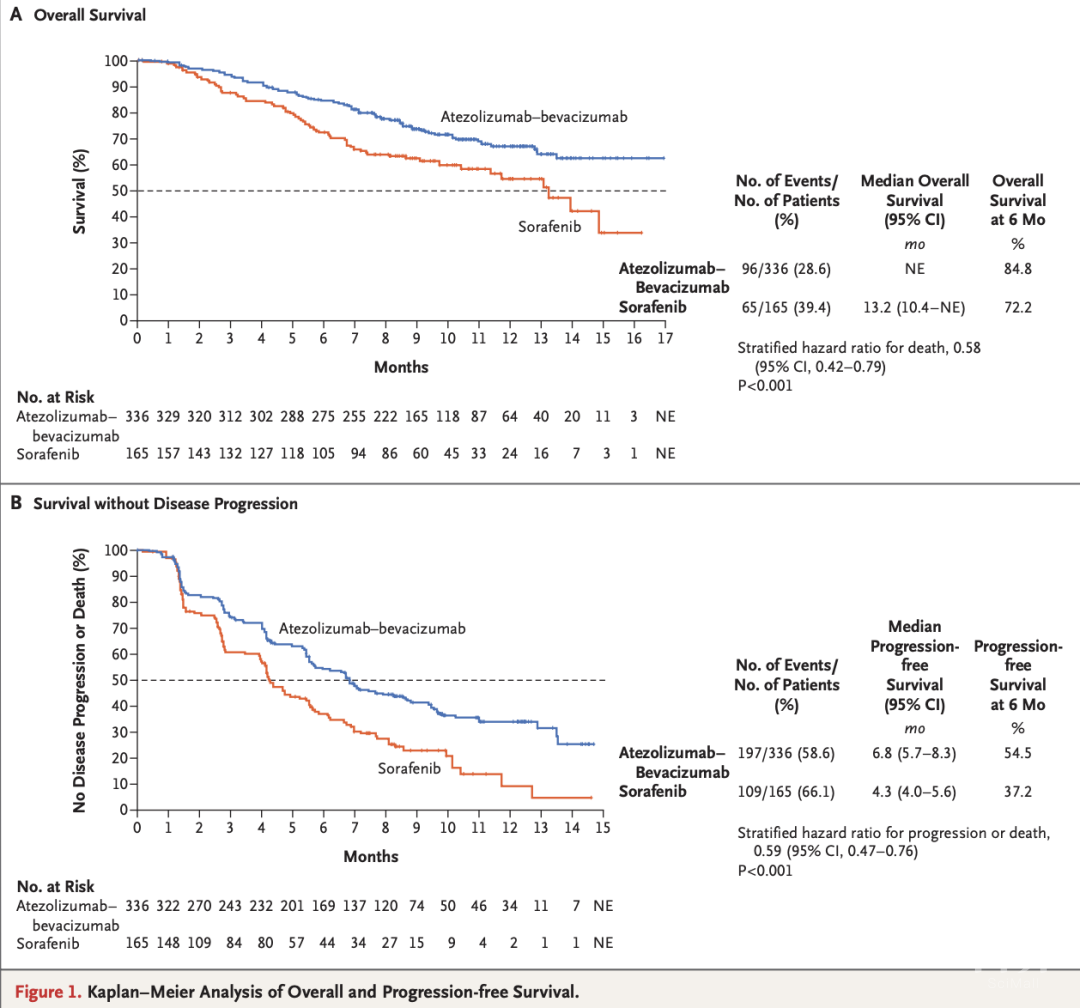
图片来源:Atezolizumab plus Bevacizumab in Unresectable Hepatocellular Carcinoma. N Engl J Med. 2020
原始出处:
https://www.firstwordpharma.com/node/1769169?tsid=4.
来源:MedSci_cn MedSci梅斯
原文链接:http://mp.weixin.qq.com/s?__biz=MzI0Njc5ODM4MQ==&mid=2247521840&idx=3&sn=ba6e7f6e5dd02c9f174cd7adfef4022d&chksm=e9bb1772decc9e64277cca96cae721a6defdc70ac65d7196ccecd48fc799d494184b49720fab&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
研究揭示鱼肝细胞脂肪聚积新机制
肝细胞是如何抵御病毒攻击的?
肝细胞损伤

Cell Metabolism:肝细胞和神经细胞一样老?
人肝细胞体外长期培养突破瓶颈

全球首例!“人胚胎干细胞来源”肝细胞治疗肝衰竭

肝细胞癌联合治疗中国专家共识发布

警惕!高果糖饮食促进肝细胞癌进展

【健康养生】警惕这7种炎症成为癌症帮凶!
肝细胞“逆生长”的分子调控基础获揭示