科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-04-07
最早分别在英国和南非发现的新冠病毒突变株B.1.1.7和B.1.351继续在欧美等地快速传播,针对野生病毒株设计开发的各种新冠疫苗能否有效防控这些突变株,愈发引起各国重视。
据央视新闻客户端等报道,在3月28日举行的国务院联防联控机制召开新闻发布会上,国药集团中国生物一位副总裁表示,"对包括在南非、英国发现的毒株"等10多株的毒株进行的实验显示,"灭活疫苗产生的中和抗体对这些毒株都有很好的中和作用"。而北京科兴中维生物技术公司总经理表示"整体的抗体水平武汉株和英国株基本没有差异,但是南非株的情况有些不同"。
今天凌晨,《新英格兰医学杂志》(NEJM)发表来自中国军事医学科学院微生物流行病研究所以及德州疾控中心等单位的论文,具体描述了两款国产疫苗对B.1.1.7和B.1.351突变株的中和抗体实验结果。
作者认为,疫苗接种者血清的中和活性对B.1.1.7无显著变化,而这两款疫苗接种者血清对B.1.351中和活性是对野生型的30%至50%。
需要强调的是,目前尚不清楚中和抗体水平与疫苗实际保护效力的关系。这项研究凸显持续监控病毒突变株的重要性。
流行SARS-CoV-2变异株对血清中和作用的敏感性
Susceptibility of Circulating SARS-CoV-2 Variants to Neutralization
Wang GL, Wang ZY, Duan LJ, et al.
DOI: 10.1056/NEJMc2103022
两种SARS-CoV-2变异株(英国的B.1.1.7和南非的B.1.351)出现后,人们担心它们可能逃逸人体因之前感染或接种疫苗而形成的免疫力。为了测定这些变异株对感染或疫苗诱导产生的中和作用的抗性,我们制备了含Wuhan-1参考株(野生型)、D614G突变、B.1.1.7或B.1.351变异株刺突蛋白的SARS-CoV-2假病毒,这些假病毒基于重组水疱性口炎病毒。(关于重组过程的详细信息见补充附录,补充附录与本文原文可在NEJM.org获取。)
随后,我们从感染Covid-19后5个月的34例已康复患者采集恢复期血清并从接种第二剂灭活疫苗(中国制造的BBIBP-CorV [国药]或克尔来福[科兴]疫苗)[1,2]后2~3周的50名参与者采集血清,并应用这些血清评估假病毒对中和作用的抗性(补充附录表S1)。我们首先测定了针对野生型假病毒的血清中和抗体滴度,在恢复期患者和疫苗接种者血清内观察到相似的几何平均滴度(GMT)(图1A),这提示接种两剂疫苗后,BBIBP-CorV和克尔来福疫苗诱导产生的抗体应答水平低[1,2]。值得关注的是,在34份恢复期血清样本中的4份、25份BBIBP-CorV血清样本中的6份和25份克尔来福血清样本中的4份中,中和抗体滴度不可测。
我们接下来评估了与对野生型假病毒中和活性相比,恢复期血清和疫苗接种者血清对D614G、B.1.1.7和B.1.351变异株的中和活性。与对野生型病毒的中和效力相比,恢复期血清对D614G假病毒的中和效力显著增强(2.4倍;95%置信区间[CI],1.9~3.0),对B.1.1.7变异株的中和效力相似,对B.1.351假病毒的中和效力显著减弱(0.5倍;95% CI,0.4~0.7)(图1B)。此外,30份恢复期血清样本中有9份对B.1.351完全丧失中和活性。
在BBIBP-CorV疫苗接种者血清样本中,尽管针对变异株的中和抗体GMT与针对野生型病毒的GMT无显著差异,但有20份血清样本对B.1.351完全或部分丧失中和活性(图1C)。在克尔来福疫苗接种者血清样本中,我们观察到针对B.1.1.7(0.5倍;95% CI,0.3~0.7)和B.1.351(0.3倍;95% CI,0.2~0.4)的血清中和抗体GMT明显降低。此外,大多数血清样本对B.1.351完全或部分丧失中和活性(图1D)。
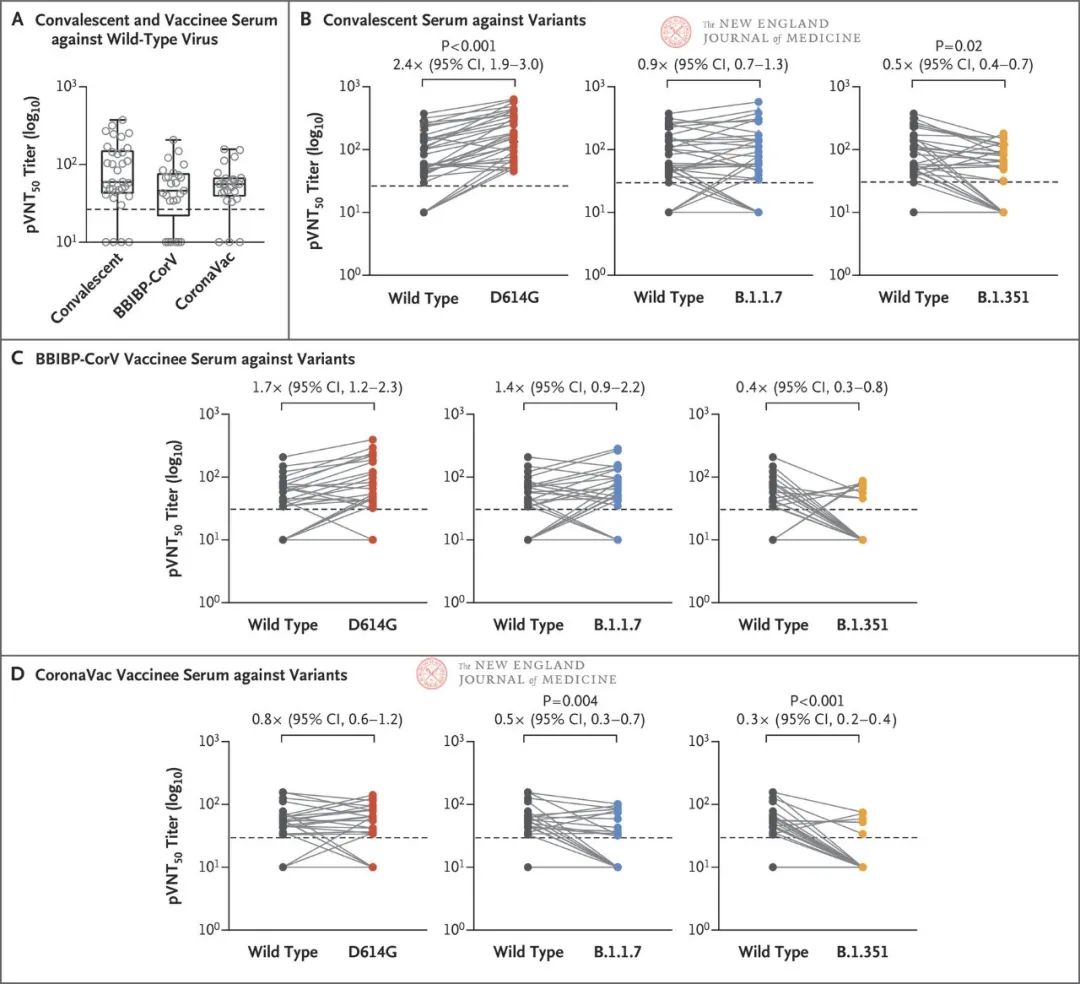
图1. 恢复期血清和疫苗接种者血清样本对SARS-CoV-2假病毒的中和活性。
图A显示了在感染SARS-CoV-2后约5个月的34例已康复患者的恢复期血清内,以及在接种第二剂疫苗(BBIBP-CorV或克尔来福疫苗)后2~3周的50名疫苗接种者的血清内,针对含Wuhan-1(野生型)刺突蛋白,并且基于重组水泡性口炎病毒的SARS-CoV-2假病毒的半数假病毒中和滴度(pVNT50)。箱线图显示了中位数和四分位距(IQR);胡须线代表IQR的1.5倍。图B显示了在34份恢复期血清样本内,与野生型病毒相比,针对D614G、B.1.1.7和B.1.351变异株的血清pVNT50的变化。图C和图D分别显示了在25名BBIBP-CorV疫苗接种者和25名克尔来福疫苗接种者的血清样本内,与野生型病毒相比,针对D614G、B.1.1.7和B.1.351变异株的pVNT50的变化。与野生型病毒相比,pVNT50滴度的几何平均滴度变化倍数和95%置信区间(CI)在P值下方显示。图中仅显示小于0.05的P值(表示达到显著性)。每个数据点均为重复测定得到的平均值。在各图中,水平虚线代表检测下限(滴度,<30);该检测限在几何平均值计算中被指定为10,并被视为血清反应阴性。所有图中的计算均在针对错误发现率校正后采用双侧Kruskal–Wallis检验法进行。
本研究的结果提示,B.1.1.7对恢复期血清或疫苗接种者血清的中和活性几乎无抗性,而B.1.351对恢复期血清(2倍)和(灭活)疫苗接种者血清(2.5-3.3倍)中和活性的抗性均超过野生型病毒对血清的抗性。本研究检测的大多数疫苗接种者血清样本丧失了中和活性,这一结果与近期对恢复期血清或者mRNA或BBIBP-CorV疫苗接种者血清中和活性开展的其他研究结果一致[3-5]。本研究的结果还凸显出在变异株流行地区持续监测病毒并评估疫苗保护效力的重要性。
参考文献
1. Xia S, Zhang Y, Wang Y, et al. Safety and immunogenicity of an inactivated SARS-CoV-2 vaccine, BBIBP-CorV: a randomised, double-blind, placebo-controlled, phase 1/2 trial. Lancet Infect Dis 2021;21:39-51.
2. Zhang Y, Zeng G, Pan H, et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18-59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. Lancet Infect Dis 2021;21:181-192.
3. Huang B, Dai L, Wang H, et al. Neutralization of SARS-CoV-2 VOC 501Y.V2 by human antisera elicited by both inactivated BBIBP-CorV and recombinant dimeric RBD ZF2001 vaccines. February 2, 2021 (https://www.biorxiv.org/content/10.1101/2021.02.01.429069v1. opens in new tab). preprint.
4. Liu Y, Liu J, Xia H, et al. Neutralizing activity of BNT162b2-elicited serum — preliminary report. N Engl J Med. DOI: 10.1056/NEJMc2102017.
5. Wang P, Nair MS, Liu L, et al. Antibody resistance of SARS-CoV-2 variants B.1.351 and B.1.1.7. Nature 2021 March 8 (Epub ahead of print).
来源:NEJM-yixueqianyan NEJM医学前沿
原文链接:http://mp.weixin.qq.com/s?__biz=MzIxNTc4NzU0MQ==&mid=2247501439&idx=1&sn=c202538cedb68d3a32e2f8d955775831
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

“德尔塔+”惊现!传播力更强!感染者已接种疫苗→
未接种疫苗者病亡率为完全接种者11倍
SARS-CoV-2 D614G突变株高侵染性的结构基础
艾滋病病毒(HIV)感染者能接种疫苗吗?
广东发现新型冠状病毒尼日利亚突变株
【科普生活】官方明确!事关"未接种新冠疫苗者"
【全民战疫】官方明确!事关“未接种新冠疫苗者”
国外研究称疫苗接种者不易出现长期新冠症状

不打疫苗不能出门!奥地利对未接种疫苗者实施“封禁”

科普·防疫 | 紧急通告!未接种新冠疫苗者,将影响出行!