科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-12-15
来源:BioArt
社交包括一系列复杂的互动行为,可以是合作的、中立的,也可以是对立的。社交可以促进互利的结果,如劳动分工、合作照顾和提高免疫力,当然社交也可以导致消极的结果,包括侵略和胁迫。在五彩缤纷的“动物王国”中,动物们表现出的社交能力是不同的:有些动物生活在高度社会化的合作团体中,如灵长类、白蚁和蜜蜂,而另外一些则趋于独居,如熊。
1973年,Konrad Lorenz、Niko Tinbergen和Karl von Frisch因在哺乳动物的遗传起源、发育和社会行为模式启发方面的开创性研究而获得诺贝尔生理学或医学奖,他们的工作为评估影响社会行为的各种内在和外在因素提供了基础。无数研究者的努力,让我们意识到,深入而全面地去理解调节社会行为的内在和外在因素,对于揭示个体和群体的繁荣发展方式、确定物种进化过程中出现的不同动物之间的交际能力差异的原因、甚至对于阐明社会行为障碍疾病的潜在病因都是极其重要的。
在临床上,发现了一些有趣的现象:约50%以上患功能性消化疾病者伴有焦虑、抑郁,当给予精神类药物治疗后,多数会取得较好的治疗效果;而精神心理疾患的诱发或加重也与消化系统疾病有关【1】。基于此现象并经过多年研究,科学家们逐渐提出了“脑-肠轴”及“脑-肠互动”的概念。“脑-肠轴”由中枢和肠神经系统之间的双向通信组成【2】,随着对肠道微生物组成和多样性的理解,新的发现表明肠道微生物群可以通过“脑-肠轴”与肠脑功能以及神经疾患相关联,进而形成了“微生物-肠-脑轴”这一新的概念【3】。相较于传统“脑-肠轴”研究集中在心理状态对胃肠道功能的影响而言,在“微生物-肠-脑轴”中则更加关注肠道菌群与“脑-肠轴”之间的相互影响。肠道菌群对“脑-肠轴”最重要的影响主要体现在对大脑发育和行为表现的调节上【4】,越来越多的研究发现了动物大脑的社交行为与微生物之间的复杂关系,提示微生物作为传播自身遗传物质的一种手段,可能影响了大脑社交行为的进化过程,那么,肠道菌群到底是如何影响社交行为的呢?
近日,来自爱尔兰科克大学的John F. Cryan教授团队在Science上发表题为Microbiota and the social brain的综述,详细总结了肠道微生物群和大脑社交行为之间的联系的潜在机制,并描述了动物世界中这种联系的多样性,同时指出这些联系可能有助于解释肠道菌群与社交障碍之间相关的原因,以及如何将其作为靶标以影响大脑健康。

一、“微生物-肠-脑轴”的作用机制
越来越多的实验证据表明,在各种动物中观察到的许多行为反应可能在其生命的不同阶段受到肠道菌群的调节,在这种模式下,人们越来越重视阐明肠道菌群与大脑沟通的机制,本文作者从以下几个方面介绍了微生物影响社会行为的交流途径(图1)。
1. 迷走神经
迷走神经是哺乳动物脑干中连接胃肠道与孤束核的主要神经通路。通过迷走神经切断术等方法,迷走神经传入最近被证明与肠内内分泌细胞形成突触连接,通过谷氨酸神经传递促进肠与大脑之间的营养信号交流,甚至有临床前的证据表明迷走神经能够将蛋白质从肠道运输到大脑。但是,也有实验发现,迷走神经切断术后,轻度胃肠道感染引起的小鼠焦虑样行为明显,这也提示并不是所有到达大脑的微生物信号都是由迷走神经介导的。
2. 微生物代谢产物
肠道菌群能够产生大量的代谢物,如挥发性羧酸、酯类、神经递质(如血清素)和各种脂肪酸,其中一些被证实可以影响大脑的生理机能和行为。例如,肠道菌群产生的各种短链脂肪酸(SCFA)代谢物可以通过它们的同源自由脂肪酸受体(FFAR)调节各种生理功能,包括某些中枢生理过程,此外,SCFA也可能通过调节参与其生物合成的酶的表达来影响大脑中神经递质的产生。当然,作者同时也指出,由于SCFA的半衰期很短,我们需要更多的证据来确定肠道菌群产生的SCFA能够到达大脑的生理相关浓度。
3. 免疫机制
研究表明,免疫在介导肠道菌群和大脑之间的交流中也起着至关重要的作用。一些临床前的证据表明,肠道菌群可能会影响免疫系统甚至中枢神经系统的发育。一方面,肠道菌群可在局部影响免疫系统,如派尔集合淋巴结(Peyer patch)或肠系膜淋巴结;另一方面,细菌也可以释放各种免疫激动剂,如脂多糖(LPS)和肽聚糖(PGN)进入血液循环,从而进入大脑。
4. 嗅觉机制
嗅觉——感知气味的能力,是地球上所有动物生命的基础,它使动物能够探索食物并感知环境中潜在的毒素,还有助于社交互动。初步证据表明,肠道细菌和环境细菌都能影响嗅觉,在整个动物界,通过嗅觉进行的肠道菌群和大脑之间的联系越来越受到重视,这些物种利用肠道微生物的副产品,如挥发性脂肪酸和酯类来调节交流。
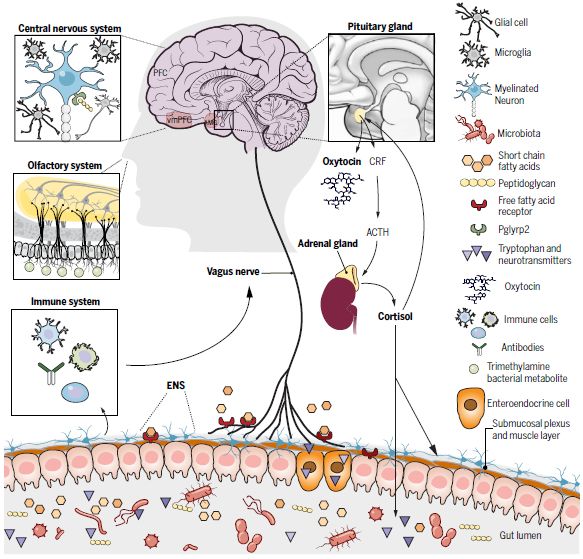
图1 肠道菌群调控社会行为的生物学途径
二、微生物和社交行为之间存在着双向关系
1. 社交性
社交行为可以影响许多无脊椎动物物种之间的菌群传播,也可以通过细菌的水平转移来塑造许多灵长类动物的微生物群,同时研究发现,在不同物种之间也可以发生微生物转移。但是作者也指出,虽然肠道菌群的变化似乎与某些物种的社交性同步变化,但情况并非总是如此,这可能是不同的选择压力导致的不同的进化过程在起作用,因此表明在寻找微生物的社交性特征时需要考虑系统发育的影响。
2. 交流
研究表明,对于一些无脊椎动物,肠道菌群可以促进同种个体之间的交流,同时,微生物群也有助于某些脊椎动物物种之间的交流,而某些物种的微生物群可能起着鉴别同种物种的作用。
3. 社会免疫力
集体生活提供了广泛的潜在好处,但它也伴随着许多代价,包括接触传染媒介风险的增加。然而研究发现,暴露于具有社会性的感染源的威胁的增加可以被微生物群多样性的增加所抵消,这使得免疫系统能够与微生物群协同工作,以抵御有害微生物。免疫和宿主对入侵病原体的反应也可能对社会行为的微生物基础产生影响,因为免疫系统通过各种免疫信号机制充当肠道共生细菌和中枢神经系统之间的管道。
4. 饮食和压力
本文作者提出,社会性对动物行为的积极影响通常伴随着一系列负面影响,比如社会压力,它会导致健康和生育能力下降,增加对疾病的易感性,从而影响物种的整体健康。虽然社会交往可能通过增加压力对肠道微生物群有害,但它们也可能是有益的,而这之间的平衡似乎在很大程度上依赖于社会关系。与此同时,草食性或肉食性饮食及其对肠道菌群组成的影响也可能影响了某些物种的社会行为的进化。
三、肠道菌群和社交障碍
社会行为缺陷表现在孤独症谱系障碍(ASD)、精神分裂症、社交焦虑和抑郁等神经精神疾病中,患者要么无法与他人互动,要么退出社交活动。考虑到微生物群和大脑社交行为在动物世界中复杂的、双向性的影响,肠道菌群在人类社交障碍中扮演重要角色的证据越来越多也就应该不是一件奇怪的事了。有趣的是,一些临床前和临床研究记录了患有这些神经精神疾病的个体中胃肠微生物群的紊乱(包括细菌多样性的减少和有益细菌数量的减少),而这种失调可能与观察到的行为症状有关。越来越多的临床发现表明肠道菌群在诸如ASD条件下受到了影响,本文作者也指出,未来的研究需要统计更多的患者并引入适当的控制,这将可能会对肠道菌群在这类疾病中的致病机制提供更深入的了解。
四、靶向微生物群治疗社交障碍
微生物群和社交障碍之间的联系表明,以微生物群为目标极有可能可以改善社会行为中的缺陷。基于微生物的治疗策略已经在各种临床前模型中显示了其改变社交行为的潜力,一些初步证据也表明了其对人类的影响,例如益生菌和饮食结构对肠道菌群的调节都将影响社交行为。
综上所述,肠道菌群对社交性及其神经生物学基础的影响对生态学、进化论和人类生物学具有潜在的巨大影响。微生物群和中枢神经系统之间的这种联系提供了一个生物学框架,用以阐明在整个动物界中,从群居性到非群居性的复杂行为模式是如何进化而来的,此外,它提出了关于某些生活方式的选择(如饮食、抗生素使用、社会关系等)对人类健康的影响的重要考虑,同时也有助于对某些神经精神疾病的神经生物学基础和未来治疗的潜在发展提供了一个更好的理解。
原文链接:
https://science.sciencemag.org/content/366/6465/eaar2016
参考文献
1. 郭椿,贺平. 脑肠轴及其研究进展. 世界最新医学信息文摘. 2017,17(95),89-91.
2. Marilia Carabotti, Annunziata Scirocco, Maria Antonietta Maselli et al. The gut-brain axis: interactions between enteric microbiota, central and enteric nervous systems. Annals of Gastroenterology (2015) 28, 203-209.
3. Clarke G, Dinan T, Cryan J.Microbiome–Gut–Brain Axis[M]. Encyclopedia of Metagenomics, 2013:425-437.
4. Chen X, D'Souza R, Hong ST. The role of gut microbiota in the gut-brain axis: current challenges and perspectives. Protein Cell. 2013 Jun;4(6):403-14.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652478910&idx=1&sn=30d2e5e9fb4cec96e6a14d54ef9b99f2&chksm=84e20e0ab395871c42fbca8d1aa290f5584751ae7de89062cf1808811668c0aa720a72daab26&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

如何能让大脑更好地控制假肢?科学家在探索道路上再进一步

阳光照射可改变肠道微生物菌群
科普:夫妻相真的与细菌有关吗?




首发嘉宾阵容 | GMR 2021聚焦肠道菌群/微生物组学/FMT/LBP转化与产业化!
郭浩等揭示肠道微生物菌群和代谢产物在电离辐射模型中的保护作用

你看视频时在想什么?人工智能助力解码大脑

DARPA新大脑设备可改善认知功能,学习速度提高40%
新突破:肠道微生物菌群可用于诊断肝脏疾病
肠道微生物也挑食?Cell:蛋白质组学揭示肠道菌群种间竞争对饮食纤维的选择性机制
生物学: 咖啡害虫的致命弱点