科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-07-22
严重的认知能力下降是阿尔茨海默病 (AD) 的标志。除了灰质丢失,在 AD 患者中还发现了显著的白质病变。
2021年6月7日,陆军军医大学梅峰,肖岚及美国加州大学旧金山分校陈儒育(Jonah R. Chan)共同通讯(陈婧菲、刘坤及胡波为本文第一作者)在Neuron 在线发表题为“Enhancing myelin renewal reverses cognitive dysfunction in a murine model of Alzheimer’s disease”的研究论文,该研究表征了 AD 的 APP/PS1 小鼠模型中髓鞘生成和丢失的动态。
出乎意料的是,该研究观察到 APP/PS1 小鼠中新髓鞘形成率的显著增加,让人联想到少突胶质细胞对脱髓鞘的强烈反应。尽管有这种增加,APP/PS1 小鼠的皮层和海马以及死后 AD 组织的髓鞘形成总体水平下降。通过少突胶质细胞缺失毒蕈碱 M1 受体或全身给药促髓鞘形成药物氯马斯汀,在遗传或药理学上增强髓鞘更新,改善了 APP/PS1 小鼠在记忆相关任务中的表现。总之,这些结果证明了增强髓鞘形成作为减轻 AD 相关认知障碍的治疗策略的潜力。

阿尔茨海默病 (AD) 是一种与年龄相关的神经退行性疾病,表现为进行性认知能力下降,有效的治疗方法仍然难以捉摸。尽管 AD 相关的认知障碍被认为是神经元功能障碍和退化的结果,但也有报道称AD 患者神经胶质功能受到严重破坏。特别是,组织学和功能成像研究发现 AD 患者的白质结构发生了显著变化。白质由轴突和髓鞘组成,髓鞘是由少突胶质细胞产生的脂肪鞘,可增加轴突传导性,对神经元信号传导至关重要。这些白质异常是否积极促成 AD 的症状和/或进展,或者只是继发于神经元变性,目前尚不清楚。
少突胶质细胞和它们产生的髓鞘包裹轴突以优化传导速度,并为神经元提供生存所需的众多代谢和营养因子。成熟的少突胶质细胞和单个髓鞘一旦生成,在成人和老化的大脑中大多是稳定的。然而,最近的研究表明,新的髓鞘是通过一生中少突胶质细胞前体细胞 (OPCs) 的分化不断产生的。在衰老过程中,髓鞘生成显著减少,这似乎是导致老年小鼠认知功能下降的原因。这些发现提出了一种可能性,即改变的髓鞘动力学可能是 AD 患者出现认知缺陷的部分原因。
多条证据表明,髓鞘和少突胶质细胞在 AD 相关病理学中发生了显著改变。单细胞转录组学分析检测到早期 AD 患者大脑中少突胶质细胞谱系细胞的显著基因表达变化,并且在 AD 模型大脑中发现了髓鞘异常。例如,Aβ 沉积导致 OPCs 局灶性脱髓鞘和衰老样变化,而转基因 AD 小鼠大脑中 OPC 增殖的平均速率增加,暗示异常髓鞘变性和髓鞘再生可能发生在 AD 大脑中。因此,了解与 AD 相关的髓鞘动态变化可能需要遗传细胞谱系追踪,以跟踪预先存在和新形成的髓鞘随时间的变化。
在这里,该研究报告了预先存在的髓鞘的加速退化,这与 APP/PS1 转基因小鼠大脑中少突胶质细胞生成和髓鞘形成的显著增加相吻合,导致净髓鞘丢失。通过删除 OPCs 中的毒蕈碱受体 (M1R) 或用促髓鞘药物氯马斯汀治疗来增强髓鞘更新,显著改善了 APP/PS1 小鼠在记忆相关任务中的表现,并增加了海马尖波的发生率和尖波涟漪波 (SPW-R)。总之,这些结果证明了增强髓鞘形成作为改善 AD 相关认知障碍的治疗策略的潜力。
来源:iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247531166&idx=7&sn=a0cd947996e60e2701d0ee62e84bd730
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
记忆是什么?能吃吗?小胶质细胞:能!
《细胞》发文!阿片类药物迎来重大突破

胶质细胞参与调节视网膜自发活动波

人工细胞与生物细胞首次实现成功融合与协作
脑脊液髓鞘碱性蛋白
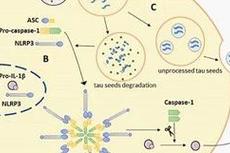
最新综述:小胶质细胞如何影响Tau病理?

尼古丁能改变小胶质细胞特性
少突胶质细胞

Neuron:mRNA m6A甲基化修饰参与少突胶质细胞发育以及中枢系统髓鞘形成

天价冬虫夏草能否抗癌成“罗生门”