科技工作者之家
加好友
科技工作者之家 2021-10-13
T 滤泡辅助 (Tfh) 细胞在调节体液免疫,尤其是生发中心反应方面发挥着重要作用。然而,CD4+ T 细胞如何在 Tfh 细胞发育中整合抗原和共刺激信号仍然知之甚少。
2021年10月12日,清华大学董晨团队在Immunity 在线发表题为“Costimulation molecules differentially regulate the ERK-Zfp831 axis to shape T follicular helper cell differentiation”的研究论文,该研究发现佛波醇 12-肉豆蔻酸酯 13-乙酸酯 (PMA) + 离子霉素 (P+I) 刺激与白细胞介素 6 (IL-6) 一起在体外有效诱导 Tfh 细胞样转录组程序。
ERK 激酶通路在 P+I 刺激下减弱;ERK2 抑制增强了体外和体内 Tfh 细胞的发育。该研究观察到诱导型 T 细胞共刺激物 (ICOS),而不是 CD28,缺乏激活 ERK 的能力,这对于维持 Tfh 细胞发育很重要。转录因子 Zfp831 的表达被 ERK 抑制,通过直接上调转录因子 Bcl6 和 Tcf7 的表达来促进 Tfh 细胞分化。因此,该研究确定了 ERK-Zfp831 轴,受共刺激信号调节,在 Tfh 细胞发育起关键调节作用。

在免疫反应中,T 细胞为 B 细胞提供帮助,有助于生存、增殖、类别转换和亲和力成熟。表达 CXCR5 的 CD4+ T 滤泡辅助 (Tfh) 细胞位于生发中心,首先被假设为辅助 T 细胞亚群,随后将 Bcl6 的表达定义为它们的谱系特异性转录因子 (TF)。Tfh 细胞是针对各种病原体的体液免疫所必需的。
在淋巴细胞脉络丛脑膜炎病毒 (LCMV) 模型中,Tfh 细胞通过促进中和抗体的产生来帮助控制慢性病毒感染。通过调节抗体产生和 B 细胞记忆形成,Tfh 细胞在对流感疫苗的免疫反应中也是必不可少的。过度的 Tfh 细胞反应可能导致自身免疫性疾病,例如系统性红斑狼疮 (SLE) 和风湿性疾病。
Tfh 细胞的发育和功能已被证明受各种 TF 的调节。虽然 Bcl6 是 Tfh 细胞反应中的谱系特异性 TF,但其功能被 TF Blimp1 抑制,Bcl6-Blimp1 轴决定了 Tfh 和非 Tfh 细胞发育的分叉点。TF Ascl2,而不是 Bcl6,诱导 Cxcr5 趋化因子受体表达并在早期 Tfh 细胞迁移中发挥重要作用。同时,T 细胞抗原受体 (TcR) 信号通过 TFs BATF 和 IRF4 调节 Tfh 细胞分化。BATF 在 T 细胞极化过程中作为多功能 TF 发挥作用,通过诱导 Bcl6 和 Rorc 的表达,对于 Tfh 和 T helper-17 (Th17) 细胞的生成都是必需的。Irf4-/- CD4+ T 细胞无法在体内产生 Tfh 细胞。
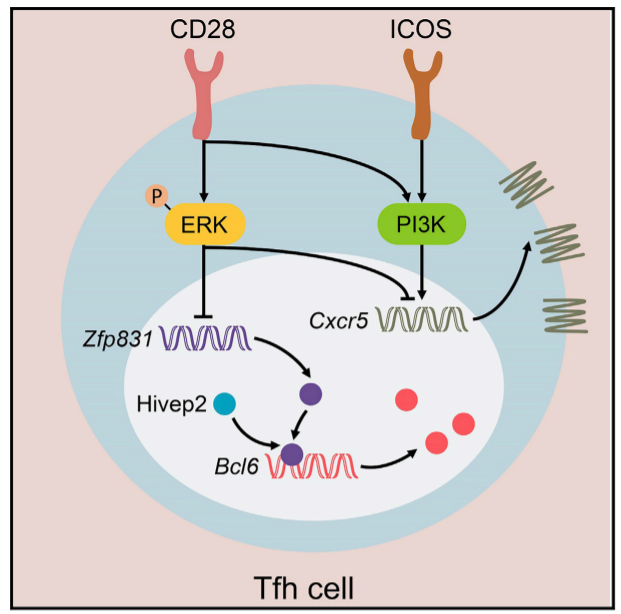
文章模式图(图源自Immunity )
此外,白细胞介素 (IL)-6-STAT3 对启动 Tfh 细胞发育至关重要。Tox2 是 IL-6 下游的 TF,可促进 Bcl6 和 Cxcr5 的表达。Tfh 细胞选择性表达 TF TCF1,它在 LCMV 感染模型中正调节 Bcl6 的表达。同时,TF Foxo1 和 Bach2 直接抑制 Bcl6 表达并限制 Tfh 细胞形成。所有这些 TF 形成了一个网络,可以精细地调节 Tfh 细胞的分化。
CD4+ T 细胞分化受细胞因子控制。IL-6 和 IL-21 先前已被报道在 Tfh 细胞的产生中具有重要性。相反,IL-2 和 IL-7 可有效抑制 Tfh 细胞发育。此外,据报道,与 IL-6 共享 gp130 共受体亚基的 IL-27 可诱导 Tfh 细胞中的 IL-21 表达,从而促进其分化。
TcR 和共刺激在 T 细胞分化中也很重要。据报道,弱 TcR 强度有利于 Tfh 细胞生成,但这种观点受到了其他人的挑战。最近的一份报告表明,弱 TcR 信号促进 Tfh 细胞分化。Tfh 细胞分化需要诱导型 T 细胞共刺激因子 (ICOS) ,属于 CD28 共刺激家族。CD28 和 ICOS 差异调节 Tfh 细胞发育:CD28 对 Tfh 细胞发育的早期阶段很重要,而 ICOS 在维持 Tfh 细胞发育方面是必要的。CD28 和 ICOS 共享一个共同的下游 PI3K 信号通路。
Tfh 细胞中的 PI3K 激活介导 CXCR5 表达及其正确定位。ICOS 激活 PI3K 已被证明是支持 Tfh 细胞发育的必要条件。此外,已发现 ICOS 中的 IProx 基序特异性募集 TBK1 激酶,这是 Tfh 细胞生成所必需的。另一方面,生长因子受体结合蛋白 2 (Grb2) 可以被 CD28 募集,但不是 ICOS,以激活 ERK 途径。在嵌合抗原受体 (CAR) 中用 ICOS 的胞内结构域替换 CD28 的胞内结构域会损害其激活 ERK 通路的能力;然而,目前尚不清楚这种差异效应是否会影响 T 细胞分化。
在这项研究中,探索了 Tfh 细胞分化过程中的信号机制。该研究表明 ERK 负向调节 Tfh 细胞分化。ICOS 不能像 CD28 那样激活 ERK,这在 Tfh 细胞生成中很重要。该研究还发现了一个受 ERK 通路负调控的 TF Zfp831,它直接与关键的 Tfh 细胞特征基因结合并起到调节 Tfh 细胞分化的作用。因此,这项研究揭示了 Tfh 细胞发育的信号机制,这对自身免疫疾病具有影响。
来源:iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247537568&idx=5&sn=1ecf1a249bd6b27413dc7a8380597964
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Science:揭示一类Tfh细胞通过分泌SOSTDC1-WNT拮抗剂
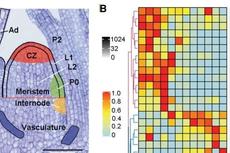
Genome Research 玉米干细胞(SAM)miRNA动态调控

天价冬虫夏草能否抗癌成“罗生门”

发现内耳干细胞调控新机制
《细胞》发文!阿片类药物迎来重大突破

学术造假必遭严惩,为何仍不断有人冒险

“促癌黑手”Ter细胞首次发现
玉米干细胞(SAM)miRNA动态调控

董晨团队《Immunity》发文报道Tfh细胞分化调控新机制

人体细胞内存在“铁路”系统,能自动优化结构