科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-03-26
近日,来自日本东京理工学院的科学家们在eLife杂志上发表论文称,他们发现了修复DNA双链断裂的重要机制。这将有助于我们理解DNA修复失败导致遗传疾病和癌症的原因。
DNA双链断裂会导致严重的DNA损伤,这种损伤可被同源重组(HR)修复。一种名为Rad51的蛋白质控制着HR过程,而Rad51自身则由几个辅助蛋白质支持。
“其中一组辅助蛋白可以被分成两个模块,每个模块有不同的作用。在这项研究中,我们想要了解模块1如何与Rad51相互作用,以及两个模块如何协作打开Rad51。”论文的第一作者、日本东京理工学院的高级研究员Bilge Argunhan说。
为了探究以上问题,研究人员首先通过基因工程改造了酵母细胞,敲除了Rad51的辅助蛋白——Swi5-Sfr1中的模块1或模块2,结果发现,HR修复DNA的效率下降,这表明Rad51需要两个模块来启动HR修复。
接下来,为了识别模块1中与Rad51结合的精确区域,研究人员从细胞中纯化了Swi5-Sfr1蛋白,然后,通过改变蛋白质序列修改了这些区域,阻止了Swi5-Sfr1与Rad51的结合。
结果发现,尽管突变的Swi5-Sfr1不能在体外打开Rad51,但包含这些突变的酵母仍然能够修复DNA。研究小组认为,可能是体内的另一组辅助蛋白启动了DNA的修复过程。
先前的遗传学研究表明,酵母中存在两种HR子通路,一种依赖于Swi5-Sfr1,另一种依赖于Rad51旁系同源分子。
为了确定另一种HR子通路是否在Swi5-Sfr1突变的酵母中拯救了DNA修复,研究人员使用了缺乏Rad51旁系同源分子的酵母进行Swi5-Sfr1突变。结果发现,在含有Swi5-Sfr1突变体伴Rad51旁系同源分子缺失的酵母中,DNA的损伤更加严重。这表明第二组辅助蛋白抑制了突变对Swi5-Sfr1辅助蛋白的破坏作用。
“虽然这两组辅助蛋白之前被认为是独立起作用的,但我们的研究表明,它们实际上共同激活了DNA修复中的Rad51。DNA修复的基本机制在酵母和人类中高度保守,因此我们的工作可以帮助理解人类相关疾病中DNA修复失败的原因。”东京理工学院教授、通讯作者Hiroshi Iwasaki解释说。
科界原创
编译:花花
审稿:alone
责编:张梦
期刊来源:eLife
期刊编号:2050-084X
原文链接:
https://phys.org/news/2020-03-scientists-reveal-proteins-team-dna.html
版权声明:本文由科界平台原创编译,中文内容仅供参考,一切内容以英文原版为准。转载请注明来源科技工作者之家—科界App。
细胞修复DNA损伤新机制揭示
Nature Cell Biology:相分离可调控DNA损伤修复


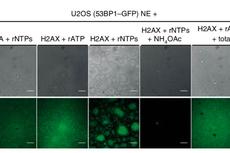

科学家探索物种间DNA组成多样性背后的奥秘

新研究揭开人类头发曲直的秘密
DNA修复之谜

DNA机器人一小步 癌症治疗一大步

DNA到底能不能预测外貌?

生态环境中心在DNA损伤修复研究方面取得重要进展
NCB:相分离可调控DNA损伤修复
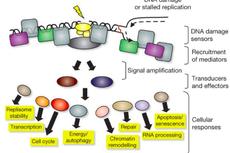

中科院生态中心DNA损伤修复研究取得进展