科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-03-31
来源:X一MOL资讯
细菌抗药性的出现与扩散严重威胁全球公共卫生安全。应对这一挑战亟需开发新型抗菌物和抗菌疗法。窄谱抗菌物/疗法可特异性地识别并清除目标病菌,从而减少对宿主共生菌群的脱靶干扰、并降低对细菌的抗药性进化压力。但是,由于区分病菌与益生菌的固有难度、以及制药公司对窄谱抗菌缺乏投资热情(出于成本-收益平衡考虑,他们自然地希望能开发一个可以杀灭所有细菌的抗菌物),窄谱抗菌物/疗法的发展一直处于极度迟滞状态。针对这一问题,中国科学技术大学阳丽华副教授课题组提出赋予现有的广谱抗菌物/疗法以辨别目标细菌的能力,从而将其转变成一种窄谱抗菌物/疗法。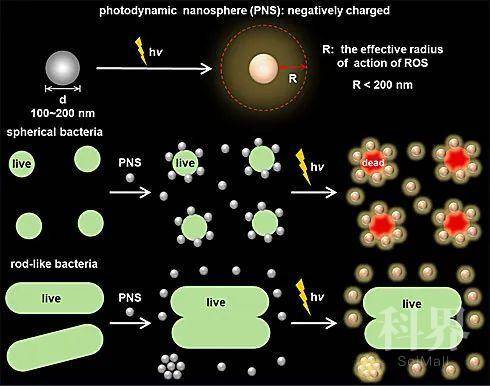
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657631611&idx=6&sn=562d2b0a6bcab7882589df1bea980a5c&chksm=80f814abb78f9dbd8792373362aff103d03263df8466b995537bcedd9a3287c15d0f8aea94c3&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
科学家首次观测到小鼠免疫系统识别入侵细菌全过程

中国微米纳米技术学会第十八届学术年会暨微系统与纳米工程高层论坛
第一届纳米纤维素材料国际研讨会在杭州召开



中国—奥地利纳米科技及新材料研讨和对接洽谈会在深圳举行




【走近桂籍科学家】用纳米武装电池新世界

中国科学家合成新型纳米发光材料有望用于肿瘤光动力治疗等

合工大研发智能水凝胶,一分钟实现96%的自修复

独家原创|调纳米材料在光动力疗法肿瘤治疗中的应用进展
国家纳米中心在上转换光动力治疗领域取得进展
中国科学家研发出新型纳米发光材料助力肿瘤光动力治疗