科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-08-08
来源:BioArt
“逆生”(paligenosis)是一种保守的细胞再生过程,是已分化的成熟细胞通过改变能量代谢逆向分化获得干细胞特性并重新进入细胞周期进而修复组织损伤的过程【1,2】。逆生可在多种器官损伤修复过程中触发,例如一些癌前疾病(胃解痉多肽表达型化生, Spasmolytic Polypeptide-Expressing Metaplasia, SPEM和胰腺腺泡导管化生Acinar-to-Ductal Metaplasia, ADM【3,4】)及神经元再生、两栖动物断肢再生等【5】。
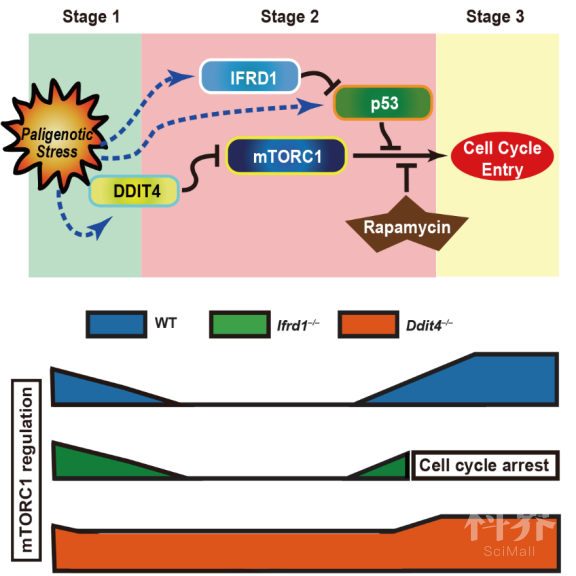
中国医科大学王振宁教授课题组在已在前期研究中【1】根据细胞形态及关键能量代谢调控蛋白复合物mTORC1活性变化,将逆生过程分为如下三个阶段:第一阶段:mTORC1失活,溶酶体增生和细胞自噬积蓄能量并清除受损细胞器;第二阶段:细胞开始表达一系列干细胞相关基因(如SOX9,KLF4,GSII等);第三阶段:mTORC1重新激活,细胞进入细胞周期1。溶酶体激活及mTORC1重新升高分别是第一阶段→第二阶段及第二阶段→第三阶段的关键调控点。
为了阐明逆生过程中的关键分子调控机制,2020年8月7日,王振宁教授(通讯作者)、苗智峰副教授(第一作者)课题组(中国医科大学胃肠肿瘤精准诊疗教育部重点实验室)与Jason Mills教授(通讯作者)课题组(圣路易斯华盛顿大学医学院胃肠病学部)联合在Developmental Cell上发表题为“A dedicated, evolutionarily conserved molecular network licenses differentiated cells to return to the cell cycle”的封面文章,利用多种转基因动物模型,首次详细阐述了DDIT4-IFRD1-p53-mTORC1轴触发并调控逆生发生的分子机制。

课题组首先对小鼠多种器官损伤-再生模型的高通量数据进行分析,发现逆生过程潜在关键调控基因Ifrd1和Ddit4。在果蝇中肠损伤、鼠神经元再生、肝脏再生等模型中均发现IFRD1可促进损伤细胞逆生后进入细胞周期,完成组织修复。进一步应用基因敲除小鼠及类器官模型证实IFRD1缺失可将逆生阻断于第三阶段,无法完成增殖过程。通过构建Ifrd1−/−;Trp53−/−双基因敲除动物模型,发现在小鼠胃主细胞及胰腺腺管细胞中IFRD1缺失可通过增加乙酰化稳定p53,进而抑制mTORC1活性使逆生进程阻滞。课题组进一步探究了DDIT4在逆生起始阶段的作用,发现DDIT4在正常小鼠胃主细胞及逆生早期表达上调,在逆生第一阶段抑制mTORC1活性、激活溶酶体功能并诱发自噬,Ddit4缺失将导致未经p53-mTORC1检查点筛选的逆生细胞更早的进入逆生第三阶段,进而增加DNA损伤累计及增加基因组不稳定性的风险,而mTORC1抑制剂雷帕霉素(Rapamycin)可显著抑制Ddit4−/−表型。
逆生是损伤应激状态下细胞再生的核心事件,异常逆生可能是肿瘤发生的潜在机制之一,深入探索逆生的触发及调控机制将为阻断肿瘤发生及细胞病理性再生提供新的靶点。
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652495022&idx=4&sn=f826680251a910acbffbee7b65caf9f3&chksm=84e24f1ab395c60cf2c66e46c8f384406da62047b25ca6fccae371ed41a0d4ed74eecc11edc6#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

NCB:蛋白激酶N调控溶酶体膜脂转换从而协调mTORC1的营养感知通路
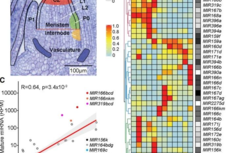
玉米干细胞(SAM)miRNA动态调控
【学术前沿】陈策实团队发现营养制剂中胱/半氨酸通过激活mTORC1和清除ROS促进结肠癌生长和耐药
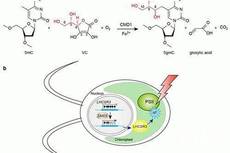
细胞命运决定与分子调控
环境友好的农林害虫生态调控与生物防治技术——2017高级研修班总结

阴阳相济的中庸之道——AMPK和mTORC1营养感知与细胞生长调节
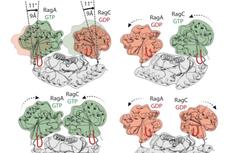
两篇Science一篇Cell :通向mTORC1活化过程的结构基础
Nat Rev MCB | 代谢调控与细胞增殖
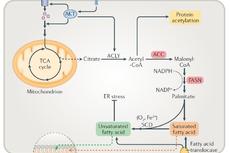
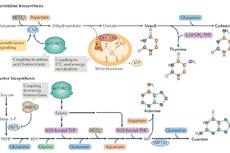
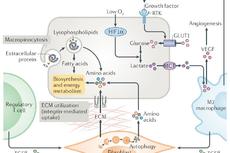

新进展 | 管坤良团队揭示负调控mTORC1机制
Molecular Plant 出版“植物激素”专辑