科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-08-09
来源:中科院之声
蛋白质半胱氨酸Cys上的谷胱甘肽化修饰作为一种可逆的氧化还原修饰,一方面可以保护蛋白免于发生磺酸化(-SO3H)等不可逆的氧化损伤,另一方面和磷酸化修饰一样发挥信号转导功能,传递氧化还原信号。Hsp70是蛋白质质量控制体系中的核心分子伴侣,对于生命体稳态平衡有极为重要的意义。除极少数 Hsp70之外,大部分 Hsp70都有至少1个Cys。深入挖掘 Hsp70的氧化还原修饰机制,对帮助揭示蛋白质稳态的氧化还原调控机制及拓展对 Hsp70功能的认识具有意义。
近日,中国科学院生物物理研究所柯莎研究组、陈畅研究组合作,发现人源应激型 Hsp70的C末端底物结合域的α螺旋盖子上的两个半胱氨酸发生谷胱甘肽化修饰后,导致其C末端α螺旋盖子发生去折叠,从而暴露 Leu542,该残基与底物结合域的相互作用导致了 Hsp70底物结合部位的封闭,而不能结合其底物,这一过程随去谷胱甘肽化的发生而完全可逆。研究结果揭示了 Hsp70的谷胱甘肽化修饰对其结构和功能的调控机制,阐明了人源应激型 Hsp70的C端结构域上的谷胱甘肽化修饰,是一种调节 Hsp70底物结合能力的新机制,可能在氧化应激时调节其底物的活性,从而传递氧化还原信号。
相关成果发表在《生物化学杂志》上。研究得到国家重点研发计划、国家自然科学基金委资助。
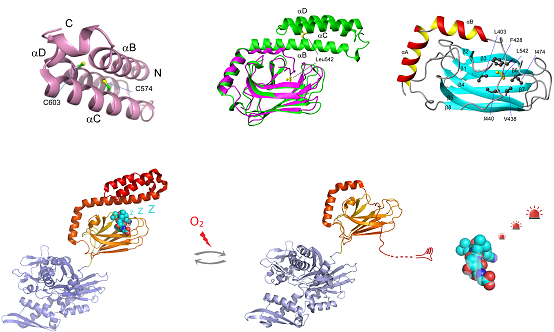
人源应激型Hsp70的C末端α螺旋盖子上的半胱氨酸(上图左)在氧化应激时发生谷胱甘肽化修饰,将导致α螺旋盖子的去折叠(上图中:绿色,谷胱甘肽化修饰前;紫红色,修饰后),其Leu542占据其自身的底物结合位点(上图右)。该过程完全可逆。底物结合位点被Leu542封闭后,Hsp70释放出底物,其中包括作为氧化应激相关的信号分子,如Heat Shock Transcription Factor、HSF1。信号分子释放后,将启动下一步的应激过程(下图)。
来源:zkyzswx 中科院之声
原文链接:https://mp.weixin.qq.com/s?__biz=MjM5NzIyNDI1Mw==&mid=2651777774&idx=4&sn=86a44bf82ce6a851ec3d3b73b0613bb7&chksm=bd2700bc8a5089aa11a2cc1ea2cf7db36baa483f9c8411e800736fa40a4499a3f3cd3a4d57eb#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
褪黑素新用法:降低农药残留

兼具NIR-I/-II成像和谷胱甘肽清除功能的金纳米团簇最大化治疗效果
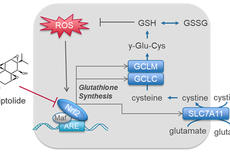
大连化物所等提出干预谷胱甘肽代谢治疗胶质瘤的新策略
红细胞谷胱甘肽合成酶
L-谷胱甘肽二硫醚
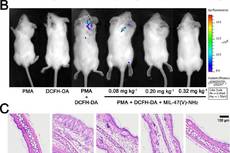
MIL-47(V)的类谷胱甘肽过氧化物酶活性的调控研究及抗炎应用
科学家提出干预谷胱甘肽代谢治疗胶质瘤新策略
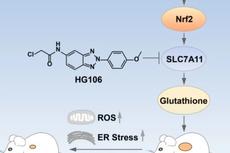
【学术前沿】刘明耀团队揭示KRAS突变肺腺癌的生长依赖SLC7A11/谷胱甘肽代谢轴
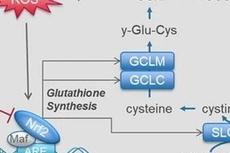
大连化物所提出干预谷胱甘肽代谢治疗胶质瘤的新策略

不止“30条”,我省科技新政打出“组合拳”