科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-09
来源 :科研圈
撰文: Sarah Zhang
翻译: 宋坤
大脑中有一类不起眼的细胞——小胶质细胞,它们不是神经元,直到最近才开始引起科学家的关注。一个极为罕见的病例表明,这些细胞其实是大脑中非常重要的“导航系统”,指引着神经元各就各位、各司其职。
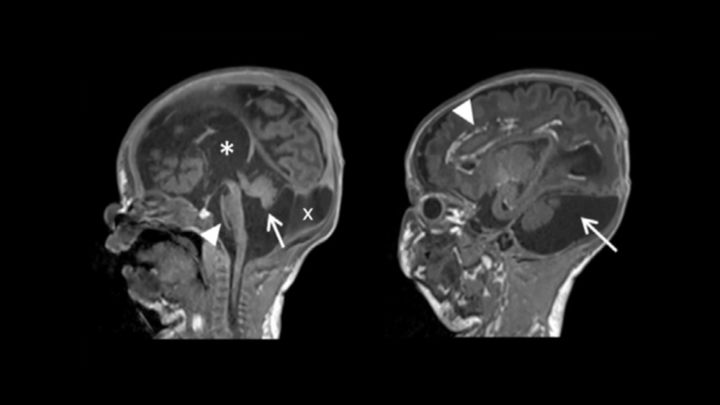
该男孩大脑的核磁共振成像(Magnetic Resonance Imaging, MRIs)表明其结构异常。图片来源:Ossterhof et al.,《美国人类遗传学杂志》(American Journal of Human Genetics )
在这个男孩出生之前,他的父母就已经知道他的大脑很不同寻常——为此,他们从阿拉斯加的农村飞到西雅图,好让孩子一生下来就能得到专家的照顾。詹姆斯·班尼特(James Bennett)就是这样遇到他的。那时他还只是几天大的婴儿,连呼吸都很困难。这个婴儿的头特别大,大脑结构看起来也有问题。班尼特,西雅图儿童医院(Seattle Children’s Hospital)的一位儿科遗传学家,负责寻找病因。
最终答案比医生们想象的更加奇怪:该男孩的大脑完全缺失一类细胞——小胶质细胞(microglia)。这是一个叫 CSF1R 的基因发生突变的结果。医生们此前从来没有见过类似情况。
小胶质细胞占大脑所有细胞的 10%,但是由于它们不是神经细胞,所以长期以来被忽视了。这个男孩的例子使该类细胞的重要性确定无疑。在没有小胶质细胞的情况下,他的神经细胞仍然增长,并填满了头骨,但是它们最终长错了位置,建立了错误的连接。科学家们开始意识到,小胶质细胞指导着大脑发育。
“这个孩子的大脑中没有一处不受到影响,”班尼特说道。这个婴儿的一部分小脑以一个奇怪的角度凸起。他的脑室太大,而正常情况下脑室只是装满了液体的小腔。被认为连接大脑左右半球的一束密集的神经——胼胝体,在该男孩的大脑中完全没有发育。
科学家之前已经在培养皿和动物中观察到,小胶质细胞将发育中的神经细胞引导到正确的位置,形成高度组织化的大脑皮层,最终构成了大脑。它们也修剪了神经元之间的连接。“当你开始操纵小胶质细胞的功能时,情况很快就会失控,”斯蒂芬·诺克托(Stephen Noctor)说道,他是加州大学戴维斯分校(University of California at Davis) 的一个发育神经生物学家,没有参与该男孩的诊查。为了进一步了解 CSF1R 基因,班尼特与研究斑马鱼的生物学家合作。在斑马鱼身上,关闭这个基因会扰乱一些细胞通路,而这些通路在人类的胼胝体发育中是至关重要的。
来自加州大学欧文分校(University of California at Irvine)的神经生物学家金·格林(Kim Green)指出,缺少小胶质细胞的变异小鼠的大脑内部具有大致相似的混乱结构。这些小鼠模型基本上预测了在人类中可能发生的情况,只是格林完全没有想过会碰到一个没有小胶质细胞的人。“这种情况绝非寻常,”他说道。
这个男孩的大脑帮助解开了这些科学奥秘。但是他终归还只是一个身患重疾的小男孩,有着一对忧虑的年轻父母。事实上,他们儿子的情况如此严重,是因为他继承了两个错误的 CSF1R 基因拷贝——双亲中每人一个。因为他的父母是表亲,他们碰巧携带了同一个罕见变异。
在成年人中,仅仅一个拷贝的 CSF1R 基因突变就能导致大脑结构混乱,这被称为成人白质脑病合并轴突球样变和色素性胶质细胞(adult-onset leukoencephalopathy with axonal spheroids and pigmented glia),它会引发记忆丧失,患者最终在 40 多岁出现痴呆。当拿到这个男孩的 DNA 测序结果时,班尼特意识到,他必须向孩子的父母解释他们自己的 CSF1R 基因突变以及患病的风险。他说,听完他的讲述,这对父母松了一口气,理解了孩子哪里出现了问题,但好像又过于震惊,无法完全理解这对于他们自己的生活的意味着什么。这对夫妻在给儿子进行 DNA 测序之前和一位遗传咨询师聊过,班尼特说他安排他们和另外一个遗传咨询师见面,在他们回到阿拉斯加州的家以后。
这个故事没有奇迹治愈或者美好结局。在 10 个月大的时候,这个男孩在阿拉斯加去世了,很可能是因为相关的原因。班尼特说这家人同意了尸检。从那以后他们就失去了联系。他们留给班尼特的手机号码无效了。他告诉我,他最近联系上了这位妈妈的姐妹,试图告诉小男孩的家人一些研究的情况,这项研究由于他们的孩子才得以进行。这是一个微妙的平衡:他感觉有告知的义务,但是他理解这对父母可能不想再提起夭折的儿子。
班尼特说,一个儿科遗传学家的工作经常是诊断那些突破人体极限的极罕见疾病。“在任何一天,你都能找到一个足以用余下的全部职业生涯去研究的病人,” 他说道。这个男孩就是其中之一。
论文信息
【标题】Homozygous Mutations in CSF1R Cause a Pediatric-Onset Leukoencephalopathy and Can Result in Congenital Absence of Microglia
【作者】Nynke Oosterhof et al.
【期刊】American Journal of Human Genetics
【时间】April 11, 2019
【DOI】https://doi.org/10.1016/j.ajhg.2019.03.010
【摘要】Microglia are CNS-resident macrophages that scavenge debris and regulate immune responses. Proliferation and development of macrophages, including microglia, requires Colony Stimulating Factor 1 Receptor ( CSF1R ), a gene previously associated with a dominant adult-onset neurological condition (adult-onset leukoencephalopathy with axonal spheroids and pigmented glia). Here, we report two unrelated individuals with homozygous CSF1R mutations whose presentation was distinct from ALSP. Post-mortem examination of an individual with a homozygous splice mutation (c.1754−1G>C) demonstrated several structural brain anomalies, including agenesis of corpus callosum. Immunostaining demonstrated almost complete absence of microglia within this brain, suggesting that it developed in the absence of microglia. The second individual had a homozygous missense mutation (c.1929C>A [p.His643Gln]) and presented with developmental delay and epilepsy in childhood. We analyzed a zebrafish model ( csf1rDM) lacking Csf1r function and found that their brains also lacked microglia and had reduced levels of CUX1, a neuronal transcription factor. CUX1 + neurons were also reduced in sections of homozygous CSF1R mutant human brain, identifying an evolutionarily conserved role for CSF1R signaling in production or maintenance of CUX1 + neurons. Since a large fraction of CUX1 + neurons project callosal axons, we speculate that microglia deficiency may contribute to agenesis of the corpus callosum via reduction in CUX1 + neurons. Our results suggest that CSF1R is required for human brain development and establish the csf1r DM fish as a model for microgliopathies. In addition, our results exemplify an under-recognized form of phenotypic expansion, in which genes associated with well-recognized, dominant conditions produce different phenotypes when biallelically mutated.
【链接】https://www.cell.com/ajhg/fulltext/S0002-9297(19)30106-5#%20
来源:keyanquan 科研圈
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5NDkzNjIwMg==&mid=2651680381&idx=3&sn=bf24e0d8e569e0445310fed12fe7a00e&chksm=8bbec398bcc94a8e8095ddcbeef30d8d292c32a3fcd1c350a977cb703b796bc1554bb7e7d134&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn