科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-21
来源:药学进展
快速导览
肿瘤
2019年4月25日,中国科学家发表BTK抑制剂专利
2019年4月17日,2019年4月17日,BP-1003在胰腺导管腺癌的异种移植模型中显示有效
2019年4月12日,武田发现新的低氧诱导因子脯氨酸羟化酶抑制剂
肿瘤免疫疗法
2019年4月23日,PD-1与CTLA-4的不同之处
2019年4月4日,分泌双特异性T细胞衔接器的CAR-T疗法能够克服胶质母细胞瘤的异质性
胃肠道疾病
2019年4月24日,武田公司发表ART-648用于治疗NASH的临床前研究数据
免疫调节剂
2019年4月10日,一款基于RNA的佐剂CV-8102与已上市狂犬疫苗联用的I期临床结果发布
感染
2019年4月24日,RO-7049389用于治疗慢性HBV感染的I期临床数据发布
代谢类疾病
2019年4月24日,帕金森药物能够抑制肥胖基因
神经系统疾病
2019年4月5日,二甲双胍在阿尔茨海默症模型中有积极作用
肿瘤
2019年4月25日,中国科学家发表BTK抑制剂专利
扬子江药业和上海海雁医药科技有限公司发表了一类1,2-二氢吡咯[3,4-c]并吡啶/嘧啶-3-酮类化合物,作为酪氨酸蛋白激酶BTK抑制剂,有望用于治疗癌症、自身免疫性疾病、过敏和炎症性疾病。
代表化合物I在LanthaScreenTR-FRET实验中能够抑制野生型BTK的活性(IC50 =48 nM),并对野生型表皮生长因子受体(EGFR)具有选择性(IC50> 10000 nM)。在HTRF实验中,化合物I能够抑制人B淋巴细胞癌Ramos细胞中的BTK在Tyr223位点上的磷酸化(IC50 = 4nm)。(详见专利WO 2019062328)。
代表化合物II在TR-FRET实验中显示能够抑制野生型BTK的活性(IC50 = 69 nM),且对野生型EGFR具有选择性(IC50 >10000 nM)。在口服30 mg/kg剂量下,化合物在ICR小鼠体内的生物利用度为79.72%,半衰期为5.93 h。(详见专利WO 2019062329)。
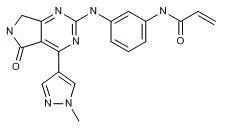
化合物I的结构,来自专利WO2019062328
2019年4月17日,BP-1003在胰腺导管腺癌的异种移植模型中显示有效
来自Bio-PathHoldings的研究人员发现了一种新的信号传导及转录激活因子-3(STAT3)抑制剂,一个脂质体结合的反义寡核苷酸BP-1003,并研究了该化合物对非小细胞肺癌和白血病细胞的抑制作用。作为候选化合物的BP-1003能够降低NSCLC细胞的生存能力,同时能降低白血病和淋巴瘤细胞的存活率,但不影响外周血单核细胞(PBMCs)的生存。体外活组织敏感性试验表明,18例胰腺导管腺癌(PDAC)患者来源的异种移植(PDXs)模型中,有9例的组织切片存活率显著降低了30%以上。在BP-1003单独治疗或联合吉西他滨用于PDAC PDX小鼠模型治疗的体内研究中,数据显示BP-1003在体内降低了STAT3的表达,它与吉西他滨的联合应用能使肿瘤缩小。这些临床前结果提示,BP-1003作为单药和联合用药都具有良好的体内活性,有望成为一种晚期和/或转移肿瘤的治疗新策略。目前已计划对BP-1003进行申报IND的研究。(Dai, B. et al. 110th AnnuMeet Am Assoc Cancer Res (AACR) (March 29-April 3, Atlanta) 2019, Abst 4786)。
2019年4月12日,武田发现新的低氧诱导因子脯氨酸羟化酶抑制剂
武田制药公司报道了一类N-(氰基取代苄基或吡啶甲基)-3-羟基吡啶酰胺类衍生物,作为缺氧诱导因子(HIF)脯氨酸羟化酶抑制剂,尤其是Egl9同源物1(EGLN1;PHD2)的抑制剂,有望用于治疗癌症,心血管、肾脏、肺部疾病,和代谢、血液学、肝脏疾病以及皮肤病变等。代表化合物在细胞HIF-alpha稳定试验中对PHD2酶的抑制活性为pIC50 = 8,对大鼠H9c2心肌细胞中PHD的抑制活性为pEC50= 5.8。(详见专利WO 2019060850)。
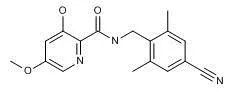
图为专利WO 2019060850中代表化合物的结构
肿瘤免疫疗法
2019年4月23日,PD-1与CTLA-4的不同之处
检查点分子程序性细胞死亡蛋白1(PD-1)在T细胞的整个生命周期中都有表达,但靶向PD-1和PD-L1并不能影响T细胞的活化,这与细胞毒性T淋巴细胞蛋白4(CTLA-4)检查点阻断剂有所不同。日本德岛大学的研究人员证实,在T细胞活化阶段,抗原呈递细胞(APCs)上表达的PD-L1能够与另一种APCs表达的表面分子CD80发生顺式作用。这种顺式作用在T细胞活化的早期破坏了PD-L1与PD-1的结合,从而抑制了T细胞的活性。作者写道:“在没有PD-L1与CD80顺式作用的敲入小鼠中,PD-1能够大大削弱肿瘤免疫和自身免疫反应。因此,靶向PD-L1/CD80顺式作用的治疗策略,可能为癌症、自身免疫性疾病和慢性炎症的治疗提供新的思路。”(Sugiura, D. et al.Science 2019, Advanced publication) 。
2019年4月4日,分泌双特异性T细胞衔接器的CAR-T疗法能够克服胶质母细胞瘤的异质性
在2019年美国癌症研究协会年会(AACR)上,麻省总医院的研究人员提出了一种新的嵌合抗原受体T细胞(CAR-T)疗法,用于治疗表达野生型表皮生长因子受体(EGFR)的胶质母细胞瘤。在此之前,研究人员制备了一个定向于EGFRvIII的CAR-T细胞,这是在30%的多发性胶质母细胞瘤患者中发现的最常见变异。虽然该治疗的安全性和耐受性良好,但残余的肿瘤细胞仍然表达高水平的野生型EGFR。在进一步的研究中,科学家修饰了上述CAR-T细胞,使其分泌一种针对野生型EGFR的双特异性T细胞衔接器(BiTE)。研究表明,由CAR-T细胞分泌的BiTEs可以与适当的抗原结合,在体外对EGFRvIII阴性肿瘤细胞和PDX神经球模型均具有抑制作用。此外,分泌的BiTEs会重新使旁观者T细胞和CAR-BiTE细胞对EGFRvIII阴性肿瘤细胞进行攻击。该疗法对EGFRvIII阴性肿瘤的小鼠模型也是安全和有效的。上述结果证实,对EGFRvIIICAR-T细胞的修饰可能有助于克服多形性胶质母细胞瘤的异质性,值得在患者中进行进一步研究。(Choi,B.D. et al. 110th Annu Meet Am Assoc Cancer Res (AACR) (March 29-April 3,Atlanta) 2019, Abst LB-066)。
胃肠道疾病
2019年4月24日,武田公司发表ART-648用于治疗NASH的临床前研究数据
磷酸二酯酶4(PDE4)通过调控细胞内的cAMP发挥着多种角色,在影响生理功能的同时也可能导致疾病。靶向PDE4的策略在治疗炎症性疾病中是有效的。遵循治疗代谢和纤维化疾病的策略,武田公司开发了ART-648(TAK-648),一种新的选择性PDE4抑制剂,用于非酒精性脂肪性肝炎(NASH)的潜在治疗。在体内试验中,ART-648被用于治疗LDL受体缺失的(LDLr-/-)改良胆碱缺乏饮食的小鼠,分别给药1、3和10mg/kg持续7周(预防模式),或4和8 mg/kg给药持续 10周(治疗模式)。ART-648也被用于治疗饮食诱导肥胖(DIO)的小鼠(3 mg/kg)。结果显示,ART-648能够剂量依赖的降低肝纤维化面积、甘油三酯含量、肝内胶原蛋白-I的基因表达(P值均< 0.05),同时降低了肿瘤坏死因子(TNF)和金属蛋白酶抑制因子1的表达(P值均<0.05)。治疗对小鼠体重和DIO小鼠的食物摄取量和脂肪量均有显著影响(P值均< 0.05),单剂量给药后能够增加氧和能量的消耗。在人全血中,ART-648以剂量依赖的方式抑制LPS诱导的TNF释放。上述数据表明ART-648具有抗纤维化、抗炎和抗代谢作用,揭示它有望应用于NASH的治疗。(Amano,Y. et al. 54th Annu Meet Eur Assoc Study Liver (EASL) (April 10-14, Vienna)2019, Abst SAT-356)。
免疫调节剂
2019年4月10日,一款基于RNA的佐剂CV-8102与已上市狂犬疫苗联用的I期临床结果发布
CureVac公司最近发表了一项I期研究的结果,评估了单独使用佐剂CV-8102或与上市狂犬病疫苗(Rabipur,GSK)联用在健康的志愿者中的安全性、耐受性和免疫原性。CV-8102是一种Toll样受体7/8(TLR7/8)和维甲酸诱导基因I(RIG-I)激动剂的基于RNA的佐剂,旨在增强免疫原性较差抗原的免疫原性。在动物模型中,CV-8102已被证明能够提高流感和狂犬疫苗的效力。此外,当与重组蛋白和抗原衍生肽结合时,它能引起强烈的体液和细胞免疫反应。在首次人体试验中,56名健康男性志愿者分别接受了50-100 mcg的CV-8102单药(n = 11)、CV-8102和Rabipur联用(n = 20)或Rabipur单药(n= 25,对照组)的研究。CV-8102的单独使用或联用主要引起1级或2级局部或全身反应,无相关的严重不良事件。100 mcg剂量的CV-8102可导致C反应蛋白的显著升高,从而停止了进一步提高剂量。诱导狂犬病毒中和效价(VNTs)是一种测量免疫增强潜力的方法,CV-8102(25-50 mcg)联合小剂量的Rabipur可显著改善VNT的反应动力学。此外,50 mcg CV-8102还能增强1/10剂量的Rabipur的VNT反应程度,但在14名受试者中有2人出现了严重但自限的流感样症状。该研究的结论是,CV-8102在25-50 mcg剂量下是安全的,并显示了可接受的反应原性,同时能够显著提高狂犬病疫苗的免疫原性(Doener,F. et al. Vaccine 2019, 37(13): 1819)。
感染
2019年4月24日,RO-7049389用于治疗慢性HBV感染的I期临床数据发布
罗氏公司的研究人员报告了RO-7049389正在进行的一期研究结果,评估了该药对慢性HBV感染且未经治疗患者的安全性、耐受性、药代动力学和抗乙型肝炎病毒(HBV)的疗效。从三组慢性HBV感染患者的机制验证(POM)研究中,分别评估了PK、安全性和药效学数据,包括200mg每日两次(n = 7,标准膳食)、400mg每日两次(n = 7,标准膳食)队列,以及600mg每日一次(n = 7,禁食),所有受试者均治疗28天。结果显示,患者的PK性质与之前研究中健康志愿者相似,RO-7049389没有出现Cmax和AUCtau的积累。所有POM队列的HBVDNA和RNA均明显下降。HBV DNA较基线下降的中位数分别为2.7、3.2和2.9log10 IU/mL(200 mg组、400 mg组和600 mg组)。HBV RNA下降的中位值为1.6和2.3 log10拷贝/mL(200mg组和400 mg组),600mg组的结果仍有待确定。给药期间未见病毒学突破,给药28天内HBsAg或HBeAg抗原水平未见明显变化。数据显示健康志愿者和HBV感染患者的安全性相似,22例HBV患者中有14例报告了总计39例不良事件(AEs)。其中3例患者治疗后出现3级ALT/AST升高,停药后随访恢复。此外有一例给药前的严重AE,导致病人被替换。无不良反应导致停药,未观察到任何安全参数的显著变化。综上所述,本研究的初步数据表明,在慢性HBV感染患者中,RO-7049389的耐受性良好,在28天的给药期间具有较强的抗HBV活性。RO-7049389将与其他药物进行进一步的联合用药评估。(Gane, E. et al. 54th Annu Meet Eur AssocStudy Liver (EASL) (April 10-14, Vienna) 2019, Abst FRI-219)。
代谢类疾病
2019年4月24日,帕金森药物能够抑制肥胖基因
来自北京生命科学研究所和中科院北京基因组研究所的研究人员近日发现,FDA批准的治疗帕金森的药物恩他卡朋(entacapone)是一个FTO蛋白抑制剂。全基因组关联分析表明,FTO编码的脂肪和肥胖基因与体重相关,FTO蛋白还影响着大脑、肝脏和脂肪组织等多个器官的代谢。研究人员使用基于结构的虚拟筛选,发现FDA已批准的药物恩他卡朋是一种潜在的FTO抑制剂。通过结构和生化研究,发现恩他卡朋在体外能够直接与FTO结合并抑制其活性。此外,恩他卡朋还能够与叉头盒转录因子O1(FOXO1)发生相互作用,降低饮食诱导肥胖小鼠的体重和空腹血糖浓度(Peng, S. et al. Sci Transl Med2019, 11(488): pii: eaau7116)。
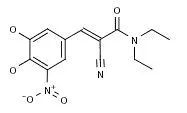
图为恩他卡朋Entacapone的结构
神经系统疾病
2019年4月5日,二甲双胍在阿尔茨海默症模型中有积极作用
有证据表明糖代谢受损与阿尔茨海默症相关,拉脱维亚大学的科学家们对糖尿病药物二甲双胍在阿尔茨海默症大鼠模型中的作用进行了评估。利用链脲霉素诱导大鼠认知功能损害后,使用口服二甲双胍75 mg/kg、100mg/kg或生理盐水21天进行治疗。结果显示,两种剂量的二甲双胍都能够改善水迷宫测试评估的空间学习和记忆能力,以及三箱社交实验中的表现,剂量越大效果越好。链脲霉素可以降低葡萄糖转运体GLUT1在皮质和海马的表达,而二甲双胍则显著增加了这些区域的GLUT1表达。上述发现给出了干预早期阿尔茨海默症发展的一种可能手段。(Pilipenko,V. et al. 14th Int Conf Alzheimer Parkinson Dis (AD/PD) (March 26-31, Lisbon)2019, Abst 338)。
目前正在进行的一项脑成像研究,将对纳入糖尿病预防成果研究(DPPOS)的患者随机使用二甲双胍或安慰剂进行治疗,以评估阿尔茨海默症大脑成像的生物标志物。(ClinicalTrials.govIdentifier NCT03757910)。
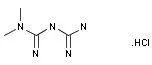
图为盐酸二甲双胍的结构
本文内容摘自科睿唯安药物新闻Bioworld Science,科睿唯安对本文的全部内容以及可能附带的全部资料拥有全部知识产权,并受法律保护。网络转载、编译及其他商业使用请联系市场部:yili1@Clarivate.com
关于药学进展
《药学进展》杂志是由中国药科大学和中国药学会共同主办、国家教育部主管,月刊,80页,全彩印刷。刊物以反映药学科研领域的新方法、新成果、新进展、新趋势为宗旨,以综述、评述、行业发展报告为特色,以药学学科进展、技术进展、新药研发各环节技术信息为重点,是一本专注于医药科技前沿与产业动态的专业媒体。
《药学进展》注重内容策划、加强组稿约稿、深度挖掘、分析药学信息资源、在药学学科进展、科研思路方法、靶点机制探讨、新药研发报告、临床用药分析、国际医药前沿等方面初具特色;特别是医药信息内容以科学前沿与国家战略需求相合,更加突出前瞻性、权威性、时效性、新颖性、系统性、实战性。根据最新统计数据,刊物篇均下载率连续三年蝉联我国医药期刊榜首,复合影响因子0.760,具有较高的影响力
《药学进展》编委会由国家重大专项化学药总师陈凯先院士担任主编,编委新药研发技术链政府监管部门、高校科研院所、制药企业、临床医院、CRO、由金融资本及知识产权相关机构百余位极具影响力的专家组成。
来源:ppsyxjz 药学进展
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5MDY3ODExNQ==&mid=2651305765&idx=2&sn=b13d591d1702f30fad0cf76be8a347af&chksm=8bf4e129bc83683f46eeec37f28df66ac7a6c8a8c65ba0ba50bb914d1bc9fbb08d576c8cebc2&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
国产新冠肺炎药物研发有突破!

人工智能助力药物研发
2016药物/化学品致癌性试验研究高级培训班在青岛举行

中国药学会药品系统评价培训班在京开班
第六届全国药物毒理学年会在重庆成功举办




国产新冠肺炎药物研发有突破!

慎重!相分离进军药物动力学与药物研发

国产新冠肺炎药物研发有突破!

人工智助力药物研发:深度学习预测药物调控激酶谱

中国药学会医院药学专业委员会持续推进高警示药品管理与风险防范