科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-07
来源:X一MOL资讯
原标题:【纳米】“火车跑得快,全凭车头带”:线粒体靶向可视化输送大量抗癌药物的DNA“纳米火车”
DNA纳米技术是一种多学科交叉的研究领域,主要利用DNA(脱氧核糖核酸)尺寸为纳米级别、刚性结构、编码性强的特点来构造各种纳米结构,应用于生物医学、化学、材料等领域。DNA纳米技术的发展刷新了人们对DNA这一生物大分子的认识,它不仅仅能作为生命遗传信息的载体,还能够作为纳米结构的构建工具。谭蔚泓院士课题组开创性的利用DNA碱基互补配对原则,构建了以核酸适配体(aptamer)为“火车头”的DNA“纳米火车”递送系统。由于整列“火车”由生物分子组成,毒副作用也非常小,可大大减轻化疗给癌症患者带来的身心痛苦。同时,核酸适配体构成的“火车头”可与癌细胞表面特异的膜蛋白结合,为给药系统提供“方向”和“动力”(PNAS, 2013, 110, 7998, DOI: 10.1073/pnas.1220817110)。然而,如何实现亚细胞水平的细胞器靶向递送,仍然是目前有待解决的重大问题和研究热点。
线粒体是一种存在于大多数细胞中的由两层膜包被的细胞器,是细胞中产生能量的结构,也是细胞进行有氧呼吸的主要场所,被称为"power house"。除了为细胞供能外,线粒体还参与诸如细胞分化、细胞信息传递和细胞凋亡等过程,并拥有调控细胞生长和细胞周期的能力。最新研究表明,线粒体对肿瘤进展为恶性起着重要的调控作用。癌细胞在一些与癌症相关的基因突变和蛋白表达推动了代谢上的变化。癌细胞通过有氧糖酵解可以获得更多的生物大分子合成原料。这些生物分子为癌细胞快速分裂增殖提供物质基础(蛋白质、脂质、核酸和碳水化合物)。这些与癌症相关的基因突变表达的蛋白还调控着线粒体的功能,控制了细胞的能量产生、氧化还原平衡,进而影响机体的先天免疫系统以及细胞凋亡等。在癌症细胞中,线粒体的生物合成和质量控制都普遍上调了。一些癌细胞中存在线粒体中三羧酸循环中相关酶的基因突变,从而促进了与癌症相关的代谢改变。通过靶向线粒体可以达到控制癌症的潜在可能性。
利用化学抗癌药物杀死癌细胞是现代医学治疗癌症的一项重要手段。但传统的化疗药物无法将癌细胞和正常细胞区分开,在杀死癌细胞的同时也会将正常细胞杀死,毒副作用大。为了可视化的研究化疗药物递送过程,解决化疗药物靶向运输和提高化疗药物的治疗效果。中国科学院深圳先进技术研究院张鹏飞副研究员、龚萍研究员以及蔡林涛研究员通过与佛罗里达大学/湖南大学谭蔚泓院士、澳大利亚新南威尔士大学刘国珍教授以及南方医科大学陈建海教授通力合作,在前期工作基础上,以DNA为基本单元,利用近红外花菁类染料自身具有的线粒体靶向功能,开发了一种线粒体靶向的DNA“纳米火车”载药系统(图1)。该载药系统具有以下特点:(1)以近红外花菁类染料Cy5.5为“火车头”,不仅可以实现对线粒体的靶向,而且由于肿瘤细胞与正常细胞线粒体活性和数量以及表面受体的差异,可以极大提高肿瘤细胞的富集能力。而且其本身具有近红外荧光信号,可以实时对整个DNA“纳米火车”进行细胞/亚细胞层次的GPS定位;(2)以DNA为“火车车身”,可以充分利用DNA碱基互补配对,并结合DNA纳米自组装特性构建多种不同结构的纳米载体系统,同时,DNA为生命体自身存在的生物大分子,不同于传统聚合物载体系统,其自身具有良好的生物相容性和安全性,具有良好的临床转化前景;(3)近红外花菁类染料不仅可以实现纳米火车实在与靶向功能,同时,可以在近红外光照射条件下产生及其微弱的活性氧成分(ROS),不同于能产生大量的活性氧的传统光敏剂(如:Ce6、孟加拉玫瑰红等),其产生的活性氧对机体没有明显伤害,因此极大降低了光毒性的担忧。而由于这些微弱的活性氧由于是产生在线粒体附近,虽然不能起到杀死肿瘤细胞的效果,但是足以调控线粒体的功能,从而增强肿瘤细胞对传统化疗药物的敏感性,从一定程度上辅助增强了化疗药物的作用效果。

图1. 线粒体靶向DNA“纳米火车”用于可视化药物输送与协同化疗示意图
首先,研究者在细胞水平验证了Cy5.5的肿瘤特异性靶向能力,并通过激光共聚焦显微共定位实验证实其在亚细胞层次主要富集在线粒体上。同时,Cy5.5进入肿瘤细胞主要通过有机阴离子转运多肽(OATPs)是一类跨膜转运蛋白,介导着众多钠离子非依赖的物质跨膜转运(图2)。
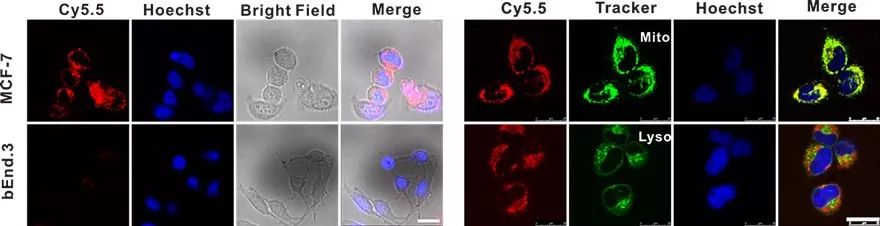
图2. Cy5.5的肿瘤细胞靶向及线粒体定位成像
Cy5.5做为一个化学小分子,能否承担牵引巨大的DNA“火车”进入目标细胞的功能呢?研究者设计了一段随机序列的DNA,然后将Cy5.5标记在DNA的5’末端。通过实验可以发现,Cy5.5的确将DNA带入细胞同时富集在了线粒体上(图3)。
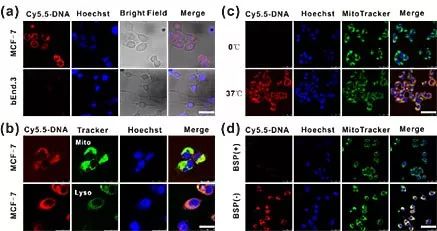
图3. Cy5.5的肿瘤细胞靶向及线粒体定位成像
研究者选择阿霉素作为模式药物,充分利用了其在DNA“火车”上富集后的聚集诱导猝灭(ACQ)效应,和Cy5.5自身的荧光特性,采用成像方法实时的可视化了DNA火车定位线粒体后逐渐释放药物的过程(图4)。
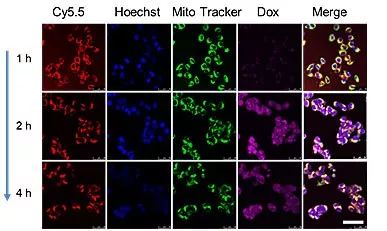
图4. 实时示踪DNA“火车”药物运输及释放过程
另外,结合Cy5.5在近红外光照射下在线粒体附近产生的微弱的单线态氧,安全并有效的增强了肿瘤细胞对化疗药物的治疗敏感性(图5)。并通过研究线粒体凋亡信号通路过程所涉及的蛋白表达,进一步证实通过在线粒体上可控的产生活性氧调控了线粒体相关信号通路,有效实现化疗增敏。
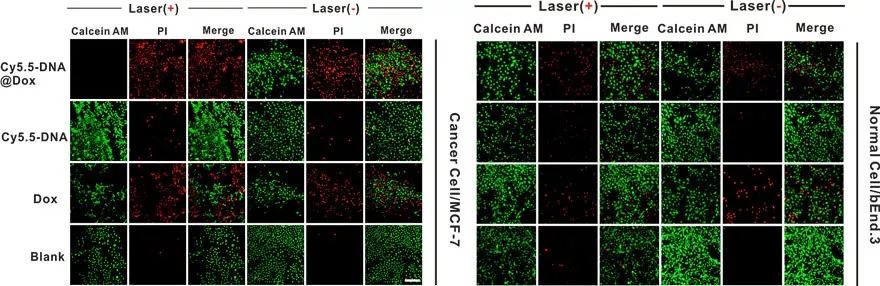
图5. Cy5.5靶向的DNA“火车”协同化疗增敏
“火车跑的快,全凭车头带”。对于如何利用具有亚细胞定位能力的小分子染料作为多功能靶向示踪的药物递送尚处于初步研发阶段。不同于传统生物大分子靶向的是,小分子染料自身具有可示踪特性,同时结合对发光材料发光过程的深入理解,可以借助小分子染料在靶向的同时实现光控协同化疗。为光学诊疗技术发展提供了新的思路。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657613127&idx=4&sn=437d8035f4a4f3c1e81c9cf0777718cb&chksm=80f7dc97b7805581bdca0fe577dd593c671a4136cc97825b276443f0bc833a582547686d29e5&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn