科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-26
来源:生物通
一项对多发性骨髓瘤(multiple myeloma,MM)患者样本的研究已经证明了“重新编程”的脂肪细胞,即使在癌症已经得到缓解后,是如何导致长期的骨损伤的。
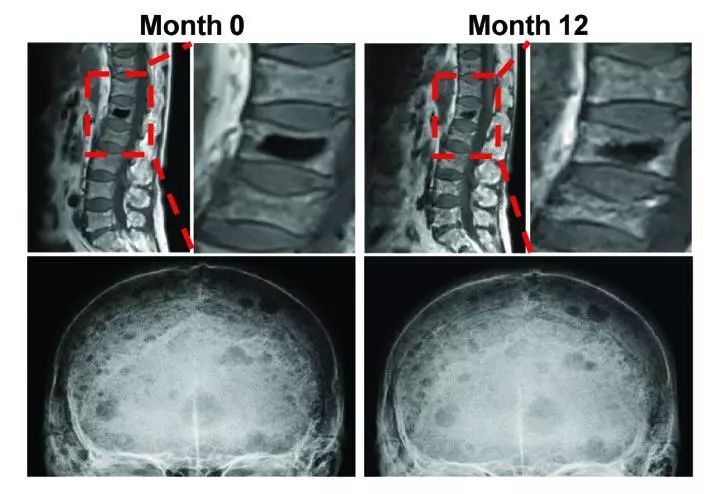
一项对多发性骨髓瘤(multiple myeloma,MM)患者样本的研究已经证明了“重新编程”的脂肪细胞,即使在癌症已经得到缓解后,是如何导致长期的骨损伤的。
以分子复合物作为靶标可减轻小鼠体内骨损害病变的严重程度,提示针对MM这种常见的且使人虚弱的并发症的可能治疗对策。
当癌性浆细胞积聚在骨髓中并对其他血细胞的制造生产产生不利影响时,就会发生这种恶性肿瘤。超过80%的MM患者的骨骼也出现溶骨病变,这可能导致严重疼痛和骨折。即使成功治疗了癌症,这些损伤也无法愈合,从而导致骨愈合的长期缺陷和较低的生活质量。为了理解为什么溶骨病变不能愈合,Huan Liu和他的同事研究了活动期骨髓瘤患者、缓解期患者和健康对照组的骨髓样本。他们观察到,靠近溶骨病变的部位含有大量的骨髓脂肪细胞(脂肪细胞)。与骨髓瘤细胞一起培养的脂肪细胞“逆生长”为重新编程状态,释放抑制骨形成和促进骨分解的酶。
进一步的分析显示,骨髓瘤细胞通过激活一种叫做PRC2的分子复合体来转化脂肪细胞,进而抑制一种叫做PPARγ的受体的活性。脂肪细胞中,PRC2复合体组分EZH2失活可阻止其重新编程,并降低MM缓解期小鼠模型中骨损伤的严重程度,这表明恢复PPARγ活性有助于治疗患者的骨损伤。
参考文献:
Reprogrammed marrow adipocytes contribute to myeloma-induced bone disease
来源:gh_c1fce5726992 生物通
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5NzMwNjYyMg==&mid=2675529798&idx=3&sn=5951bf78a053cbc149183d975a47d50a&chksm=bc51f1d78b2678c19f0391b0cb4e5c3378be43ecd6858dddb127bdf91249205903e8808056a2&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
Science子刊封面“致命脂肪细胞”

脂肪细胞有助伤口愈合

Hepatology:脂肪细胞与肝损伤和炎症

《细胞》:鱼油促进健康的方式,居然是增加脂肪细胞?
石远凯的面对面视频
营养与健康所等发现脂肪前体细胞分化命运的重要调控机制
石远凯:探索抗癌新药
脂肪细胞“变身”各种组织植入物
营养与健康所等发现脂肪前体细胞分化命运的重要调控机制
趣味科学:仰卧起坐会导致瘫痪,这是真的吗?