科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-07-31
来源:生物谷
铁死亡(ferroptosis)是一种由细胞代谢和铁依赖性脂质过氧化作用驱动的细胞死亡过程。它与缺血性器官损伤和癌症等疾病有关。谷胱甘肽过氧化物酶4(GPX4)是铁死亡的一种至关重要的调节剂,通过中和脂质过氧化物来保护细胞,其中脂质过氧化物是细胞代谢的副产物。直接抑制GPX4,或通过剔除它的底物谷胱甘肽或用于产生谷胱甘肽的前体分子(比如半胱氨酸)间接抑制GPX4,都可触发铁死亡。铁死亡有助于增强p53、BAP1和延胡索酸酶等几种肿瘤抑制蛋白的抗肿瘤功能。不过,违反直觉的是,易于发生转移并且经常对各种治疗产生抵抗性的间充质癌细胞(mesenchymal cancer cell)对于铁死亡高度敏感。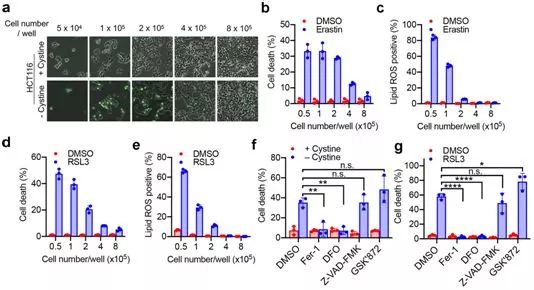 图片来自Nature, 2019, doi:10.1038/s41586-019-1426-6。在一项新的研究中,中国空军军医大学的陈志南(Zhi-Nan Chen)团队和美国纪念斯隆凯特琳癌症中心的Xuejun Jiang团队发现钙粘蛋白介导的细胞间相互作用能够非细胞自主性地调节铁死亡。相关研究结果于2019年7月24日在线发表在Natue期刊上,论文标题为“Intercellular interaction dictates cancer cell ferroptosis via NF2–YAP signalling”。在上皮细胞中,由E-钙粘蛋白介导的这种相互作用通过激活细胞内NF2(也称为merlin)和Hippo信号通路来抑制铁死亡。抑制这种信号轴允许转录共激活因子YAP通过上调包括ACSL4和TFRC在内的几种铁死亡调节物来促进铁死亡。这一发现为具有间充质或转移特性的癌细胞对铁死亡高度敏感的观察结果提供了机制上的新见解。值得注意的是,类似的机制也调节一些非上皮细胞中的铁死亡。最后,鉴于肿瘤抑制基因NF2失活是间皮瘤中的一种常见的致癌事件,这些研究人员在恶性间皮瘤原位小鼠模型中,通过遗传手段让肿瘤抑制基因NF2失活可使得癌细胞对铁死亡更加敏感。这些研究结果展示了细胞间相互作用和细胞内NF2-YAP信号通路在调节细胞铁死亡中的作用,而且还指出NF2-YAP信号通路中的恶性突变可能能够预测癌细胞对潜在的铁死亡诱导性疗法(ferroptosis-inducing therapy)的反应性。
图片来自Nature, 2019, doi:10.1038/s41586-019-1426-6。在一项新的研究中,中国空军军医大学的陈志南(Zhi-Nan Chen)团队和美国纪念斯隆凯特琳癌症中心的Xuejun Jiang团队发现钙粘蛋白介导的细胞间相互作用能够非细胞自主性地调节铁死亡。相关研究结果于2019年7月24日在线发表在Natue期刊上,论文标题为“Intercellular interaction dictates cancer cell ferroptosis via NF2–YAP signalling”。在上皮细胞中,由E-钙粘蛋白介导的这种相互作用通过激活细胞内NF2(也称为merlin)和Hippo信号通路来抑制铁死亡。抑制这种信号轴允许转录共激活因子YAP通过上调包括ACSL4和TFRC在内的几种铁死亡调节物来促进铁死亡。这一发现为具有间充质或转移特性的癌细胞对铁死亡高度敏感的观察结果提供了机制上的新见解。值得注意的是,类似的机制也调节一些非上皮细胞中的铁死亡。最后,鉴于肿瘤抑制基因NF2失活是间皮瘤中的一种常见的致癌事件,这些研究人员在恶性间皮瘤原位小鼠模型中,通过遗传手段让肿瘤抑制基因NF2失活可使得癌细胞对铁死亡更加敏感。这些研究结果展示了细胞间相互作用和细胞内NF2-YAP信号通路在调节细胞铁死亡中的作用,而且还指出NF2-YAP信号通路中的恶性突变可能能够预测癌细胞对潜在的铁死亡诱导性疗法(ferroptosis-inducing therapy)的反应性。来源:BIOONNEWS 生物谷
原文链接:http://mp.weixin.qq.com/s?__biz=MzI2NjY1NjA5Mw==&mid=2247502872&idx=2&sn=11470382749b01cbc3f781621e768eec&chksm=ea884c2addffc53c65f0adbe782f285b1f0548037c40c8f3b60bf219811374dc1637d85c7a6b&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

癌症研究大牛最新Cancer Cell:是什么让癌细胞中的巨噬细胞错乱?
癌症: 正在扩散当中的早期转移癌细胞的捕捉

靠不吃“饿死”癌细胞?癌症患者补品食用指南来了
癌症转移,癌细胞最容易转移至哪些部位?

新型癌症疗法:关闭癌细胞里的发电站!

治疗癌症的最好方法,是不要杀光所有癌细胞?
第22届全国肿瘤防治宣传周启动仪式在北京举行




靠不吃“饿死”癌细胞?癌症患者补品食用指南来了
哈佛大学医学院Kucherlapati教授访问中国抗癌协会


治疗癌症的最好方法,是不要杀光所有癌细胞?


