科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-08-02
来源:ScienceAAAS
评述论文:The pigment-protein network of a diatom photosystem II – light-harvesting antenna supercomplex (Science 2 August 2019: Vol 365, Issue 6452)
光合作用是地球生态系统中物质与能量循环最关键的过程。光合生物大规模地利用太阳能将二氧化碳和水转换为有机物,植物、藻类和蓝细菌等放氧光合生物还能裂解水释放出氧气,因此光合作用为地球上几乎所有生命体提供最基本的物质基础和能量来源,也是提高农作物产量、开发新能源和维护可持续发展生态环境的基础。
光合作用分为光反应和暗反应两个阶段,光反应阶段是由光合膜上一系列膜蛋白超级复合体协同配合来完成的,包括光系统II(photosystem II,PSII),光系统I(photosystem I,PSI),细胞色素b6f,以及ATP合成酶。PSII 利用其外周的捕光天线(Light-harvesting complex,LHC)吸收并传递光能,在反应中心实现水的裂解,释放出氧气、质子和电子。PSII释放的电子,经过细胞色素b6f和 PSI等一系列电子传递过程最终将NADP+还原成NADPH。PSII与PSI 进行电子传递的同时形成跨膜质子梯度驱动ATP合成酶合成ATP。NADPH和ATP则进一步用于CO2的同化过程生成有机物。
在漫长的生物进化过程中,放氧光合生物PSII的反应中心具有高度保守性,然而为了适应复杂多变的光环境,尽可能高效的利用光能,它们进化出多种多样的捕光天线。蓝细菌和红藻主要利用水溶性的藻胆体作为捕光天线,绿藻和高等植物则利用镶嵌于膜内的色素-蛋白复合物体进行捕光。在高等植物PSII反应中心的外周,结合了三聚体的主要捕光复合物LHCII和单体的次要捕光复合物CP29、CP26和CP24,形成PSII-LHCII二聚体超级复合体(1,2)。高等植物PSII的捕光天线结合了大量的叶绿素a/b (Chl a/b)及类胡萝卜素分子,它们不仅能够高效的捕获和传递光能,还参与激发能在PSII和PSI之间的平衡分配(3,4),以及耗散强光照时过剩的光能,保护植物免受强光损伤(5)。
在海洋中,硅藻是主要的浮游生物之一,贡献了海洋中约40%的原初生产力,其吸收二氧化碳的能力占全球生态系统的五分之一左右,比热带雨林的贡献还要高(6,7)。与高等植物显著不同的是,硅藻PSII外周的捕光天线是结合岩藻黄素(Fucoxanthin,Fx)和 Chl a/c的膜蛋白(Fucoxanthin Chl a/c binding proteins: FCPs), 这使得硅藻呈现出棕色外观,并且具有很强的在水中捕获蓝绿光的能力和极强的光保护能力(8)。尽管关于高等植物PSII-LHCII复合物的结构研究已相当广泛(1,2,9),但硅藻PSII-FCPII复合物还没有任何结构报道。研究硅藻PSII-FCPII的精细结构,将从分子水平上揭示海洋光合生物进行光能捕获、传递和耗散的机理。
在本期Science杂志中,中科院植物研究所沈建仁和匡廷云研究组,清华大学隋森芳研究组联合报道了中心纲硅藻 (Chaetoceros gracilis) PSII-FCPII超级复合体3.0 Å分辨率的冷冻电镜结构。这是该团队在前期解析了羽纹纲硅藻FCP二聚体晶体结构基础上的又一重大突破(10)。该结构构建了硅藻PSII-FCPII复杂的蛋白和色素网络,揭示了复合体中各个亚基的相互作用方式及硅藻PSII独特的捕光天线组装排布。依据结构,作者发现了硅藻PSII-FCPII复合体中多条能量传递途径,为揭示硅藻PSII高效吸收、传递和转化光能的机理提供了分子基础。
硅藻PSII-FCPII超级色素-蛋白复合体是由两个PSII-FCPII单体组成的二聚体(图1A),每个单体包含24个核心亚基和11个外围FCP天线亚基(图1B)。PSII-FCPII二聚体总体分子量超过1.4 MDa,结合了288个叶绿素分子、146个类胡萝卜素分子、锰簇、电子传递体及大量的脂分子等。硅藻PSII-FCPII的核心复合物与蓝藻及红藻相似,但是具有额外的两个核心亚基(PsbG和Psb34)位于核心亚基CP47的外侧,以及一个特有的外周放氧亚基Psb31(图1B,C)。Psb31亚基没有与放氧反应中心直接结合,其主要功能可能是保护反应中心锰簇并促进反应中心质子的排出。在硅藻PSII反应中心外周,捕光天线FCP具有独特的组装和排布方式,与高等植物PSII外周天线的排布明显不同。在每个硅藻PSII单体外周的11个FCP亚基中,有八个FCP(作者将其暂定为FCP-A)形成两个四聚体,分别结合在PSII核心两侧,其中一个FCP四聚体通过PsbG与核心亚基CP47结合,被命名为强结合型四聚体(Strongly associated tetramer,ST);在另外一侧,FCP四聚体通过两个单体FCP(FCP-D和FCP-E)连接在核心亚基CP43上,被命名为中等结合型四聚体(moderately associated tetramer,MT)。此外,还有一个FCP单体(FCP-F)结合在MT的外周(图1A,B)。
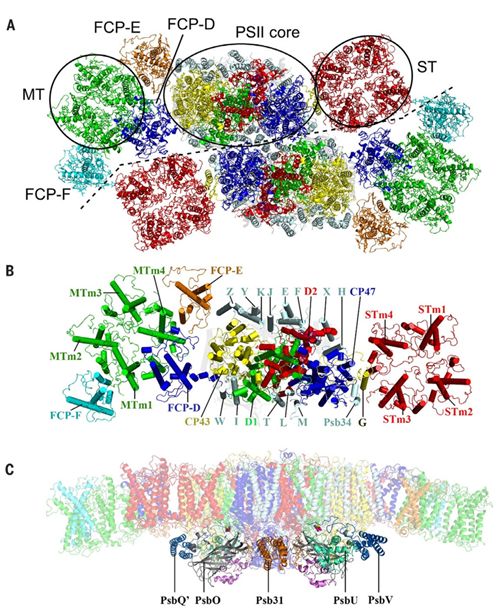 图1. 中心纲硅藻PSII-FCPII超级复合物结构。 (A) PSII-FCPII二聚体基质侧俯视图。(B) PSII-FCPII单体各亚基组成及排布。(C) PSII-FCPII外周放氧蛋白亚基的侧视图。
图1. 中心纲硅藻PSII-FCPII超级复合物结构。 (A) PSII-FCPII二聚体基质侧俯视图。(B) PSII-FCPII单体各亚基组成及排布。(C) PSII-FCPII外周放氧蛋白亚基的侧视图。本文报道的PSII-FCPII复合物结构来源于中心纲硅藻,其外周天线FCP-A,FCP-D和FCP-E都与已解析的羽纹纲硅藻FCP晶体结构具有相似的三维结构和色素结合位点,但在类囊体腔侧,它们都具有一段亲水的Helix D靠近C末端(图2A-E),这也是中心纲硅藻FCP能形成四聚体的重要原因之一。在FCP四聚体中,每个FCP-A单体都结合6个Chl a,3个Chl c和6个Fx分子,ST中的四个FCP-A单体还额外结合了一个Chl a410位于类囊体腔侧的Helix E附近。FCP-E连接了MT和PsbZ亚基,在FCP-E与PsbZ及MT相互作用的界面上分别了结合了的一个额外的Chl分子(Chl a400和a411)(图2B,D)。FCP-D是硅藻PSII的几种捕光天线中最大的亚基,其N-末端、C-末端loop以及Helix C都较长。FCP-D位于反应中心亚基CP43以及两个FCP四聚体形成的三角形区域中(图1A),维持着硅藻PSII-FCPII二聚体的稳定性。FCP-D是一个PSI天线Lhca的类似蛋白,只具有三个类胡萝卜素结合位点,分别结合了两个Fx分子和一个硅甲藻黄素(Diadinoxanthin, Ddx)分子。与Lhca2类似,FCP-D结合了一个额外的Chl601分子(图2C,E)(3,11)。这些硅藻FCP脱辅基蛋白的结构特征及特殊的色素结合位点使它们表现出不同的聚集状态。中心纲硅藻PSII-FCPII复合物中的所有FCP亚基都缺少羽纹纲硅藻FCP二聚体晶体结构中位于二体界面处的两个类胡萝卜素分子Fx304和Ddx308(10);而在中心纲硅藻FCP四聚体中,相邻FCP-A单体位于腔侧的Helix D,BC loop和两个Fx分子(Fx307和Fx302),以及位于基质侧的AC loop及Chl401分子共同参与了四聚体的形成(图2F-H),这些相互作用是在FCP二聚体晶体结构中不存在的。
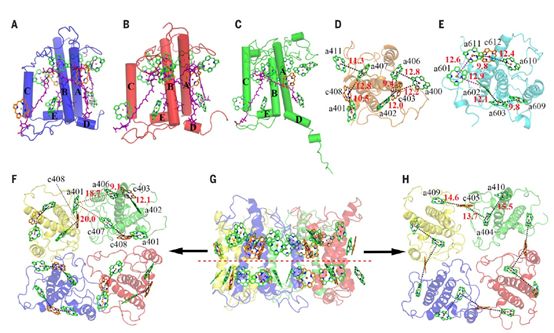 图2. FCP单体及四聚体结构。(A-C)FCP-A,FCP-E,FCP-D单体结构及色素排布。(D)FCP-E基质侧叶绿素排布。(E)FCP-D基质侧叶绿素排布。(F-H)强结合型FCP四聚体结构及叶绿素排布(F,基质侧叶绿素的基质侧俯视图;G,基质侧及腔侧叶绿素侧视图;H,腔侧叶绿素的基质侧俯视图)。绿色,叶绿素a(Chl a);橙色,叶绿素c(Chl c);紫色,岩藻黄素Fx;蓝色,硅甲藻黄素Ddx。
图2. FCP单体及四聚体结构。(A-C)FCP-A,FCP-E,FCP-D单体结构及色素排布。(D)FCP-E基质侧叶绿素排布。(E)FCP-D基质侧叶绿素排布。(F-H)强结合型FCP四聚体结构及叶绿素排布(F,基质侧叶绿素的基质侧俯视图;G,基质侧及腔侧叶绿素侧视图;H,腔侧叶绿素的基质侧俯视图)。绿色,叶绿素a(Chl a);橙色,叶绿素c(Chl c);紫色,岩藻黄素Fx;蓝色,硅甲藻黄素Ddx。与高等植物C2S2M2型PSII-LHCII复合物类似,硅藻PSII-FCPII的叶绿素也可以分成基质侧和腔侧两层(图3)。依据硅藻PSII-FCPII复合体结构所定位的色素网络,作者发现了多条能量传递途径(图3A),其中ST可以将激发能直接传递给反应中心,而MT则需要通过FCP-E和FCP-D的调节。结合在PSII核心复合物外周的PsbG,PsbW和PsbZ亚基位于FCP和PSII核心之间的界面上,调节了FCP向反应中心的能量传递。硅藻外周天线FCP结合的众多Fx分子,有些结合在FCP内部的叶绿素附近,有些结合在FCP亚基之间或FCP与PSII核心结合的界面上,起着捕光和能量调节的作用。在FCP-D亚基中,Ddx616结合在叶绿素簇a602/a603/a609附近(图3B,C),可能是一个重要非光化学淬灭位点。
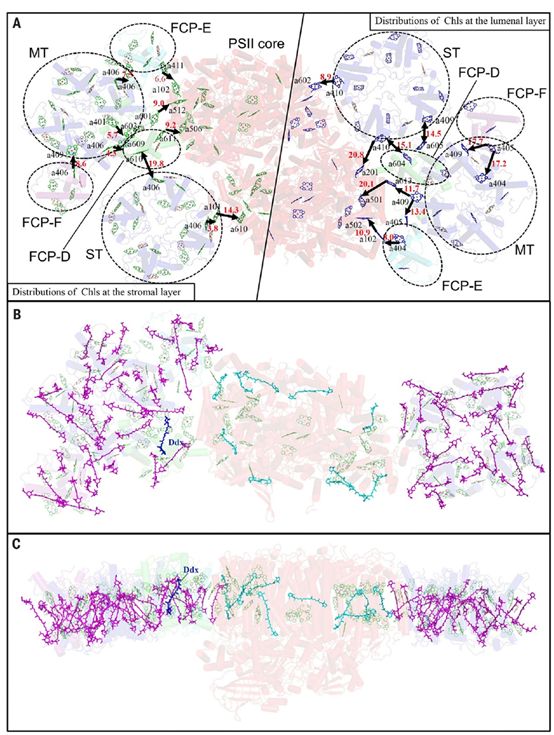 图3. PSII-FCPII色素排布网络和能量传递途径。(A) PSII-FCPII单体中靠近基质侧(左)和腔侧(右)的叶绿素排布网络和能量传递途径。 (B-C) PSII-FCPII单体中叶绿素和类胡萝卜素分子排布的基质侧俯视图(B)和侧视图(C)。绿色,叶绿素a(Chl a);小麦色,叶绿素c(Chl c);紫色,岩藻黄素Fx;青色,β-胡萝卜素;蓝色,硅甲藻黄素(Ddx)。
图3. PSII-FCPII色素排布网络和能量传递途径。(A) PSII-FCPII单体中靠近基质侧(左)和腔侧(右)的叶绿素排布网络和能量传递途径。 (B-C) PSII-FCPII单体中叶绿素和类胡萝卜素分子排布的基质侧俯视图(B)和侧视图(C)。绿色,叶绿素a(Chl a);小麦色,叶绿素c(Chl c);紫色,岩藻黄素Fx;青色,β-胡萝卜素;蓝色,硅甲藻黄素(Ddx)。硅藻PSII-FCPII的冷冻电镜结构揭示了硅藻PSII核心复合物中几个特有亚基的结构特征;发现了以往未鉴定出的FCP四聚体形式;揭示了FCP在硅藻PSII反应中心外周特殊的排布方式。该结构构建的硅藻PSII-FCPII复杂的Chls a/c和Fxs色素网络,提供了硅藻PSII在能量捕获、传递和激发能淬灭过程中的细节信息,为继续深入研究其超快动力学和理论计算奠定了结构基础;对于进一步深入了解硅藻的捕光和光保护机制,以及研究光合生物的进化也具有重要意义。
述评人简介:潘晓伟博士,中国科学院生物物理研究所副研究员,中科院青年创新促进会会员。主要研究领域为高等植物和藻类光合作用相关膜蛋白复合体的结构与功能。
参考文献:
1. X. Su et al., Structure and assembly mechanism of plant C2S2M2-type PSII-LHCII supercomplex. Science 357, 815 (Aug25, 2017).
2. X. Wei et al., Structure of spinach photosystem II-LHCII supercomplex at 3.2 A resolution. Nature 534, 69 (Jun 2,2016).
3. X. Pan et al., Structure of the maize photosystem I supercomplex with light-harvesting complexes I and II. Science 360, 1109 (Jun 8, 2018).
4. M. Goldschmidt-Clermont, R. Bassi, Sharing light between two photosystems: mechanism of state transitions. Current Opinion in Plant Biology 25, 71 (Jun, 2015).
5. A. V. Ruban, M. P. Johnson, C. D. Duffy, The photoprotective molecular switch in the photosystem II antenna. Biochim Biophys Acta 1817, 167 (Jan, 2012).
6. P. G. Falkowski et al., The evolution of modern eukaryotic phytoplankton. Science 305, 354 (Jul 16, 2004).
7. S. Malviya et al., Insights into global diatom distribution and diversity in the world's ocean. Proceedings of the National Academy of Sciences of the United States of America 113, E1516 (Mar 15,2016).
8. P. Kuczynska, M. Jemiola-Rzeminska, K. Strzalka, Photosynthetic Pigments in Diatoms. Mar Drugs 13, 5847 (Sep 16, 2015).
9. L. S. van Bezouwen et al., Subunit and chlorophyll organization of the plant photosystem II supercomplex. Nature Plants 3, (Jul, 2017).
10. W. Wang et al., Structural basis for blue-green light harvesting and energy dissipation in diatoms. Science 363, (Feb 8, 2019).
11. X. Qin, M. Suga, T. Kuang, J. R. Shen, Photosynthesis. Structural basis for energy transfer pathways in the plant PSI-LHCI supercomplex. Science 348, 989 (May 29, 2015).
来源:Science-AAAS ScienceAAAS
原文链接:http://mp.weixin.qq.com/s?__biz=MzI3NDY3NzQ2Mg==&mid=2247487661&idx=4&sn=a09f4c8a492fdfb85b1e24ca3932de39&chksm=eb113b14dc66b202e15a043991a63bf06a7cfc56850215ffe0c335aa5dbb474ae7491609442b&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

8月份我市CPI同比上涨1.0%

CPI、PPI连续下降:通缩压力显现,政策宽松空间增大
ACS Chem. Biol:植物色素用于哺乳动物细胞的光遗传学调控

2022年3月CPI同比涨幅扩大 PPI同比涨幅继续回落

2019年中国CPI上涨2.9%,创8年新高

31省份CPI出炉,22地物价降了!黑龙江啥情况?

食物掉色就不能吃了吗?植物色素的种类和性质
统计局:5月CPI同比增长2.7% 鲜果价格上涨26.7%
猪肉跌了!CPI时隔18个月重回“1时代”,感受到了吗?

7月份运城CPI同比上涨0.8%