科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-08-24
来源:X一MOL资讯
芳烃cis-二氢二醇类化合物是一类通过细菌双羟化酶催化芳烃的不对称双羟化反应得到的代谢产物。由于其官能团丰富且易于转化,从而得到广泛的关注,有机合成中得到了广泛的应用,实现了一大类天然产物和药物,如达菲、吗啡、河豚毒素(tetradotoxin)等的化学酶促合成(chemoenzymatic synthesis)。但是到目前为止,它们的合成却严重依赖于酶催化。化学合成这些代谢产物面临巨大的挑战。最近一个突破性贡献是由UIUC的David Sarah课题组做出的,他们发展一个光催化的去芳构化的策略实现了芳烃cis-二氢二醇类化合物的消旋合成(Nat. Chem., 2016, 8, 922)。然而,对映选择性化学合成此类代谢产物仍然是个巨大的挑战,到目前为止仅有一例通过手性池策略实现的报道。2013年,Metz和Sun以D-ribose为原料,经过九步合成了一个芳基cis-二氢二醇衍生物(Synlett, 2013, 24, 457)。
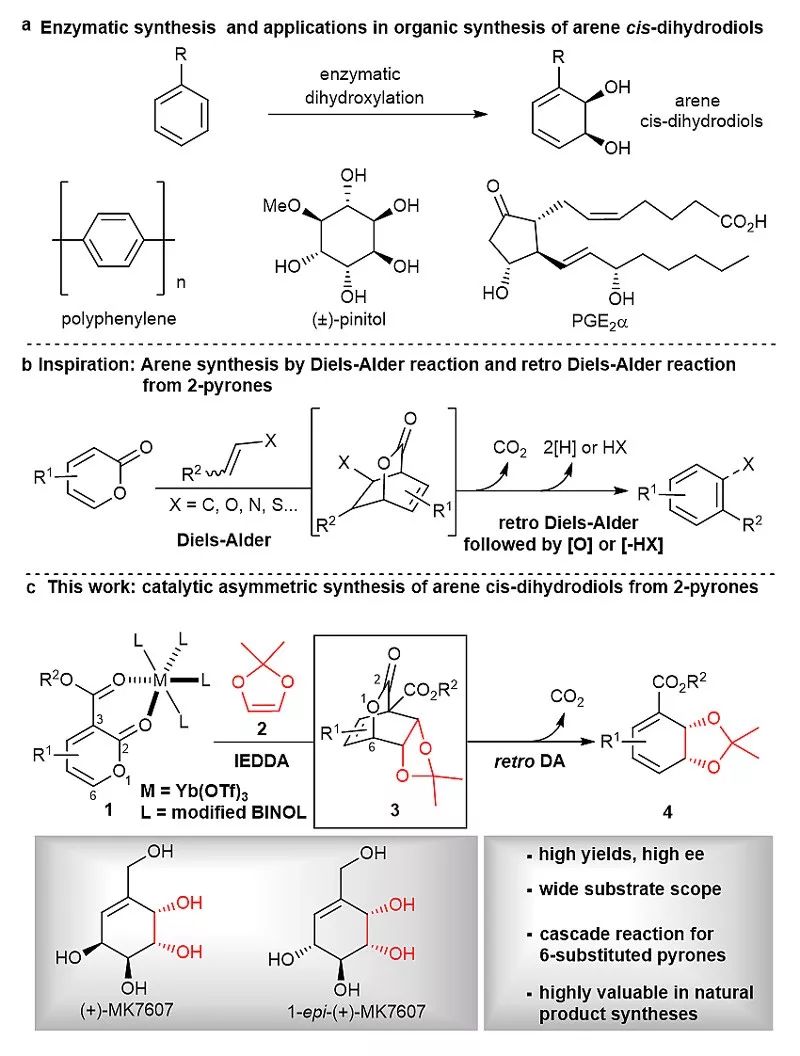
图1. 合成背景。图片来源:Angew. Chem. Int. Ed.
最近复旦大学化学系蔡泉研究组在《德国应用化学》(Angew. Chem. Int. Ed.)上首次报道了芳烃cis-二氢二醇的化学不对称催化合成。该策略通过三氟甲磺酸镱催化的2-吡喃酮1与烯二醚2的反电子需求的Diels-Alder反应以及逆Diels-Alder反应脱出CO2得以实现。该策略有广泛的底物适用性,并实现了活性伪糖类天然产物(+)-MK7607及合成活性类似物1-epi-(+)-MK7607的高效简洁全合成。
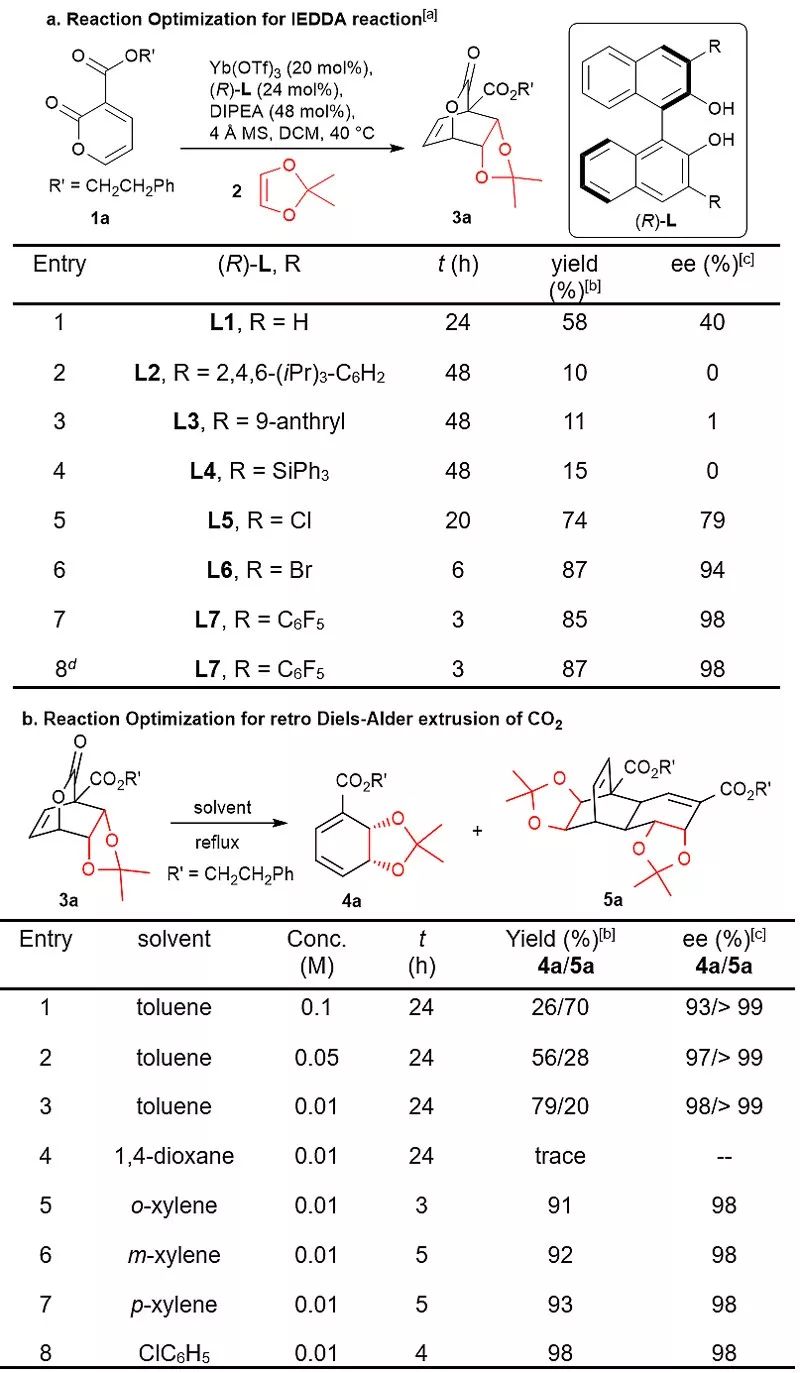
图2. 合成条件考察。图片来源:Angew. Chem. Int. Ed.
作者使用2-吡喃酮1和烯二醚2进行条件的考察。由于烯二醚2的双键没有发生极化,与烯基醚相比反应活性更加惰性。由此作者通过在BINOL的3,3'位引入吸电子的五氟苯基取代基来提高催化剂的活性,并给出给出较高的的对映选择性控制。接着作者考察了桥环内酯3a的逆Diels-Alder反应脱除CO2的反应条件。其难点在于产物4a的不稳定性,容易发生芳构化、二聚反应、6π电环化等副反应。经过大量的尝试发现其最优条件为以较低的浓度 (0.01 M) 在氯苯中回流。

图3. 底物拓展。图片来源:Angew. Chem. Int. Ed.
在最优条件下,作者对底物进行了拓展,如Table 2a所示,2-吡喃酮上的各种酯都能得到很好的兼容,以较高的产率和ee值桥环内酯产物3a-3e (76-86% 产率,92-98% ee)。在下一步的逆Diels-Alder反应中,目标产物4a-4e 很顺利的得到,并且没有ee值的降低。吡喃酮的4-位、5-位取代基同样能够得到兼容。为了验证反应的实用性,作者也尝试了化合物1h的克级规模合成,其产物的产率和ee值得到保持。
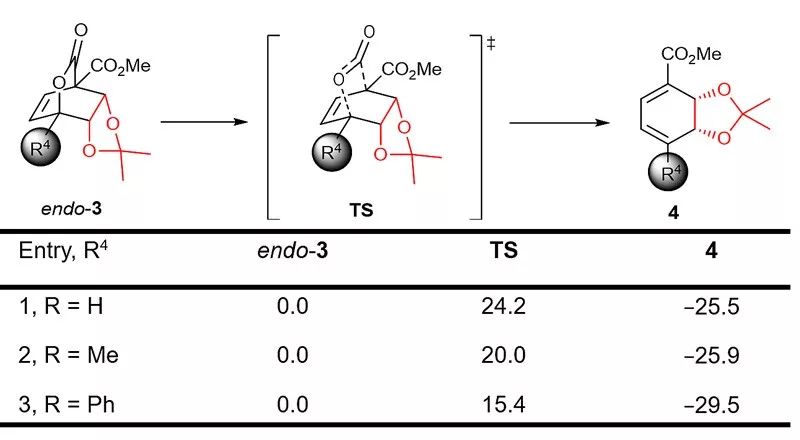
图4. DFT计算支持。图片来源:Angew. Chem. Int. Ed.
接着作者希望对6-位取代的吡喃酮进行考察。由于双季碳立体中心的形成,可以预想,第一步的Diels-Alder反应具有较大挑战。但是,所生成的桥环内酯3或许会因为6位取代基的引入从而在动力学和热力学上有利于逆 Diels-Alder反应脱除CO2的反应。作者与中国科学院上海有机化学研究所的郑超研究员合作,通过DFT计算的预测了该设想。计算的结果表明,随着各种不同6位取代基的引入,该位点的碳正离子的稳定性得到逐步的增强,从而使得脱除CO2的逆DA反应的能垒更低 (R4 = H, 24.2 kcal/mol; R4 = Me, 20.0 kcal/mol; R4 = Ph, 15.4 kcal/mol)。带着这样的预测,作者考察了不同6位取代的吡喃酮底物,发现该类型的底物能够在温和条件下实现相应的多取代以及多环芳基cis-二氢二醇产物的一步合成,并且较高的产率和几乎完美的非对映选择性、对映选择性得到几乎光学纯的产物(> 99% ee,> 99% dr)。
尽管芳基cis-二氢二醇产物在合成中已得到了广泛的应用,作者认为通过化学合成的方法也有其独特的优势。例如,相比较于酶催化,化学不对称催化合成能够通过配体或催化剂的调节,很容易的得到产物的一对对映体。为了验证该设想,作者通过(R)-构型的配体得到了与酶催化合成绝对构型相反的cis-二氢二醇产物4b。并以4b为原料通过简单的转化实现了活性伪糖类天然产物(+)-MK7607及合成活性类似物1-epi-(+)-MK7607的简洁全合成。该方法为该类活性分子的药物化学的研究提供了有效的思路。
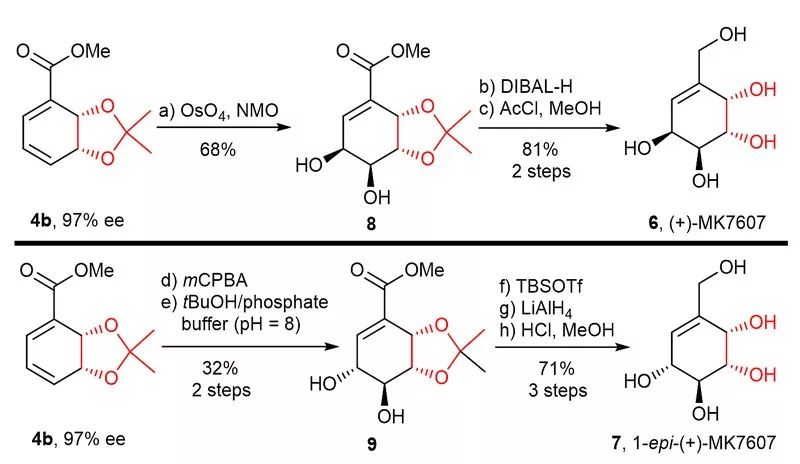
图5. 不对称合成(+)-MK7607及1-epi-(+)-MK7607。图片来源:Angew. Chem. Int. Ed.
综上,作者实现了芳烃cis-二氢二醇的首例化学不对称催化合成,其底物普适性广,对映选择性控制优秀,特别是对于6取代吡喃酮的底物能通过一步反应即可合成各种多取代和多环芳烃cis-二氢二醇产物。该策略为这类重要合成子的合成提供一种新的除了传统酶催化合成之外的一个可靠的选择。更重要的是,相比较于酶催化反应,化学不对称催化在合成的可操作性、某些特殊取代的底物合成以及不同绝对构型产物的立体选择性控制方面具有独特的优势。可以预想,该方法将在其它更加复杂的活性天然产物的合成中得到广泛的应用。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657618216&idx=5&sn=edee97ab22c6e5e1c3af865fe868c8c1&chksm=80f820f8b78fa9ee7513285f985beddbaf8a2921f94609ee0b638d22553c3fb3cb2bedb10541&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn