科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-09-24
来源:X一MOL资讯
如果说细胞是一个微型工厂,那么细胞内的酶就是这个工厂内的机器,这些纳米级别的机器无时不刻的催化着细胞内的多种化学反应。天然的生物催化体系通常在细胞这个微型工厂内会形成物理上、空间上组织有序的多酶复合体、酶分子脚手架或者反应微区,这种类似机器组装的高度组织性带来了高效的催化能力。然而,目前合成生物学中构建的人工合成体系失去了自然系统原有的协调运行机制,不但大大降低了整体的催化效率,也会导致代谢流不平衡,使带有毒性的中间产物发生积累进而增加了宿主细胞的代谢压力。
武汉大学刘天罡课题组、香港中文大学夏江课题组近期在Nature Communications 联合发表了题为“Modular enzyme assembly for enhanced cascade biocatalysis and metabolic flux”的论文,香港中文大学康巍博士、武汉大学马田博士为本文共同第一作者。
该研究采用一种人工蛋白骨架结构,该结构基于一对简单的多肽相互作用标签RIAD和RIDD,实现了两种酶体外以及体内的有效组装。RIDD是一段来源于cAMP依赖的蛋白质激酶A的由四十四个氨基酸构成的多肽,RIAD则是一段来源于激酶A锚定蛋白质的仅由十八个氨基酸构成的两亲性多肽。RIDD会自发形成生理条件稳定的二聚体,RIAD则会进一步与RIDD二聚体结合,形成稳定的三聚结构。通过在目的蛋白上分别融合表达这一对多肽标签,就能实现两个酶体外和体内的组装。该体系有以下几个优点:1)多肽标签较短,降低对酶本身活性的影响;2)亲和力高,能够确保酶复合物的完整性;3)能够以2:1的比例进行酶组装;4)可以将不同表达强度的酶在不改变酶结构的前提下,进行空间组装;5)特异高效结合,且生理状态下稳定。
首先,作者利用维生素K生物合成中的酶进行了体外组装实验。利用该技术进行体外组装时,能够观察到RIAD和RIDD可以有效地介导相关酶形成多种形态、催化亚基比例各异的多酶复合物,并且多肽标签并不会影响催化亚基的催化活性。通过调节催化亚基比例,多酶连续催化反应效率可以人为地进行调控,并在增加多比例组装时进一步提升产量。
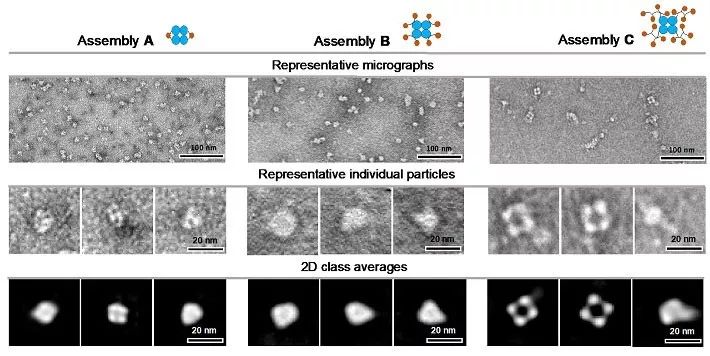
图1. MenD4-MenH2 (Assembly A), MenD4-MenH8 (Assembly B) and MenD4-MenH16 (Assembly C)酶组装体在透视电镜下的聚合结构
更重要的是,该技术同时在微生物体内针对重要的代谢节点实现了有效组装。
萜类是自然界中最为丰富的一类化合物,在生物医药、能源、食品和化妆品领域有着广泛应用。其合成途径可分为上下游,上游部分提供萜类合成前体——异戊烯基焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP);下游部分则通过对前体进行缩合、环化、氧化等一系列修饰,最终生成多样的萜类化合物。Idi为上游代谢途径的最后一个酶,负责催化IPP和DMAPP的异构化反应,该酶游离在细胞质内;CrtE是下游类胡萝卜素生物合成的第一个酶,然而,该酶分布在细胞膜上。IPP和DMAPP作为萜类合成的通用前体,当靶向合成类胡萝卜素时,上下游的空间效应降低了人工细胞工厂的合成效率,同时,上下游的不平衡也导致IPP和DMAPP的积累进而抑制了细胞生长。
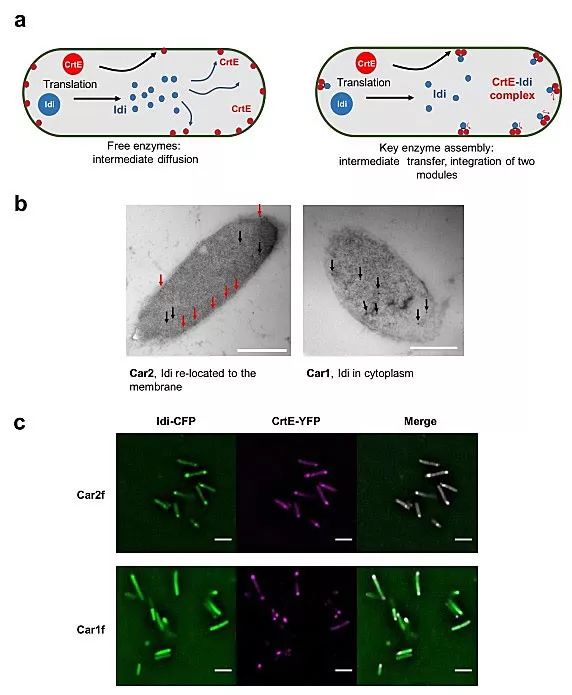
图2. 在细胞内组装类胡萝卜素生物合成的关键限速酶。(a) 不同空间分布的上下游关键节点酶的组装示意图;(b) RIAD-RIDD肽相互作用使Idi从细胞质再分配到细胞膜;(c) Idi-CFP和CrtE-YFP发生共定位。
通过利用RIAD-RIDD组装构建Idi-CrtE多酶复合物,作者在分布膜蛋白CrtE的细胞膜上发现了大量的Idi,同时,类胡萝卜素的合成通量发生了极大地提高。该技术将原本存在物理分割的代谢通路实现了链接,Idi-CrtE多酶复合物如同一个纽带,将更多的萜类合成前体引流至下游目标途径。通过在虾青素大肠杆菌高产菌株体内构建Idi-CrtE多酶复合物,虾青素产量提高了2.7倍,类胡萝卜素产量提高了5.7倍。通过在番茄红素酿酒酵母高产菌株体内构建Idi-CrtE多酶复合物,番茄红素产量提高了58%,达到2.3 g/L,与目前报道的酿酒酵母产番茄红素的最高产量在同一水平。
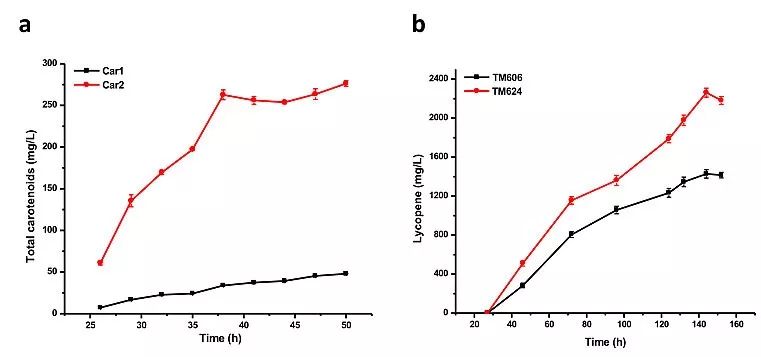
图3. Idi-CrtE多酶复合物分别在大肠杆菌(a)和酿酒酵母中提高了(b)目标途径的代谢通量
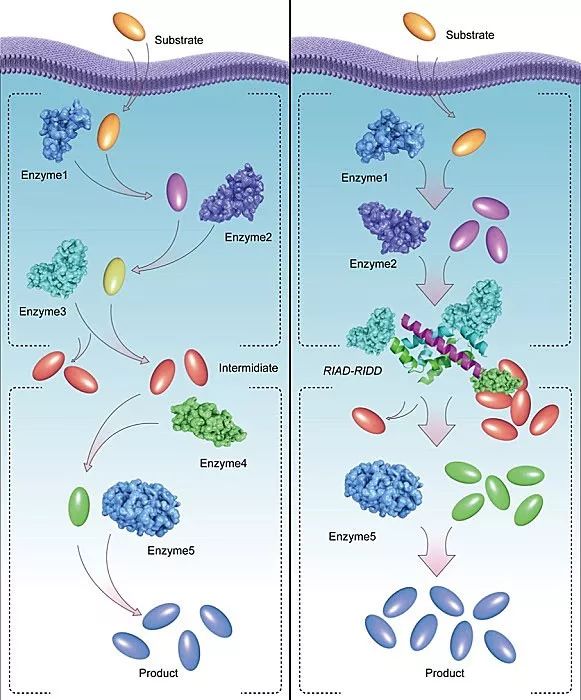
图4. 由RIAD-RIDD介导的代谢关键节点组装促进微生物细胞工厂的高效合成
通过构建多酶复合物的方式链接生物合成的关键代谢节点来实现目标途径产量的提升,尤其针对具有不同空间分布酶的人造代谢体系,不仅解决了底物传递通道问题,也减轻了人工代谢体系的不平衡问题,对于实现目标产物的创新高产具有重要意义。该技术丰富并拓展了人工蛋白骨架的应用环境及适用范围,是目前人工蛋白骨架技术发展中非常适合微生物体内使用并且实用有效的一种技术,其不仅为萜类化合物的高效合成提供一种新的策略和思路,也为多酶组装的相关应用及发展提供一个新的突破口。开发能够实现更复杂体系组装的人工蛋白骨架技术无疑将是未来合成生物学的一个热点。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657619979&idx=6&sn=68258854c56a7af9191922cc49c14d57&chksm=80f839dbb78fb0cd9ab7799a9e9280d66ae97f05a9ee1ce2441ebb72995de7806d224b514ad2&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn