科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-10-11
来源:ScienceAAAS
评述论文:Direct electrosynthesis of pure aqueous H2O2 solutions up to 20% by weight using a solid electrolyte (Science, 10 October 2019)
双氧水的分解产物是水和氧气,不会产生二次污染物,是一种环境友好的大宗化学品。双氧水内部的活性氧含量为47%,仅次于分子氧。
因此,它可作为氧化剂、漂白剂、消毒剂、聚合物引发剂等,广泛用于化工合成、造纸、纺织、环保、食品、电子、航天等行业。随着绿色化工过程的不断发展和国家环保法规的日益严格,双氧水作为绿色氧化剂和环境友好的漂白剂及消毒杀菌剂的应用日益广泛。如在绿色化工领域:己内酰胺、环己酮、对苯二酚、环氧丙烷等新兴清洁生产过程均以双氧水作为氧化剂;在环保领域:双氧水正在取代次氯酸盐成为主流的漂白剂和消毒杀菌剂,尤其是在消毒杀菌方面,双氧水有望替代氯气,作为城市饮用水的漂白和消毒剂,这些都促使双氧水产量保持持续的增长。
目前,全球的双氧水总生产能力达到了2200万吨/年,并且其生产能力以年平均8%~11%的速度增长。国外的双氧水生产商主要集中在比利时的Solvay公司、德国的EVONIK(Degussa)公司、法国的Arkema公司、美国的FMC公司、芬兰的Kemira公司、瑞典Eka Nobel公司和日本的MGC公司等,其中,比利时的Solvay公司为全球最大的双氧水生产公司,约占全球产能的35%。
我国国内的双氧水产能达到了约为1300万吨(以27.5 wt.%来计)。我国近年双氧水生产能力增长的主要驱动力是以双氧水为原料生产己内酰胺和环氧丙烷的技术开发成功,并进一步形成生产规模,需要大量的双氧水配套原料。此外,随着国民生活水平的提高,双氧水作为饮用水、食品添加剂的消毒杀菌剂的应用,将会进一步的扩大双氧水的需求量。
自从1818年法国化学家Thenard采用湿化学方法发现双氧水物质后,双氧水的合成一直是工业界和学术界关注的课题。其合成的工艺从早期的湿化学(wet Chemical Process)到电化学合成(Riedel–Loewenstein process电解硫酸铵和硫酸)、异丙醇法(Shell Process)再到蒽醌法(Riedel–Pfleiderer process)以及近半个世纪的研究广泛的氢氧复合合成法等等[1]。
目前,发展最为成熟的方法是蒽醌法也叫自氧化工艺(AO Process),其主要包括蒽醌的加氢、蒽氢醌的氧化、萃取、再生等步骤,蒽醌在整个过程中实现循环使用。目前蒽醌法生产双氧水的产能占据了全球产能的95%,占据了我国国内产能的98%。
然而,蒽醌法生产双氧水工艺的最大问题在于:一是危险性,在氧化蒽氢醌的过程中,产生的双氧水溶解在芳烃等工作液溶剂中,工艺控制参数要求苛刻;二是污染性,生产蒽醌原料的过程中不仅会产生大量酸性废水,而且在蒽醌法制备过程中萃取以及洗涤工作液的过程中也会产生含有机物的废水。基于蒽醌法存在的问题,采用氢气和氧气直接进行合成双氧水无疑是一条环保、绿色的工艺路线。
采用氢气和氧气直接进行合成双氧水是一项非常有挑战的课题。其难点在于:一是爆炸危险性,由于氢气在空气中的爆炸范围比较大,约为4-75.6 v/v%,为了避免这种危险性,一般会加入惰性的气体如二氧化碳、氩气或者是氮气,但是这种方法无疑降低了生产的效率以及产品的浓度。
而且为了提高双氧水的生产效率,一般会采用气液固三相操作单元,增加了溶剂与双氧水的分离、纯化步骤,进而会降低双氧水的品质[2,3],如图1A。二是氢氧直接反应的可控性差,其主要包括氢氧反应生成水、氢氧反应生成双氧水、双氧水加氢生成水和双氧水分解反应,上述的反应全部是热力学稳定且强放热的反应,如何控制氢氧生成双氧水而抑制其他反应是非常难实现的,尤其是在反应中采用的催化剂基本为贵金属催化剂,如Pd、Pd-Au、Pd-Sn等[2,3]。
相比较而言,采用电化学合成的方法可以有效避免氢氧的直接混合,把氢氧的氧化还原反应分割成两个独立的电池反应,有效避免了氢氧直接混合的爆炸性问题。但是传统的电化学方法主要采用液体电解质,为了得到纯双氧水需要进一步的分离纯化过程,且此过程反应速率慢、产品浓度以及法拉第效率非常低,难以实用化。
为了解决上述的问题,美国莱斯大学的Haotian Wang及其团队创新性提出了采用多孔固体电解质实现了电化学方法一步氢氧直接合成浓度高达20 wt.%的高纯双氧水,而且此过程不需要后续的分离纯化,具有很强的竞争优势。
文章发表在2019年10月10日上线的Science上(文末“阅读原文”可查看原文)。文章指出,采用电化学固体电解质成功实现了H+和HO2-的结合生成纯双氧水溶液。通过优化2-电子氧的功能炭黑催化剂,研究团队实现了双氧水选择性为90%,收率高达3660 mole/(kgCat. Hr)的合成研究成果。且通过调控去离子水的流通量可以实现浓度最高为20 wt.%的双氧水合成,且催化剂的活性和选择性在100 hr的运行中没有明显的衰减。
研究者及其团队很有创意地设计了采用多孔固体电解质的电化学合成双氧水的装置,如图1B。其主要包括了氢氧物料分别通过的含有氢氧化(HOR)和氧还原(2e--ORR)催化剂的气体扩散层电极,阳极和阴极分别夹杂着阳离子交换膜(CEM)和阴离子交换膜(AEM),中心部分为薄的固体电解质(Porous SE,其主要是结合H+与HO2-生成H2O2,并且提供去离子水的流通区域)。研究者在阳极HOR材料上选择了具有高H2-to-H+转化率的Pt/C催化剂,在阴极2e--ORR材料上选择了具有高比表、低成本的炭黑催化剂,多孔固体电解质选择了具有高离子电导率、高稳定性的磺酸基修饰的苯乙烯-二乙烯基苯共聚物微球。
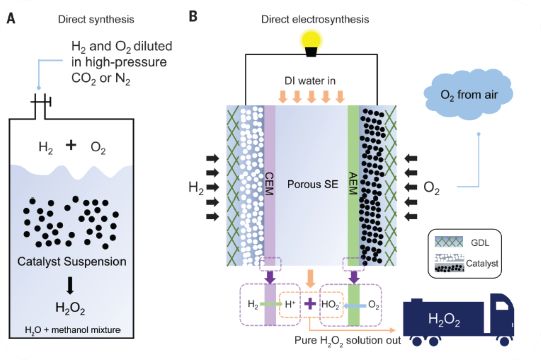
图1.氢/氧直接复合合成H2O2的两种不同制备工艺示意图
A、采用氢气、氧气直接混合方式的合成路线;B、采用以固体电解质的电化学方法合成路线
在上述电化学合成H2O2的基础上,研究者重点开展了以下三个方面的工作:一是发现阴极材料-炭黑酸处理后的氧覆盖度与H2O2的选择性和活性有很大的关联性,随着炭黑的氧覆盖度增加,H2O2的选择性会增加,经过优化,具有10%的氧覆盖度的炭黑(CB-10%)作为阴极材料是比较理想的。二是在固定去离子水流量下,优化了装置的电化学参数,在电势为0.61 V,电流密度为200 mA/cm2的情况下,H2O2的法拉第效率(FE)达到了~90%,也就是说,在同时考虑了阴阳极催化剂的情况下,H2O2的生产效率达到了3660 mol(kgCat*Hr),而且研究者认为其他的固体电解质材料如OH-的聚合导体和无机的阳离子导体CsxH3–xPW12O40都可以很好实现H2O2合成。三是优化去离子流速与双氧水浓度的关系,在保持H2O2生成电流固定条件下,通过调控去离子水的流量可以实现20 wt.%以下,不同浓度的高纯双氧水的连续合成。而且,通过连续100 hr的长周期运行,验证了设备的鲁棒性和催化剂的稳定性。
此外,研究者采用自合成的H2O2净化了当地的雨水,使当地雨水中的有机物含量(TOC)从未处理前的5 ppm降到了当地标准的2 ppm以下,验证了设备合成双氧水的经济性和环境友好性。值得一提的是,研究者进一步简化了制备双氧水的设备,从原来的H2//SE//O2体系简化到O2//SE//H2O,再简化到Air//SE//H2O体系,H2O2的选择性基本都大于90%。为了验证固体电解质设备的规模放大性,研究者将电极的面积从4 cm2放大到80 cm2,此时H2O2的选择性降低到了80%,生产效率为0.3 mol/hr,且生产20 wt.%的双氧水量为5.4 ml/hr。
尽管在产业化的道路上还需要一定的时间,不过,研究者提出了一种全新的生产纯度高、绿色、安全、浓度可调控的氢氧复合直接合成双氧水的路线,尤其是在特殊的、高纯双氧水的应用领域,最先有望替代传统的合成方法。此研究也为其他液体化学品的合成,提供了一个全新的电化学合成思路。
述评人简介:苏宏久
博士,中国科学院大连化学物理研究所研究员,中国科学院青年创新促进会会员,主要从事无机氧化物可控制备及其应用研究。
参考文献:
1. Chanchal Samanta, Direct synthesis of hydrogen peroxide from hydrogen and oxygen: An overview of recent developments in the process, Applied Catalysis A: General 350 (2008) 133–149.
2. Simon J. Freakley, Qian He, Jonathan H. Harrhy et al., Palladium-tin catalysts for the direct synthesis of H2O2 with high selectivity. Science 351(2016) 965-968.
3. Jennifer K. Edwards,1 Benjamin Solsona,1 Edwin Ntainjua N, et al., Switching Off Hydrogen Peroxide Hydrogenation in the Direct Synthesis Process. Science 323(2009)1037-1041.
来源:Science-AAAS ScienceAAAS
原文链接:http://mp.weixin.qq.com/s?__biz=MzI3NDY3NzQ2Mg==&mid=2247488278&idx=5&sn=dfba6bfb31b8b602f2769ca652cfeb74&chksm=eb1138afdc66b1b925a23079d35ab35478d8bbb1d3db1f88bcf9c99bfb04b6de665167ef31ab&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
金属所纳米碳材料高效催化过氧化氢电合成研究取得进展
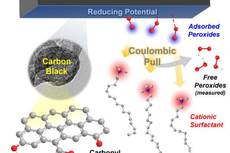
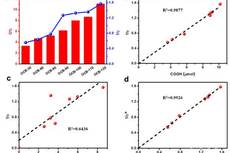
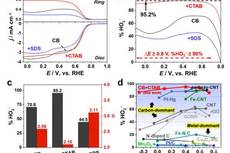
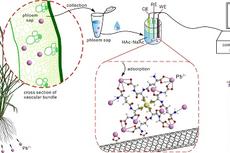
合肥研究院利用功能化碳纳米管材料实现对水稻伤流液中重金属离子的选择性检测----中国科学

前沿透视:电化学制备过氧化氢电极设计领域取得进展

宁波材料所在电化学制备过氧化氢研究中取得进展

研究发现内源性过氧化氢近日节律震荡调控生物钟

合肥研究院电催化合成过氧化氢研究取得进展

金属所纳米碳材料高效催化过氧化氢电合成研究取得进展

超显微镜观察到锂离子在双层石墨烯中迁移

宁波材料所陆之毅团队联合陈亮研究员团队在电化学制备过氧化氢电极设计领域取得进展

中科院科学家在电化学制备过氧化氢研究中取得进展