科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-01-05
来源:高分子科学前沿
菌类生物体内的电子转移与控制是微生物生存和活动的重要组成部分之一,其具体表现为细菌呼吸时的级联反应推进最终的电子转移至位于细胞外部的电势更高的氧化还原受体。这类在细菌增殖过程中可持续的电子外流过程会产生积聚的还原势能(Eh),同时也会为其周围的环境提供一定的能量。这类积聚的还原势能不仅从微观层面上证实了微生物在细胞体外会有电子转移的过程,也被科学家们用来进一步探究微生物的成长过程,并将其应用在生物电子合成领域。然而,对于该类电势在特定培养皿和培养溶液中的应用却一直被人们所忽视,仍待发掘。
通过使用活性组织或细胞来协助合成新型材料,尤其是工程化的活性材料这一想法,成为了21世纪生物合成领域的一大焦点。工程化活性材料通常由合成类的乙烯基聚合物组成,其聚合物的物理化学性质对应的细胞表型都分别可以通过自由基聚合来把控。因此,通过微生物所产生的还原势能来合成乙烯基类聚合物的想法便应运而生。在最近的报导中,通过细菌还原系统,已经能够实现将铜类二价化合物还原至一价化合物,从而激活乙烯类单体发生自由基原子转移聚合反应(ATRP)。然而,由于依赖铜类金属催化剂,而金属类反应物本身又具有一定的细胞毒性,因此大大限制了该类方法的发展。
为了大大拓展该类方法的普适性,降低反应所可能产生的细胞毒性,澳大利亚墨尔本大学Greg G Qiao教授团队开发了由一种无金属参与的细菌电子回流推动产生的自由基引导可控自由基聚合反应(BacRAFT)。他们证实了还原势能可以在一系列活性的微生物培养环境中生成,利用卤代芳基重氮盐类氧化还原活性物作为聚合引发剂,通过自由基可逆加成断裂链转移聚合方法,合成良好可控的乙烯基类聚合物。
【方法的建立】
首先,为了验证方法的可行性以及挑选出较为理想的细菌,作者使用手持ORP传感器(银/氯化银作为参考),测试了几种典型的细菌接种在成长和增殖24小时之后的还原电势能Eh。作者以大量的变化变量和不同的细菌测试结果作为支持,最终选择了大肠杆菌(菌株MC4100)和鼠伤寒沙门氏菌(菌株TAS2010)作为实验使用对象,其原因主要是它们可以达到相对较低的还原电势能。在细菌增殖4小时之后,其还原电势能达到小于负200毫安。并且,对于大肠杆菌而言,不摇动的培养皿可以产生最低的还原电势能,改变无氧或者有氧环境并不会对其电势增长的动力学产生影响。
在决定了菌类的选择之后,作者尝试建立起一个完整的反应路径(图1)。卤代芳基重氮盐类氧化还原活性物,被选为了该聚合反应的引发剂,原因是其报导的还原电势能恰巧为负200毫安,使其可以完美接受细菌氧化还原后所转移的电子(负300毫安)。并且,该类化合物的电子还原反应已被广泛研究,还原后所产生的活跃的卤化芳基自由基可以引导诱发之后的可控自由基反应。除此之外,在与两个细菌菌株培养24小时之后,它也并未呈现出十分明显的毒性。这些综合因素使其完美胜任该聚合反应的引发剂。
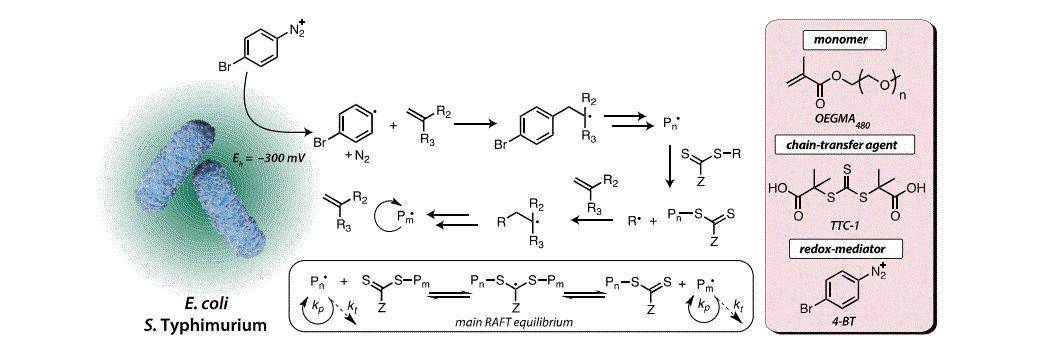
图 1:反应合成方法和具体反应路径原理
其次,作者选择寡聚乙二醇甲醚甲基丙烯酸酯(OEGMA)作为反应单体,M9作为基础培养基,RAFT作为反应方法,将反应混合物和两种细菌同时分别培养至一个较高的最初细胞数目之后,再充入氮气去氧。尽管在反应剂加入的初始阶段,电势一度上升到正值,但是在混合两个小时之后,反应的电势再度达到负值。在8个小时后,反应单体的反应率达到70%,而对比不添加引发剂或者无细菌培养的环境,在这种情况下它是没有发生反应的。并且,作者通过对其他类型的乙烯基类反应单体(例如丙烯酸类,丙烯酰胺类,苯乙烯类单体)进行聚合,进一步证实了该方法的普适性。作者也尝试直接将还原电势作用在RAFT反应剂上,但该方法并没有成功,不可逆的RAFT反应断裂链是导致其失败的直接原因,这也间接证实了加入卤代芳基重氮盐类引发剂的必要性和重要性。
【方法的验证与优化】
之后,作者分别对这两个细菌环境下的聚合反应进行了反应动力学的测试(图2)。结果证明其反应单体的反应率随着时间线性增加,符合准一级反应方程。这结果不仅证实了在反应过程中自由基的稳定输出,也说明了聚合反应可控和RAFT反应剂的高活性。最终分别在各个细菌环境下所合成的高分子不仅具有十分低的分散系数(Đ < 1.3),其反应率也都超过了70%。
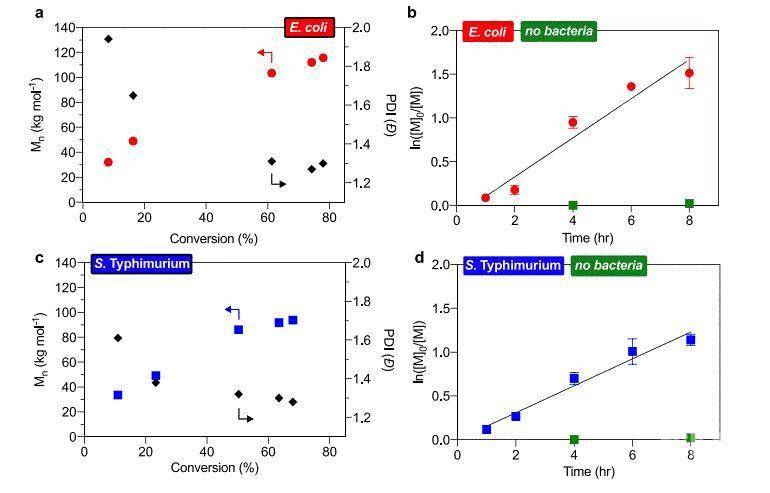
图 2:在大肠杆菌和鼠伤寒沙门氏菌中聚合反应的动力学。a,b为在大肠杆菌环境(红点),c,d为在鼠伤寒沙门氏菌环境(蓝点)。绿点则为不使用细菌的环境,作为参照。
在BacRAFT方法建立的基础上,作者尝试通过改变细菌环境来观察其对聚合反应的影响。首先,两种活性细菌的上层清液被分离出来,用来测试脱离细菌的溶液环境下单体的反应情况,在4小时后作者并未观测到聚合反应发生,证明细菌的存在是必要条件。其次,作者利用超声将两种细菌进行裂解,来评估达到与引发剂相互作用和创造自由基的要求下所需的细菌表面膜的完整度。在这一情况下,聚合反应在4小时内达到了很高的反应率,作者认为其原因是细菌在裂解下所排除的微生物质或是未完成的裂解步骤中仍然存活的细菌所带来的影响。最终,作者尝试通过加热使所有的细菌失活,在失活状态下进行聚合反应。令人意外的是,在该条件下,大肠杆菌作用下的反应仍然可以达到一个相对较高的反应率,而鼠伤寒沙门氏菌作用下则未发生显著反应。这种热刺激下的与膜相关的回应现象仍然有待继续深入研究。但值得注意的是,由裂解和加热细菌所最终生成的聚合物,相较于不做任何处理的细菌环境中所合成的聚合物而言有更高的分散系数和较低的分子质量。该现象类似于自由基聚合反应,表明有很多短分子链在反应的最初阶段被同时生成,也从侧面说明了稳定的还原势能供给的缺失。
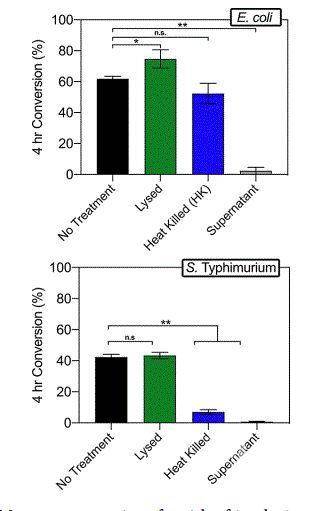
图 3:不同外部作用下两种细菌环境中的聚合反应的单体反应率。
另一方面,通过基因技术,作者改变鼠伤寒沙门氏菌细菌中的氧化还原介质来控制反应速率。结果证实细菌中的氧化还原介质在反应过程中起到了运输电子到反应引发剂的作用,并且可以通过基因技术进行宏观干预。
【细菌供给还原势能原理的推测】
最后,结合已有的数据,作者对细菌供给还原势能的机理进行了预测。活性微生物在反应过程中扮演着关键的角色,它们不断地将氧化还原介质从细菌里层的细胞质膜内推送到细胞外的引发剂中,在创造自由基调控中起到了稳定和促进的作用。
【总结】
作者通过对两种细菌(大肠杆菌和鼠伤寒沙门氏菌细菌)电子回流所产生的还原势能,来供给卤代芳基重氮盐类化合物,从而源源不断地产生自由基,在细菌培养皿环境内引发乙烯基类单体的可控自由基聚合反应。其所产生的聚合物可控、选择多样化、具有低分散系数、可在末端功能化。作者对反应的具体机理也进行了大量的研究,最终发现细菌通过氧化还原介质不断地运输电子到引发剂中。并且,活性微生物的存在对反应的稳定可控起到了关键性的作用。该方法的诞生,为工程化活性材料的研究打开了一扇崭新的大门。
来源:Polymer-science 高分子科学前沿
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5NjM5NzA5OA==&mid=2651767306&idx=6&sn=94cce4951a9c3687f53c3a1bde241204
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn