科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-01-28
来源:病毒学界
PARPs (Poly(ADP-ribose)polymerase)是一类负责将ADP-核糖基团转移至靶蛋白并对靶蛋白进行ADP核糖基化(ADPr)修饰的蛋白质超家族。与其他蛋白翻译后修饰(甲基化,磷酸化等)类似,ADPr修饰也是可逆的过程,它们广泛参与到DNA损伤修复,转录调控,染色体蛋白重构等重要的生物学过程。在哺乳动物体内,目前一共发现17个PARP家族成员,被命名为PARP1-16,其中PARP5有PARP5a和PARP5b两个亚型。近年来的研究表明,PARPs不仅在维持基因组稳定性和调节信号通路等方面起着不可替代的作用,而且在抗病毒天然免疫中发挥着重要的调控作用。
近日,福建医科大学郑春福教授应邀在Trends in Microbiology发表综述:When PARPs Meet Antiviral Innate Immunity. 系统综述了相关领域的最新研究进展,总结了PARPs在调节机体抗病毒天然免疫中的作用及其分子机制。非常值得一提的是,这是郑春福教授发表的第100篇SCI文章。
该文重点阐述了PAPRs家族成员在抗病毒天然免疫信号通路中的调节功能。天然免疫是抗病毒免疫的第一道防线,在控制病毒的感染和复制过程中发挥重要的作用。经典的抗病毒天然免疫是由模式识别受体(Pattern-recognition receptors, PRRs)介导的一型干扰素(Type I interferon, IFN-I))释放和下游JAK-STAT (Janus kinase-signal transducer and activation of transcription)信号通路诱导产生大量的干扰素诱导基因(Interferon-stimulated genes, ISGs)组成的。

图1. PARPs家族成员调控抗病毒天然免疫信号通路
PARP13,又被称为ZAP (zinc-finger antiviral protein),是目前研究较为深入的具有抗病毒功能的PARPs家族成员之一。ZAP不仅能直接通过结合RNA病毒的基因组以及mRNA并介导它们的降解,从而抑制病毒的复制,而且能通过与模式识别受体RIG-I (Retinoic acidinducible gene-I)结合以促进RIG-I的寡聚化,从而增强RIG-I的信号传递功能以及介导的IFN-I的产生。此外,某些PARP,如PARP9对JAK-STAT信号通路也具有调控作用。PARP9通过与E3 泛素连接酶DTX3L (E3 ubiquitin ligase Deltex E3 ubiquitin ligase 3L)相互作用并形成复合物,进一步促进STAT1的入核及对ISGs的转录调控功能。
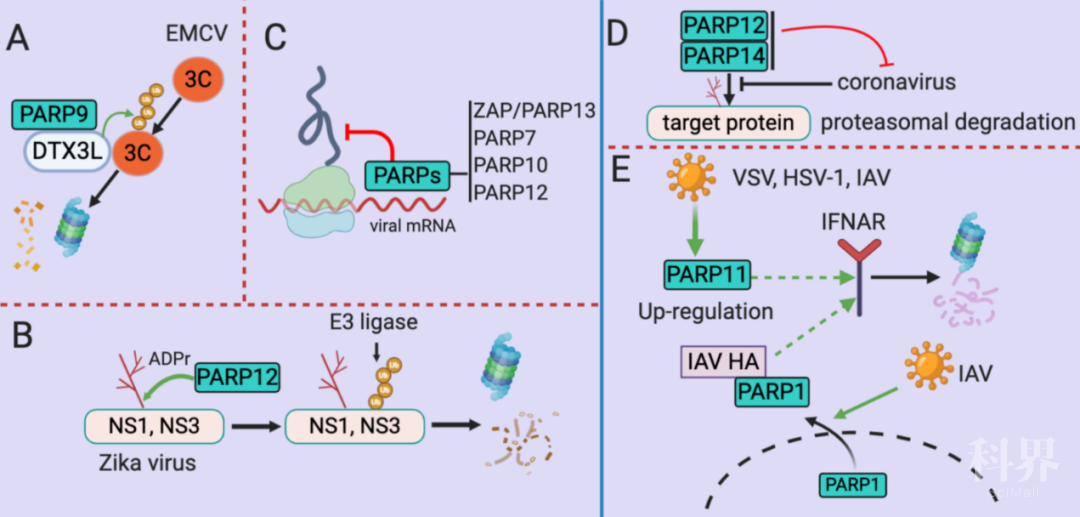
图2. PARPs家族成员的直接抗病毒作用以及病毒的免疫逃逸策略
除了促进宿主的抗病毒天然免疫反应,有些PARPs家族成员还协助病毒完成免疫逃逸。PARP11可促进I型干扰素受体(IFN-α/β receptor, IFNAR)被蛋白酶体途径降解;PARP1在正常生理功能下,通常定位于细胞核中,而在面对甲型流感病毒(Influenza A virus, IAV)感染时,IAV 表达的血凝素(hemagglutinin, HA)可将PARP1从细胞核带入细胞质,并进一步诱导IFNAR的降解。此外,冠状病毒(Coronavirus, CoV)可通过表达含保守性macrodomain结构域的病毒蛋白,以拮抗PARP12和PARP14的抗病毒功能,达到免疫逃逸的作用。
目前已知的参与抗病毒天然免疫调控的PARPs主要针对RNA病毒具有限制作用,而在应对DNA病毒感染时的天然免疫调控功能知之甚少;此外,所涉及的模式识别受体也非常有限,目前为止,仅发现对RIG-I介导的天然免疫反应具有调控功能。因此,在未来的研究工作中,或许可深入探索PARPs在抗DNA病毒天然免疫中的作用,以及在其他模式识别受体类型,如TLRs (Toll-like receptors) 或DNA受体如cGAS-STING介导的天然免疫信号通路中的功能。PAPRs介导的抗病毒天然免疫将是未来非常有潜力和价值的研究领域。
第一作者为朱惠芳(中国科学院博士),赣南医学院第一附属医院,儿童医学中心,新生儿科,讲师。通讯作者为郑春福,福建医科大学特聘教授
来源:viramedia 病毒学界
原文链接:http://mp.weixin.qq.com/s?__biz=MzIyMzQ3NTMyMQ==&mid=2247503855&idx=1&sn=c275a5d082c57c57693696a55b08d87b
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

病毒,不单单是“祸害”
磷酸伯安喹
新冠病毒侵染的磷酸化蛋白质组全景图
滴灌到底选择磷酸二铵还是磷酸一铵?
磷酸二苯酯
5'-三磷酸腺苷
磷酸氧钛钾
磷酸氯喹啉

我国首个P4实验室正式运行,致力于最危险病毒研究
磷酸三钠