孙熙宸
加好友
孙熙宸 2019-12-10
来源:纳米人

研究亮点:
1. 提出新概念,使用适配体修饰介孔硅纳米粒子作为拖拉机特异性拖运致癌性外泌体至小肠进行排泄;
2. 纳米粒子-外泌体作为单一体通过穿胞作用穿越肝胆细胞;
3. 通过清除致癌性外泌体,实现体内控制肺转移。
研究背景:
血液物质通常通过两种途径从全身循环中排出:(1)肾脏滤过,排泄到尿液中;(2)肝胆清除,通过Oddi括约肌进入小肠。小于6 nm的物质通常通过肾小球滤过而被清除。不能被Kuffer细胞立即捕获的较大物质通常通过肝胆清除进入小肠而被清除。
外泌体是由所有细胞产生和释放的细胞外囊泡。纳米大小的细胞外囊泡(40–150 nm)自然存在于血液中,并参与细胞间的通讯。大小和膜脂质双层有助于它们有效进入其他细胞。致癌外泌体在特定器官部位定居,并通过其整合素介导的与器官特异性常驻细胞的融合,启动转移前生态位的形成。外泌体的表面富含各种表面生物标志物,包括来自原始细胞的四跨膜蛋白(CD9,CD63,CD81和CD82)和表皮生长因子受体(EGFR;或ErbB-1;HER1)。EGFR是一种重要的跨膜蛋白,可通过其胞外域与其特异性配体结合而激活。
人工智能纳米材料可以在体内识别其靶标(酶,受体,细胞等)并选择性地结合它们。研究人员证明了,偶联在一起的双抗体或双适体可以在体内以高特异性捕获稀有循环肿瘤细胞(CTC),这是因为它们能够识别CTC上的两个生物标记并用双手抓住它们。
成果简介:
有鉴于此,福州大学贾力教授团队利用中空介孔二氧化硅纳米粒子(MSNs)作为拖拉机,将结合的外泌体从循环系统中拖入胃肠道。即:用EGFR靶向适配体功能化的带正电的介孔二氧化硅纳米粒子(MSN-AP)特异性识别并结合血源性带负电荷的致癌性外泌体(A-Exo),并将A-Exo穿过肝胆层和Oddi括约肌拖入小肠。该创新概念和生物技术方法为将有害的循环生物危害倾倒入小肠开辟了一条途径。
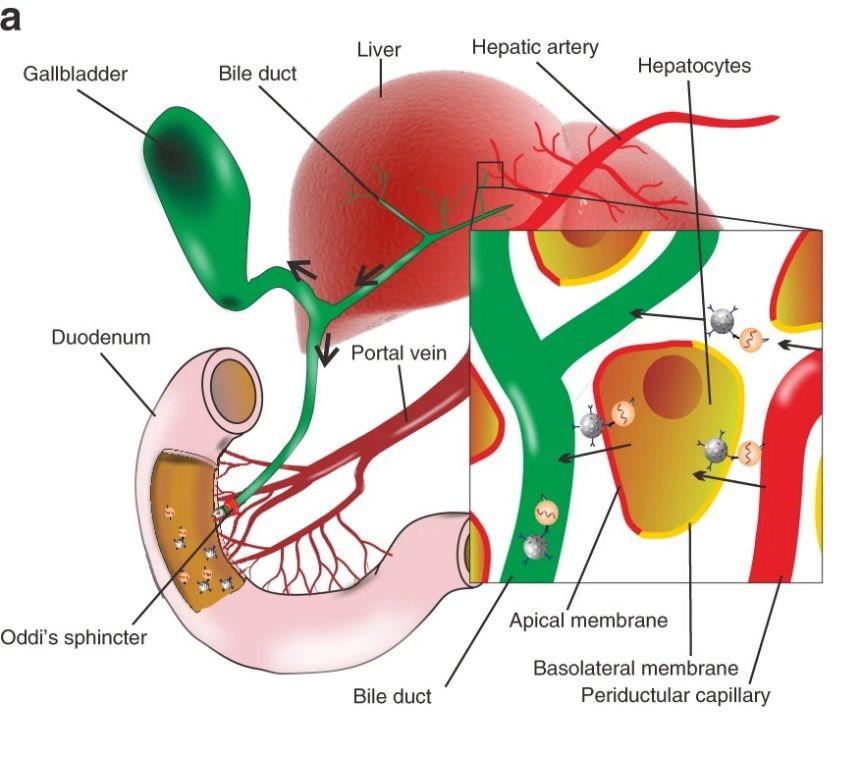
图1. 示意图
要点1:材料制备
通过超速离心从A549细胞培养上清液中分离出A-Exo和从人胚肺成纤维细胞培养基中分离出H-Exo作为对照。并分析其相关生化特性,发现只有A-Exo表达EGFR。
同时,研究人员制备了正负两种电荷的纳米介孔硅材料,并利用抗EGFR DNA适配体功能化。
要点2:MSN-AP与A-Exo体外特异性结合
然后,研究人员探究了MSN是否可以特异性识别并结合外泌体。通过共聚焦显微镜和流式细胞术分析,MSN-AP和MSN-AP-都与A-Exo特异性结合,与EGFR表达低的H-Exo几乎没有结合。结果还表明带正电的MSN-AP比带负电的MSN-AP更能吸引和结合A-Exo。
分析了MSN-AP和A-Exo之间的分子间识别和结合力。使用最胡克定律来评估分子间力,并利用AFM测定。力分布反映了当分子间距离达到最大值(直到键突然断裂)时施加到MSN-Exo键上的力。结果显示平均分子间力为200 nN,最大距离为〜70 nm,这代表了MSN-Exo键的识别力和电荷力。该结果表明静电力是形成MSN-Exo的主要力。
要点3. MSN携手Exo一起穿过肝细胞
为了研究共轭MSN-Exo是否可以穿越一系列肝细胞,研究人员使用延时图像序列和transwell等实验,表明MSN-Exo,MSN-AP和A-Exo容易渗透胆管细胞,内皮细胞和LO2细胞,但却容易被Kuffer细胞吞噬,然而研究人员表示这不能代表MSN-Exo在体内的状态。
另外,通过细胞通路抑制试验表明,MSN-Exo可以通过穿胞作用穿过LO2细胞,内吞作用和胞吐作用是MSN-Exo跨LO2单层运输的主要渠道。
要点4. Exo在体内分布、排泄及控制肺转移
通过尾静脉注射,进行一系列实验发现,血液中的MSN-AP有助于A-Exo而不是H-Exo分布到肝脏,然后重新分布到小肠进行排泄,这与特异性识别有关。
然后,研究人员又检查了血液中A-Exo的减少是否可以减弱A-Exo诱导的肺癌转移。结果显示了致癌性外泌体能诱导的A549 CTC向小鼠肺的器官性转移,同时能被MSN-AP治疗抑制。
小结:
总体而言,智能设计的安全生物材料可以准确地识别,结合并从血液中拖曳目标性生物危害物进入胆管以消除。这项研究开辟了视野,只要能够确定生物危害的分子结构和理化特性,就可以通过Oddi括约肌将血液中引起疾病的生物危害转入小肠。
来源:nanoer2015 纳米人
原文链接:https://mp.weixin.qq.com/s?__biz=MzUxMDg4NDQ2MQ==&mid=2247512486&idx=7&sn=2dd7a7821babb9355f89a688a60fd981&chksm=f97edea4ce0957b2d8e3b3140875ed6ec17ce421d700da470641eebc05f4f0fbd6a702e5b3e7#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

【走近桂籍科学家】用纳米武装电池新世界
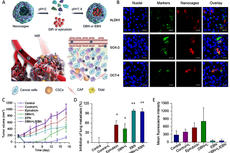
上海药物所发现仿生纳米笼可特异性靶向肿瘤干细胞抗肿瘤转移
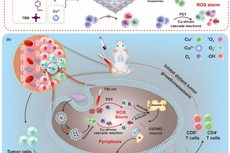
理化所等在特异性诱导肿瘤细胞焦亡纳米药物研究中获进展
外泌体大突破:吉林大学等开发细胞纳米化生物芯片,显著提高外泌体产量和核酸包载效率

研究发现狼疮特异性B细胞干预新靶点

研究:配位数精准调控钼单原子纳米酶特异性

乳腺细胞发育中细胞状态特异性转录因子网络和细胞谱系关系
失去细胞核的细胞在3D环境中举步维艰

【纳米】肿瘤组织特异性激活级联反应的聚合物囊泡纳米反应器
Angew封面:多肽修饰的铂纳米颗粒化身特异性肝癌杀手