科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-01-08
来源:BioArt
责编 | 兮
胚胎早期发育和干细胞多能性的维持需要细胞保持高水平的rRNA转录和核糖体生成活性,抑制细胞正常的rRNA转录和核糖体生成状态都会导致胚胎干细胞多能性的丧失【1-4】。因此,核仁中rDNA染色质的稳定对于胚胎干细胞多能性的建立和维持至关重要。胚胎干细胞rDNA保持低H3K27me3表观修饰,伴随分化过程中异染色质形成其水平升高。然而,仍然不清楚细胞是如何调控rDNA区域PRC2的活性及H3K27me3的表观修饰,以及这种调控和干细胞多能性的关系。RNA结合蛋白对PRC2活性的拮抗作用亦未见报道。
2020年1月7日,清华大学沈晓骅团队在Cell Reports杂志上发表文章DEAD-Box Helicase 18 Counteracts PRC2 to Safeguard ribosomal DNA in Pluripotency Regulation,发现了一个参与胚胎干细胞多能性维持和rDNA表观调控的RNA结合蛋白DDX18。

DDX18定位于核仁的外层区域,结合pre-rRNA及rDNA,并促进细胞rRNA的转录,核糖体合成及蛋白翻译,在早期胚胎发育和胚胎干细胞多能性维持中起到重要的作用。比较DDX18敲低,rRNA转录抑制和翻译抑制后转录组变化发现,DDX18通过促进rRNA转录维持干细胞多能性。胚胎干细胞维持高水平的DDX18表达和rRNA转录,而在分化过程中DDX18表达和rRNA转录显著降低,这不仅是分化的结果,也是干细胞多能性退出的原因。
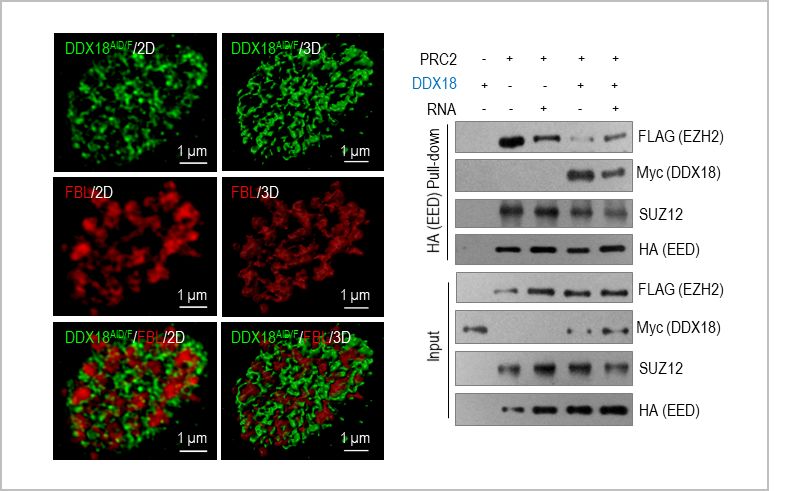
那么,机制上DDX18是如何调控rRNA转录的呢?通过分析DDX18的相互作用蛋白质组发现,DDX18可与PRC2相互作用。体内免疫共沉淀和体外蛋白pull-down实验验证了这种相互作用,并发现DDX18可单独,或与RNA一起破坏EZH2与PRC2其他组分的结合。DDX18敲低或蛋白快速降解均会导致核仁EZH2增多,引发rDNA位点PRC2的活性并起始H3K27甲基化,促使核仁异染色质形成。抑制PRC2活性可以部分拯救DDX18缺失导致的分子和细胞形态上的缺陷。
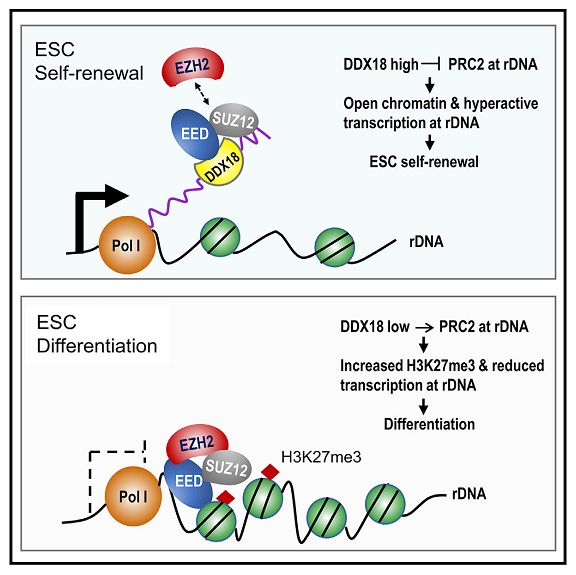
DDX18位于核仁的外层并破坏PRC2复合体形成
总之,此项研究提供了RNA结合蛋白DDX18结合pre-rRNA并定位于核仁外层,破坏PRC2复合物形成并拮抗其在rDNA区域H3K27甲基化的活性,促进rRNA转录并维持干细胞多能性这一完整的证据链。揭示了RNA结合蛋白拮抗PRC2并维持rDNA低H3K27甲基化的新机制。RNA结合蛋白不仅调控核糖体合成活性,而且表观控制基因表达和染色质结构,从而维持干细胞多能性。此项研究亦为PRC2/H3K27me3表观修饰的建立和维持机制提供了新的见解。
据悉,此项工作的第一作者为沈晓骅实验室的博士后张惠,博士生吴中洋和卢雨阳,通讯作者为沈晓骅博士和张惠博士。这一课题的胚胎实验得到了清华大学颉伟课题组和黄波博士的帮助。美国哥伦比亚大学王建龙课题组提供了有益的指导意见。
原文链接:
https://doi.org/10.1016/j.celrep.2019.12.021
制版人:珂
参考文献
1. Lin, C. J., Koh, F. M., Wong, P., Conti, M. & Ramalho-Santos, M. Hira-mediated H3.3 incorporation is required for DNA replication and ribosomal RNA transcription in the mouse zygote. Developmental cell 30, 268-279, doi:10.1016/j.devcel.2014.06.022 (2014).
2. Corsini, N. S. et al. Coordinated Control of mRNA and rRNA Processing Controls Embryonic Stem Cell Pluripotency and Differentiation. Cell stem cell 22, 543-558 e512, doi:10.1016/j.stem.2018.03.002 (2018).
3. Percharde, M. et al. A LINE1-Nucleolin Partnership Regulates Early Development and ESC Identity. Cell 174, 391-405 e319, doi:10.1016/j.cell.2018.05.043 (2018).
4. Bi, X. et al. RNA Targets Ribogenesis Factor WDR43 to Chromatin for Transcription and Pluripotency Control. Molecular cell 75, 102-116 doi:10.1016/j.molcel.2019.05.007 (2019).
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652479735&idx=3&sn=441da70d736142f3965c194135c8207f&chksm=84e23343b395ba55888f6fda6275314fabb8e85e0ff43b32fd7f47da4ffc65a0442caeb378c3&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

广州生物院揭示体细胞多能性调控新机制
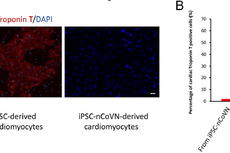
中国学者发现新冠病毒致病新机制:破坏诱导多能干细胞的多能性并将其转变为成纤维细胞

灵长类早期胚胎发育多能性变化模式揭示

DNA机器人一小步 癌症治疗一大步
演化:“最奇怪动物”身份揭秘
合成生物学: 一个用来控制转基因生物的内置毁灭开关

基于DNA聚合反应,能维持胚胎干细胞多能性

猪多能性干细胞最新进展与展望

利用人多能性干细胞产生脊髓神经干细胞

张毅团队再取新突破,发现全能型向多能性细胞转变的机制