科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-08-23
世界卫生组织国际癌症研究机构(IARC)今年发布的全球最新癌症负担数据显示,2020年我国新增结直肠癌(CRC)患者约56万例,死亡约29万例[1]。一直以来,手术是治疗CRC的主要手段,尽管化疗和靶向治疗不断发展,但晚期CRC预后仍然不佳。根据美国国立卫生研究院(NIH)最新统计数据显示,晚期CRC患者的5年生存率仅为15%[2],患者亟待更有效的创新治疗方案。
在结直肠癌患者中,有10%-15%表现为微卫星高度不稳定(MSI-H)或者DNA错配修复功能存在缺陷(dMMR)。 微卫星不稳定性(MSI)是导致CRC发生的重要分子途径之一,具有MSI-H/ dMMR表型的早期CRC预后较好,而在晚期CRC中,MSI-H/dMMR则被认为是不良预后因素[3]。
随着免疫治疗时代的到来和对肿瘤微环境探索的不断深入,研究发现MSI-H/dMMR CRC患者的肿瘤突变负荷(TMB)升高,导致肿瘤浸润淋巴细胞升高,肿瘤微环境中PD-L1表达上调,提示免疫检查点抑制剂有治疗MSI-H/dMMR CRC的潜力[4]。
2021年美国肿瘤学会(ASCO)大会上公布的KEYNOTE-177研究的最终总生存(OS)分析结果显示,PD-1抑制剂帕博利珠单抗(国内俗称“K药”)一线治疗MSI-H/dMMR转移性结直肠癌3年OS率达到61%(vs.对照组50%),显示出具有临床意义的OS获益趋势[5]。
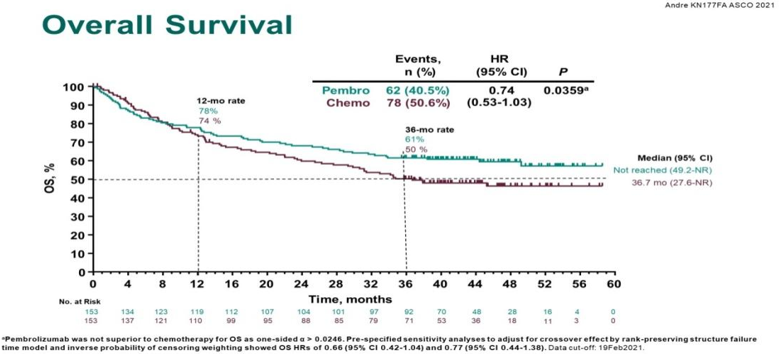
图1. KEYNOTE-177研究的最终OS分析结果
值得注意的是,OS曲线在36个月之后趋于平缓,提示这部分存活患者将很有希望获得长期生存,甚至临床治愈。
基于KEYNOTE-177研究结果,美国和欧盟先后于2020年和2021年批准帕博利珠单抗单药一线治疗不可切除或转移性MSI-H/dMMR CRC,中国国家药品监督管理局(NMPA)也于2021年6月批准该适应证。
免疫治疗一线可以给晚期MSI-H/dMMR CRC患者带来显著获益,那么免疫治疗能否应用于局部晚期甚至更早期患者的治疗呢?
在KEYNOTE-177研究中,K药单药一线治疗的客观缓解率(ORR)达45.1%, 显著高于研究者选择治疗组的33.1%,而且13.1%的人群获得完全缓解(CR),是对照组的3.3倍。K药单药治疗能获得如此高的ORR/CR比例,不得不让结直肠癌外科医生“刮目相看”,甚至“跃跃欲试”。
事实上,中国研究者在CRC免疫新辅助治疗上已经做了很多尝试,初步结果令人鼓舞。来自中山大学附属肿瘤防治中心的一项回顾性研究分析显示,8例局部晚期和IV期MSI-H/dMMR CRC(2例RAS突变阳性)患者应用PD-1单药,或者PD-1联合化疗或CTLA-4单抗新辅助治疗后,1例患者获得影像学CR, 5例获得部分缓解(PR), 2例疾病稳定(SD); 所有PR+SD患者经手术后获得主要病理缓解(MPR), 5例获得病理完全缓解(pCR)。仅有1例患者出现3级免疫治疗相关不良反应[6]。
免疫治疗是否有可能改变早期和局部晚期CRC临床实践?当前MSI-H/dMMR检测的临床应用现状如何?未来应该如何做到“应检尽检”?带着这些问题,借“2021肿瘤免疫治疗新纪元论坛”的机会,记者采访了中国医学科学院肿瘤医院结直肠外科主任王锡山教授。
专家简介

王锡山 教授
主任医师、博士生导师
中国医学科学院肿瘤医院 结直肠外科 主任
中国医师协会结直肠肿瘤专业委员会 主任委员
中国抗癌协会大肠癌专业委员会 主任委员
中国抗癌协会大肠癌专业委员会青年委员会 主任委员
《中华结直肠疾病电子杂志》主编
国际NOSES联盟 主席
中国NOSES联盟 主席
中国医师协会第四届理事会 常务理事
中国医师协会结直肠肿瘤专业委员会NOSES专委会 主任委员
中国医师协会外科医师分会MDT专业委员会 副主任委员
中国抗癌协会整合肿瘤学分会 副主任委员
中国医师协会外科医师分会 常委
中华医学会肿瘤学分会结直肠肿瘤学组 副组长
免疫治疗将改变早、中期MSI-H/dMMR CRC治疗格局
王锡山教授:MSI-H/dMMR型CRC发生率随分期升高而降低。我国I-II期CRC患者中, 约有15%为MSI-H/dMMR,而III-IV期患者中,这一比例约为7.7%。如果将免疫治疗前移,应用于更早阶段MSI-H/dMMR CRC的治疗中,是否可以使肿瘤负荷较大的患者实现降期;或者应用于CRC的新辅助治疗中,能否提升整体CRC的治疗效果,提高手术切除率,降低局部复发率,加强脏器功能保护?
在KEYNOTE-177研究中,K药一线治疗KRAS、NRAS和BRAF基因均为野生型的MSI-H/dMMR CRC患者, ORR接近60%,CR率更是达到18%。
对于肿瘤患者来说,获得CR意味着体内可见病灶完全消失,无需手术治疗,可以采用等待观察(W&W)策略。K药单药治疗能达到如此高的CR,这或许将彻底改变结直肠癌的新辅助治疗格局和治疗理念。
而且免疫治疗带来的CR率可能还会更高。由于KEYNOTE-177采用RECIST(v1.1)标准评估肿瘤治疗疗效,RECIST标准追求的是肿瘤的缩小,而免疫治疗可能产生假性进展,由此推断可能一些评估为部分缓解(PR)的患者实际上已获得了CR。在临床实践中不乏影像学检查为PR的患者在术后发现实际上是pCR(病理完全缓解)。
KEYNOTE-177的结果无疑增强了我们将免疫治疗用于更早阶段CRC的信心,期待未来有更多高级别的免疫新辅助治疗的循证医学证据,为临床实践提供更可靠的依据。
应当提高CRC患者MSI/MMR状态的检测率
王锡山教授:MSI-H/dMMR是目前公认的指导免疫治疗的生物标志物之一。在临床实践中,可以对有条件的CRC患者开展相关检测,对于MSI-H/dMMR的患者,可以选择通过K药治疗来争取最大可能的长期生存甚至治愈。而且通过免疫治疗,这部分患者或许可以免于手术、化疗等治疗带来的痛苦。
MSI状态对于不同分期的CRC患者均有明确的指导意义。另外在中国CRC患者中,右半结肠癌MSI-H/dMMR发生率为20.5%,左半结肠癌这一比例为9.2%,直肠癌则为5.1%[7]。当前仍有医生认为只需要对右半结肠癌进行MSI/MMR检测,但是这组数据告诉我们,对于左半结肠癌和直肠癌,我们也要检测MSI/MMR。
未来要实现MSI/MMR“应检尽检”,需要分几个步骤:首先,可以从卫生经济学角度对MSI/MMR检测及免疫治疗进行宏观评价,让社会了解这一情况;其次,让患者知晓该检测的意义,进而选择是否进行检测;第三,在获得更多的数据后,由CRC专业委员会制定指南,将MSI/MMR列入必检项目。相信随着MSI-H/dMMR检测率的提高,我国CRC诊疗水平将会得到进一步提升。
参考文献:
[1] GLOBOCAN 2020. https://gco.iarc.fr/
[2] SEER Explorer. https://seer.cancer.gov/explorer/
[3] Fabio Gelsomino,et al. Cancer Treat Rev. 2016;51:19-26.
[4] Narayanan S, et al. Sci Rep. 2019; 9(1):13455.
[5] André T, et al. Presented at ASCO 2021
[6] Ding-Xin Liu ,et al. OncoImmunology. 2020;9(1):1711650.
[7] Raut CP, et al. Mutat Res. 2004 Dec 21;568(2):275-82.

来源:gh_03316850f273 中国抗癌协会大肠癌专业委员会
原文链接:http://mp.weixin.qq.com/s?__biz=MzIyMzQyNDczNg==&mid=2247486563&idx=1&sn=95081e9b861e0452a15058491330c942
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn