科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-01-17
来源:iNature
iNature
铁死亡是一种铁依赖性形式的调节性细胞死亡,它由过度的脂质过氧化作用诱导,在形态学和机制上均不同于凋亡。目前的研究表明,铁死亡主要是由含有多不饱和脂肪酸(PUFA,最明显的是花生四烯酸)磷脂(PLs)的过氧化引起的。放射疗法是许多癌症治疗的基石,但放射抵抗仍然是导致放射疗法失败的主要因素。放射疗法使用高能电离辐射(IR)产生DNA双链断裂,从而诱导细胞周期停滞,衰老和各种细胞死亡模式,包括细胞凋亡,坏死,自噬和有丝分裂灾难。除了直接破坏DNA外 ,IR可以诱导间接的细胞作用。
2020年1月16日,中南大学王晖及德克萨斯大学安德森癌症中心Gan Boyi共同通讯在Cell Research 在线发表题为“The role of ferroptosis in ionizing radiation-induced cell death and tumor suppression”的研究论文,该研究发现电离辐射(IR)诱导癌细胞中的铁死亡。从机制上讲,IR不仅诱导活性氧(ROS),而且诱导ACSL4的表达,ACSL4是铁死亡的必需脂质代谢酶,导致脂质过氧化和铁死亡的升高。ACSL4缺失可在很大程度上消除IR引起的铁死亡并增强放射抵抗力。
总而言之,该研究揭示了IR和铁死亡之间的先前未知的联系,并表明有必要进一步探索放射治疗和FINs在癌症治疗中的结合。

调节细胞死亡,最明显的是细胞凋亡,是肿瘤发展的天然障碍。对细胞死亡的抗性是癌症的标志。在肿瘤发展过程中或在存在癌症疗法的情况下,应激刺激可诱导凋亡。虽然凋亡明显由许多癌症疗法诱导并参与其中,无论是否以及如何癌症疗法诱导其他形式的调节性细胞死亡尚不清楚。
铁死亡是一种铁依赖性形式的调节性细胞死亡,它由过度的脂质过氧化作用诱导,在形态学和机制上均不同于凋亡。目前的研究表明,铁死亡主要是由含有多不饱和脂肪酸(PUFA,最明显的是花生四烯酸)磷脂(PLs)的过氧化引起的。相应地,可以通过失活ACSL4(长链脂肪酸辅酶A连接酶,PUFA-PL生物合成所需的酶,并优先利用花生四烯酸作为其底物,来显著减轻铁死亡。GPX4,谷胱甘肽过氧化物酶利用还原型谷胱甘肽将脂质氢过氧化物转化为脂质醇,从而减轻脂质过氧化作用并抑制铁死亡。谷胱甘肽是由甘氨酸,谷氨酸和半胱氨酸合成的,其中半胱氨酸是限速前体。
大多数细胞通过氨基酸转运蛋白SLC7A11(也称为xCT)导入胞外cystine(半胱氨酸的一种氧化的二聚体形式)而获得半胱氨酸。相应地,通过遗传或药理学方法灭活了GPX4或SLC7A的研究已经确定了几类有效抑制SLC7A11或GPX4的铁死亡诱导物(FINs)。例如,第1类FINs(例如erastin和柳氮磺吡啶)抑制SLC7A11介导的胱氨酸转运,第2类FIN(例如RSL3和ML162)通过抑制GPX4活性发挥作用,而第3类FIN(例如FIN56)通过消耗GPX4蛋白和辅酶Q10来诱导铁死亡。这些FIN不仅为铁死亡研究提供了重要工具,也是治疗由铁死亡引起的疾病的潜在治疗剂。
像其他形式的受调节的细胞死亡一样,铁死亡在正常细胞中受到严格的调节,其失调与多种病理状况和疾病有关。例如,过度的铁死亡与缺血再灌注损伤,肾衰竭和神经退行性疾病有关,而铁死亡不足则可导致癌症。先前得研究表明,将铁死亡确定为一种天然的肿瘤抑制机制,并发现灭活了铁死亡,有助于肿瘤的发展。
放射疗法是许多癌症治疗的基石,但放射抵抗仍然是导致放射疗法失败的主要因素。放射疗法使用高能电离辐射(IR)产生DNA双链断裂,从而诱导细胞周期停滞,衰老和各种细胞死亡模式,包括细胞凋亡,坏死,自噬和有丝分裂灾难。除了直接破坏DNA外 ,IR可以诱导间接的细胞作用。例如,电离辐射(IR)通过细胞水的辐射分解和氧化酶的刺激而产生细胞损伤,从而产生诸如羟基和过氧化氢之类的活性氧(ROS),这可能会损坏核酸,蛋白质和脂质。
该研究显示了电离辐射(IR)诱导癌细胞中的铁死亡。从机制上讲,IR不仅诱导活性氧(ROS),而且诱导ACSL4的表达,ACSL4是铁死亡的必需脂质代谢酶,导致脂质过氧化和铁死亡的升高。ACSL4缺失可在很大程度上消除IR引起的铁死亡并增强放射抵抗力。
电离辐射(IR)还诱导了包括SLC7A11和GPX4在内的铁死亡抑制剂的表达,作为适应性反应。IR或KEAP1缺乏症诱导的SLC7A11表达通过抑制铁死亡而促进了放射抵抗。用铁死亡诱导剂(FINs)灭活SLC7A11或GPX4可使抗辐射的癌细胞和异种移植肿瘤对IR敏感。此外,放疗在癌症患者中诱发铁死亡,而铁死亡与癌症患者对放疗的较好反应和更长生存期相关。该研究揭示了IR和铁死亡之间的先前未知的联系,并表明有必要进一步探索放射治疗和FINs在癌症治疗中的结合。
参考消息:
https://www.nature.com/articles/s41422-019-0263-3
来源:Plant_ihuman iNature
原文链接:https://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247506824&idx=6&sn=cd2c7f00c26c4dbf325009710885067d&chksm=fce6a857cb912141e71b7a0f379dc992e795ecfddb41c5264c96e9b0405cc62fc97ede78c538#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

科学家发现阻止癌细胞消耗葡萄糖的新方法
癌症演化树:揭示癌症转移机制



生态环境部发布国家放射性污染防治标准《电离辐射监测质量保证通用要求》的公告
在细胞病变最早期剥开癌细胞“画皮”
科学家新发现:癌细胞的另类杀手——合成非免疫细胞

这种糖竟能抑制癌细胞生长,科学家发现癌细胞致命弱点
癌细胞的自我介绍
近代物理所发现电离辐射引起核内染色质结构调控证据
癌细胞太狡猾?这一次,科学家决定主动出击!
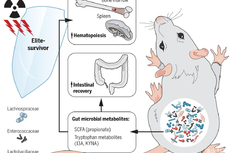
郭浩等揭示肠道微生物菌群和代谢产物在电离辐射模型中的保护作用