科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-03-20
来源:中科院再生医学
脊髓损伤会导致损伤平面以下感觉和运动功能的障碍,为家庭和社会带来沉重负担,一直以来脊髓再生修复是世界性的医学难题。研究表明,脊髓损伤后,损伤部位会形成不利于神经再生的抑制性微环境,不仅抑制神经元轴突的生长及神经前体细胞向神经元分化,而且形成致密的瘢痕组织会阻止功能细胞向损伤区迁移。如何利用功能生物材料重塑脊髓再生微环境是领域内研究热点。N-cadherin是一种在中枢神经系统中高表达的跨膜糖蛋白,通过其胞外串联重复序列之间的嗜同性结合介导了细胞与细胞之间的黏附。在神经前体细胞中,N-cadherin胞内部分与多种蛋白形成蛋白复合体,可以将胞外的机械力传导到胞内并将其转化为细胞的迁移信号,驱动细胞骨架F-actin运动。同时,N-cadherin保持激活态可以激活β-catenin降解复合体,从而下调胞质中β-catenin的水平,促进神经干细胞向神经元分化。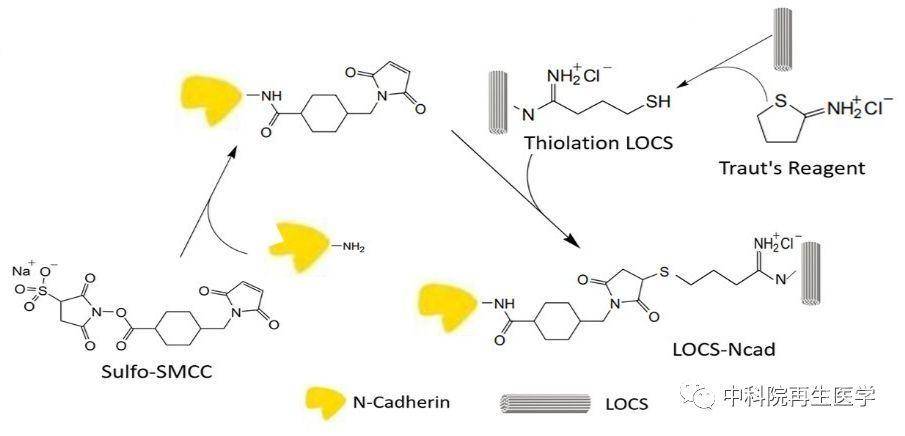
来源:dailab2003 中科院再生医学
原文链接:https://mp.weixin.qq.com/s?__biz=MzA4MjUwMTM4NA==&mid=2675604322&idx=1&sn=296f38313e928ede62ab9f4f16c01966&chksm=850a1105b27d9813f097113f60ff3c1650398c47c83fdbec73c23ce10946e32567bd8675fc0c#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
“脊髓损伤国际行动项目”启动会于2015年2月19-27日在瑞士举行
脑损伤激活胶质细胞产生神经元研究获进展
揭秘癌细胞与神经元的“共生共舞”

Cell:星形胶质细胞保护神经元免受毒素累积
小胶质细胞监测和保护神经元的功能

《Cell》神经元诱导干细胞重生

人类大脑有多少个神经元细胞

金纳米粒子保护神经元免于细胞死亡
陈荣清/彭碧文/王云/朱沛旻 共同主持专刊 | 非神经元细胞对神经元的调节
星形胶质细胞首次转为功能性神经元