科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-04-20
来源:学术经纬

▎药明康德内容团队编辑
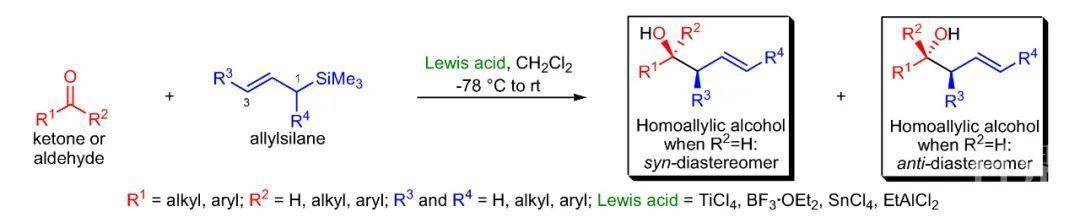
▲Sakurai烯丙基化反应(图片来源:参考资料[1])
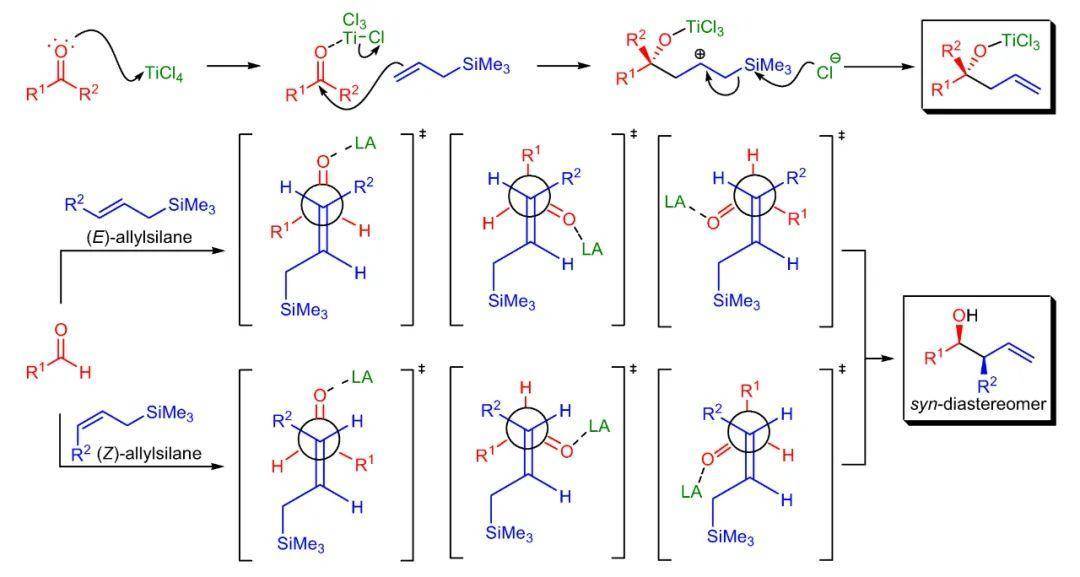
▲Sakurai烯丙基化反应的机理(图片来源:参考资料[1])
往期回顾
Stork烯胺反应
Stobbe缩合
Stevens重排
Stetter反应
题图来源:Pixabay
参考资料
[1] László Kürti, Barbara Czakó. Strategic applications of named reactions in organic synthesis [M]: Elsevier, 2005来源:global_academia 学术经纬
原文链接:http://mp.weixin.qq.com/s?__biz=MzI5MDQzNjY2OA==&mid=2247498411&idx=2&sn=5359a8dd5141de9e3d72b0d743f3e784&chksm=ec1d59f8db6ad0eea648d70f0d4be8e3b857d6dee8e7efc6d93025af39a0ba397046e290ccff&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
N-烯丙基甲胺

手性磷酸双功能催化:基于α-烯基取代烯丙基硼酸酯的不对称烯丙基化
烯丙基三苯基溴化膦
Keck自由基烯丙基反应
聚(烯丙基胺)

Science:由腈一锅合成手性伯胺,关键是——做点“无用功”
氯甲酸烯丙基酯
烯丙基丁基醚

Angew:Rh催化β,γ-不饱和-α-氨基腈的不对称烯丙基烷基化反应
烯丙基三甲氧基硅烷