科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-05-06
来源:iNature
血管健康与人类健康息息相关,俗话说:“血管有多老,人就有多老”,说的就是血管的健康关乎寿命长短。血管是输送血液的通道,分为动脉和静脉等。动脉将心脏泵出的血液输送至全身各个器官,在器官稳态维持中发挥重要作用。血管老化导致血管弹性下降,脂质异常沉积,从而形成斑块,最终导致动脉粥样硬化、冠心病、脑梗等衰老相关疾病。由于不同来源的血管壁细胞存在高度异质性,目前尚不明确人类老年血管的细胞组成和分子特征,这在一定程度上限制了人们对血管衰老机制的深入理解,并制约了心血管疾病的预防和治疗。

2020年5月5日,中国科学院动物研究所曲静研究组、刘光慧研究组与北京大学汤富酬研究组合作在Nature Communications 杂志在线发表题为“A single-cell transcriptomic landscape of primate arterial aging”的研究论文。该研究首次绘制了非灵长类食蟹猴动脉血管衰老的单细胞基因表达图谱,进而揭示长寿基因FOXO3A的表达下调是血管衰老的驱动因素。
主动脉弓和冠状动脉是血管动脉粥样硬化的易感部位。研究人员利用单细胞转录组测序技术绘制了主动脉弓及冠状动脉的内皮细胞、平滑肌细胞和成纤维细胞等血管细胞类型的基因表达图谱,并鉴定出8种区分主动脉和冠状动脉的新型分子标志物。衰老伴随的差异基因表达网络分析显示,转录因子FOXO3A(长寿基因FOXO3A编码的蛋白产物)是调控动脉血管差异表达基因网络的关键分子节点。FOXO3A在六种衰老的血管壁细胞中表达均下调,是灵长类动脉血管衰老的重要特征。
进一步的研究证实了FOXO3A对于维持灵长类动脉稳态的关键作用。通过结合胚胎干细胞基因编辑和定向诱导分化技术,研究人员获得了靶向敲除FOXO3A基因的人类血管内皮细胞。与野生型细胞相比,FOXO3A缺失的血管内皮细胞表现出增殖、迁移和成管等能力的退化。在被移植到小鼠的缺血后肢中后,FOXO3A缺失的内皮细胞的血管修复能力较野生型细胞也显著降低。

该项研究首次实现了灵长类血管衰老单细胞图谱的绘制,不仅有助于深入理解血管衰老过程中细胞组成和分子特征的变化规律,而且揭示了长寿基因FOXO3A表达水平的沉默是驱动灵长类动脉血管衰老的关键因素。这些发现为人类血管衰老及相关疾病的干预奠定了重要的理论基础。
中国科学院北京基因组研究所张维绮研究员、北京大学博士研究生张书、中国科学院动物研究所博士研究生颜鹏泽和北京大学博士研究生任杰为文章并列第一作者。中国科学院动物研究所曲静研究员、北京大学汤富酬教授和中国科学院动物研究所刘光慧研究员为共同通讯作者。
来源:Plant_ihuman iNature
原文链接:https://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247508639&idx=6&sn=e3d08e7137216b9a6837db1c9f5c0a0f&chksm=fce6d140cb91585698239221b18d2c9029b31468a374eec244a1e8e2edbf6e93ffa84a7f19fc#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

3D生物打印血管动物试验成功

曲静/汤富酬/刘光慧/王思合作揭示灵长类视网膜衰老机制
中国微循环学会周围血管疾病专业委员会成功召开2015学术年会暨第二届朝阳血管医学论坛

中国微循环学会休克专业委员会成功召开2015年全国休克、微循环及其相关血管病学术会议
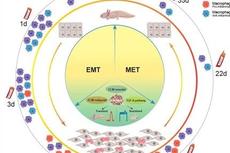
徐讯/顾颖/刘光慧合作绘制蝾螈肢体再生的动态细胞及分子图谱

【喜报】2020年度北京市科学技术奖揭晓,邵峰、刘光慧获奖!

刘光慧:让干细胞逆龄重生的“魔法师”
澳门国际论坛暨澳门卫生局医生协会2015学术年会
首届亚太血管学术联盟深圳会议暨第三届深港澳血管论坛(SVF2016)会议通知

这不是养生,是找病!这些“土味”养生法,千万别再做了