科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-06-07
来源:BioArt
撰文 | Katherina
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652487305&idx=3&sn=602a3f4394e4631416616695589960ca&chksm=84e22d3db395a42bc414cdebfcd01c44338f38621c0b4a1fcc17e224ed073d010a1cf74e38f8#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
气候变化将带七种惊人影响,人类性生活或减少



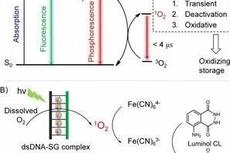
氧化还原媒介助力活性氧-Luminol化学发光传感分析
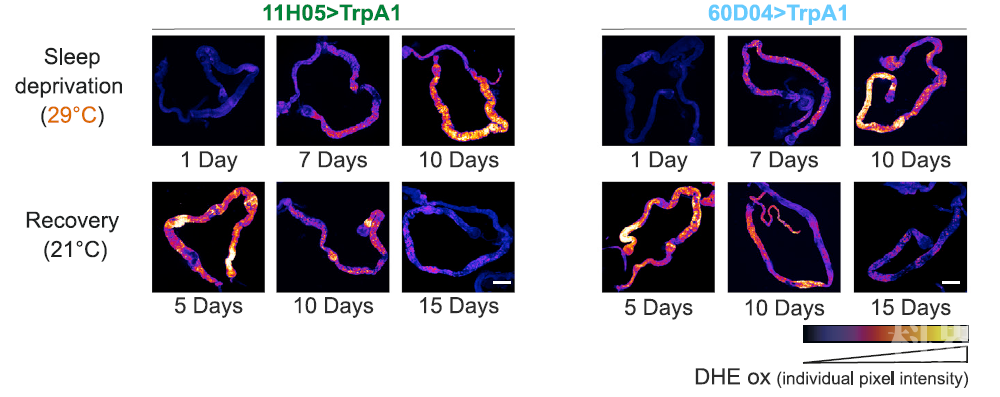
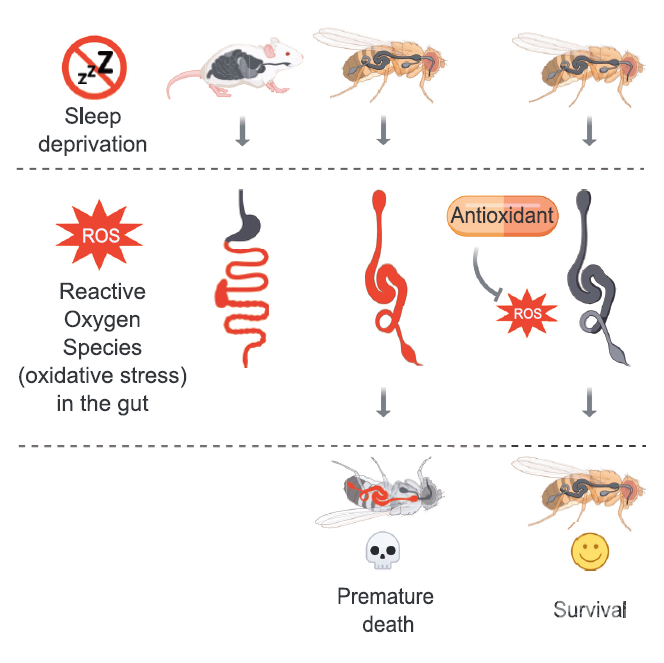
睡眠不足会由于肠道内活性氧的积累而导致死亡
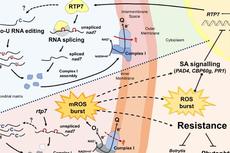
我国科学家找到线粒体活性氧调控植物免疫的分子机制

《细胞》:如果长期睡眠不足肠道中也会产生大量有害的活性氧
雪上加霜!熬夜加班身体被掏空,结果却胖了!
心理学:幼儿使用触屏与睡眠较少有关

睡眠好不好,通过手机软件就能得出结果吗?
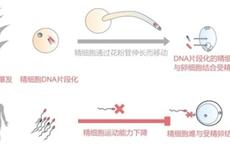
研究揭示活性氧是单倍体诱导的核心因子
中国睡眠研究会第五届五次常务理事会在京召开


