科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-06-29
来源:BioArt
以美拉德反应(the Maillard reaction)(蒋华良:红烧肉中的美拉德反应)为代表的“糖化”(Glycation)作用具有悠久的研究历史,尤其在食品化学中具有重要科学意义【1】。糖类是生命体最为重要的营养和供能物质之一,在细胞内外也均有还原性糖的存在,能够与生物大分子中的亲核基团发生糖化反应。在生理和病理条件下,糖化反应发生的速度虽然相对缓慢,但却是糖尿病和衰老过程的重要生物标记物(例如糖尿病病人的HbA1c测试)。
近年来,生物大分子糖化后修饰的生物学作用开始被逐步揭示,例如NRF2-KEAP1通路中的糖化修饰对于肿瘤的发生发展具有“双刃剑”的作用【2, 3】(BioArt: Cell亮点| “糖化”而非“糖基化”修饰—控制肿瘤生长的“红绿灯”)。与其他胞内蛋白相比,组蛋白具有更长的半衰期和较多的糖化修饰反应位点(赖氨酸和精氨酸),理应是细胞中糖化反应最重要的靶点之一。但是实际上组蛋白的糖化翻译后修饰近年来才开始被系统性地研究和报道【4, 5】,由于没有表观遗传学书写器蛋白(writer enzyme)的限制,这样的“非酶促”翻译后修饰反应主要依赖于细胞微环境中小分子的浓度和浓度持续的时间【6, 7】。由于生物大分子糖化产物化学结构的多样性和复杂性以及该反应自身的高度动态性,对于生物体内自发糖化反应的研究具有较大的挑战。
美国纽约纪念斯隆凯特琳癌症中心的Yael David课题组的郑庆飞博士在组蛋白糖化修饰领域做出了一系列的原创性贡献,他与合作者开发了一系列用于检测和表征组蛋白糖化的化学生物学工具【8, 9】,并发现了组蛋白糖化对于真核细胞染色质结构和功能的影响及其在乳腺癌中的表观遗传学作用(郑庆飞博士等揭示组蛋白糖化翻译后修饰对于染色质结构的影响及其在疾病中潜在的调控作用)【5】。基于前期的研究,以还原性单糖甲基乙二醛(MGO)诱导的组蛋白糖化反应为模型,David课题组提出了组蛋白糖化后修饰对于染色质结构影响的“双阶段模型”(图1),用以解释糖化反应对于癌细胞生长的“双刃剑”作用【5, 7】。
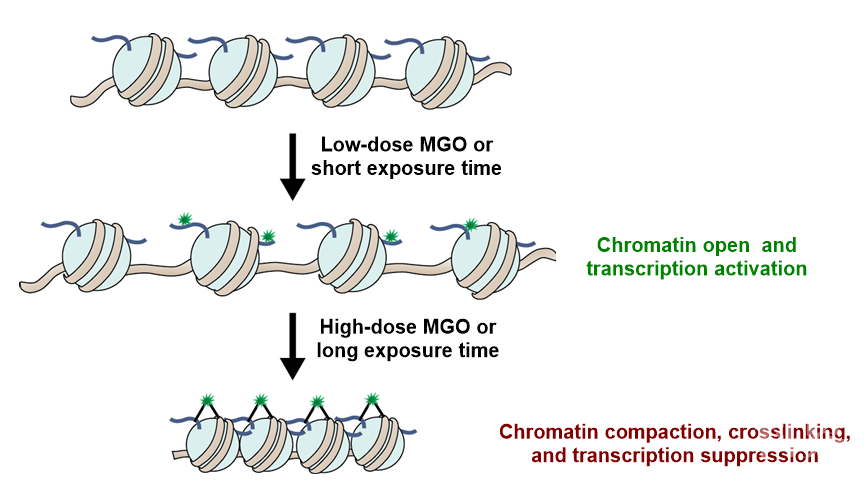
为了维持对于自身恶性增殖有利的“糖化第一阶段”而不进入可能导致凋亡的“糖化第二阶段”,癌细胞进化出了一系列控制糖化程度的调控和保护机制,其中包括David课题组前期报道的组蛋白去糖化酶DJ-1【5】。那么除了DJ-1之外,是否还存在其他能够直接作用于糖化组蛋白的调控酶呢?2020年6月26日,纪念斯隆凯特琳癌症中心Yael David课题组的郑庆飞博士等在Nature Communications杂志上发表了题为Protein arginine deiminase 4 antagonizes methylglyoxal-induced histone glycation的研究论文,首次报道了肽酰基精氨酸脱亚氨酶4(PAD4)在组蛋白糖化表观遗传学调控过程中的新功能【10】。

在本研究中,作者通过综合使用化学生物学,生物物理学和细胞生物学等研究手段,证明了PAD4在控制组蛋白糖化修饰过程中的“双重作用”(图2)。PAD4能够识别组蛋白H3和H4的N端大部分精氨酸作为底物并将之转化为在生理条件下无法进一步与MGO反应的瓜氨酸(瓜氨酸结构稳定,不参与绝大多数翻译后修饰反应),由此起到第一重“保护”作用;同时作者使用不同种类的底物,通过一系列体外(in vitro)和体内(in vivo)实验证明了PAD4能够将几种糖化后的精氨酸(包括早期产物Aminocarbinol和晚期的CEA)直接转化为瓜氨酸,由此实现了其第二重“逆转-改写”作用。基于PAD4酶促反应的独特性[有别于传统的“擦除器蛋白”(eraser enzyme)],作者将这样一类调控蛋白命名为表观遗传学“涂改器蛋白”(rewriter enzyme),即将一种翻译后修饰转化为另一种翻译后修饰类型。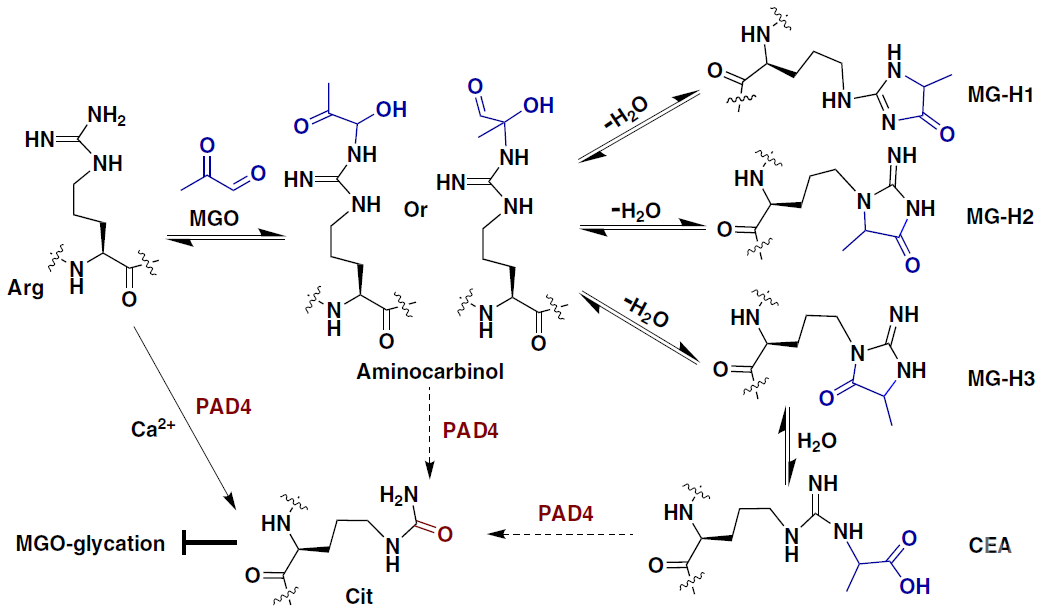
图2. PAD4在调控组蛋白MGO糖化过程中的“双重作用”
最后,通过对于临床肿瘤样本的分析,作者发现PAD4蛋白在乳腺癌细胞中过量表达,进一步印证了其在肿瘤发生发展中的“控组蛋白糖化”作用。结合此前报道过的PAD4对于组蛋白精氨酸甲基化的调控作用【11, 12】,作者进一步给出了组蛋白(H3和H4)中精氨酸的甲基化、瓜氨酸化和糖化三中翻译后修饰的相互作用网络(图3)。
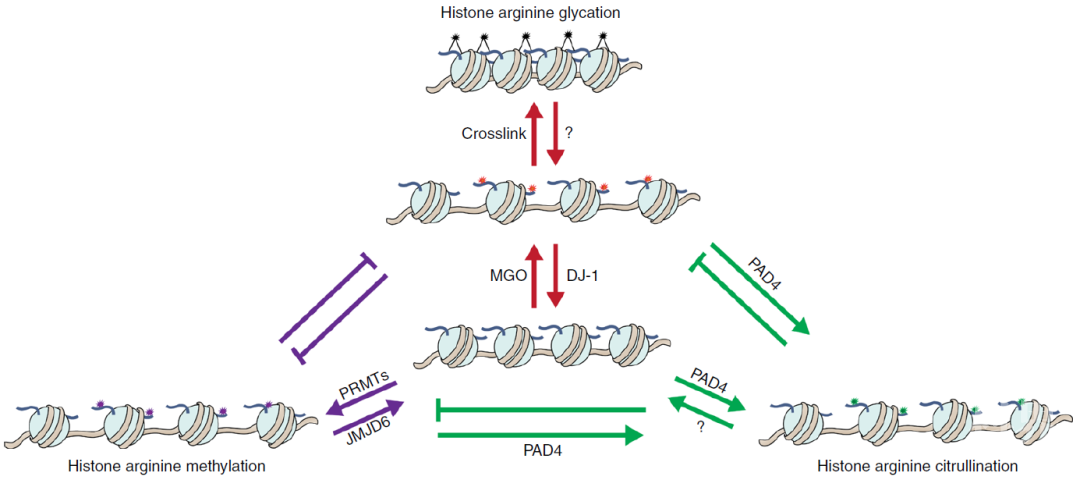
总之,本研究系统性地阐释了PAD4这一古老蛋白在真核细胞组蛋白糖化修饰调控过程中的全新表观遗传学功能,填补了癌细胞自身组蛋白糖化调控网络拼图中缺失的一部分,不仅为糖生物学和癌症表观遗传学的研究提供了新思路,也为未来的临床抗癌治疗提供了一个新的潜在靶点。
参考文献
1. Hellwig M, Henle T. Baking, ageing, diabetes: a short history of the Maillard reaction. Angew Chem. Int. Ed. Engl., 2014, 53, 10316-10329.
2. Bollong MJ, et al. Ametabolite-derived protein modification integrates glycolysis with KEAP1-NRF2 signalling. Nature, 2018, 562, 600-604.
3. Sanghvi VR, et al. The oncogenic action of NRF2 depends on de-glycation by fructosamine-3-kinase. Cell, 2019, 178, 807-819.
4. Galligan JJ, et al. Methylglyoxal-derived posttranslational arginine modifications are abundant histone marks. Proc. Natl. Acad. Sci. USA., 2018, 115, 9228-9233.
5. Zheng Q, et al. Reversible histone glycation is associated with disease-related changes in chromatin architecture.Nat. Commun., 2019, 10, 1289.
6. Zheng Q, et al. (De)Toxifying the epigenetic code. Chem. Res. Toxicol., 2019, 32, 796-807.
7. Zheng Q, et al. Non-enzymatic covalent modifications: a new link between metabolism and epigenetics. Protein Cell, 2020, 11:401-416.
8. Zheng Q, et al. Synthesis of an alkynyl methylglyoxal probe to investigate nonenzymatic histone glycation. J. Org. Chem., 2020, 85, 1691-1697.
9. Maksimovic I, Zheng Q, et al. An azidoribose probe to track ketoamine adducts in histone ribose glycation. J. Am. Chem. Soc., 2020, 142, 9999-10007.
10. Zheng Q, et al. Protein arginine deiminase 4 antagonizes methylglyoxal-induced histone glycation. Nat. Commun., 2019, DOI: 10.1038/s41467-020-17066-y.
11. Cuthbert GL, et al. Histone deimination antagonizes arginine methylation. Cell, 2004, 118, 545-553.
12. Wang Y, et al. Human PAD4 regulates histone arginine methylation levels via demethylimination. Science 2004, 306, 279-283.
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652489228&idx=5&sn=2cca1ecaaf3702c5830d2b5420a1b6d1&chksm=84e255b8b395dcae91a0c6eed221485c496084ee2a63714129ceb03fc5f44f7b4d4ab7ce9eee#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
PNAS | 复旦大学研究揭示植物组蛋白分子伴侣识别组蛋白的结构基础
杭州又一区、县(市)“科普中国”科普员注册人数 突破5000

一味药用的好,一张方子就灵了
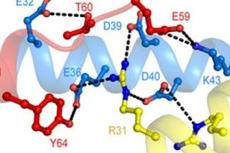
【前沿进展】复旦大学董爱武团队与麻锦彪团队合作揭示植物组蛋白分子伴侣识别组蛋白的结构基础
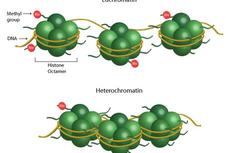
遗传发育所发表“组蛋白甲基化修饰在表观遗传调控和温度响应中的作用”综述文章
蛋白质设施用户揭示植物组蛋白分子伴侣识别组蛋白的结构基础

73岁院士接种新冠重组蛋白疫苗

植物何时发芽开花由组蛋白因子“操控”

研究揭示组蛋白巴豆酰化在人类胚胎干细胞分化中的关键作用
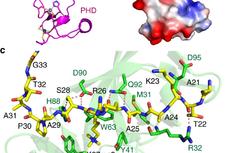
研究揭示SHL蛋白对抑制和活性组蛋白修饰的识别机制