科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-02-15
2月6日,国际学术期刊《美国国家科学院院刊》(PNAS)在线发表了中国科学院上海巴斯德研究所江陆斌课题组题为DNA helicase RecQ1 regulates mutually exclusive expression of virulence genes in Plasmodium falciparum via heterochromatin alteration 的最新研究成果。
疟疾是一类严重威胁人类健康的寄生虫病。致病性最强的恶性疟原虫每年在全世界范围内造成数以亿计的临床感染病例,并导致近50万人死亡。恶性疟原虫独特的var基因家族(约60个基因组成)编码的变异抗原PfEMP1是恶性疟原虫在病人体内实现免疫逃逸的关键因子。在感染红细胞过程中,单个恶性疟原虫在特定时间内只能表达某一个var基因,恶性疟原虫利用这种相互排斥性表达策略来逃避人体对PfEMP1抗原的免疫反应。阐明var基因家族的表达调控机制有望为疟疾疫苗和抗疟药的研发提供新的靶点,因此,这方面研究一直是该领域的国际前沿与热点。
江陆斌团队曾先后证明组蛋白甲基化酶PfSET2(Nature,2013)与一类长链非编码RNA(Front Microbiol,2018)分别参与调节了var基因的沉默和激活。但由于传统的恶性疟原虫基因编辑技术周期长、效率低,直接阻碍了研究人员对整个var基因调控网络的解析,因此其他相关调控因子目前仍不清楚。江陆斌团队利用自主研发的基于CRISPR/dCas9系统的、高效的恶性疟原虫表观遗传基因编辑技术(PNAS,2018),在该研究中证实DNA解旋酶PfRecQ1是维持var基因家族相互排斥性表达的关键因子。研究人员在恶性疟原虫中敲除PfRecQ1后,整个var基因家族处于沉默状态;而在敲除株中回复表达PfRecQ1后,又恢复了var基因相互排斥性表达的表型。进一步的研究表明,PfRecQ1控制了var基因转录起始位点附近组蛋白H3K9me3修饰,并且通过调节var基因在细胞核内周上的定位调控var基因的表达。这一研究成果为深入理解恶性疟原虫免疫逃逸的分子机理提供了新的线索,并为新型抗疟药的研发提供了一个全新的潜在靶点。
中国科学院大学硕士研究生李舟,博士研究生尹世刚、孙茂新(上海科技大学)、程秀为论文并列第一作者,江陆斌及其团队的副研究员戴雪瑜和博士研究生黄正辉为论文的共同通讯作者。该研究得到科技部国家重点研发计划、国家科技重大专项、国家自然科学基金、中科院国际合作项目和美国国立卫生研究院(R01)等的资助。
论文链接
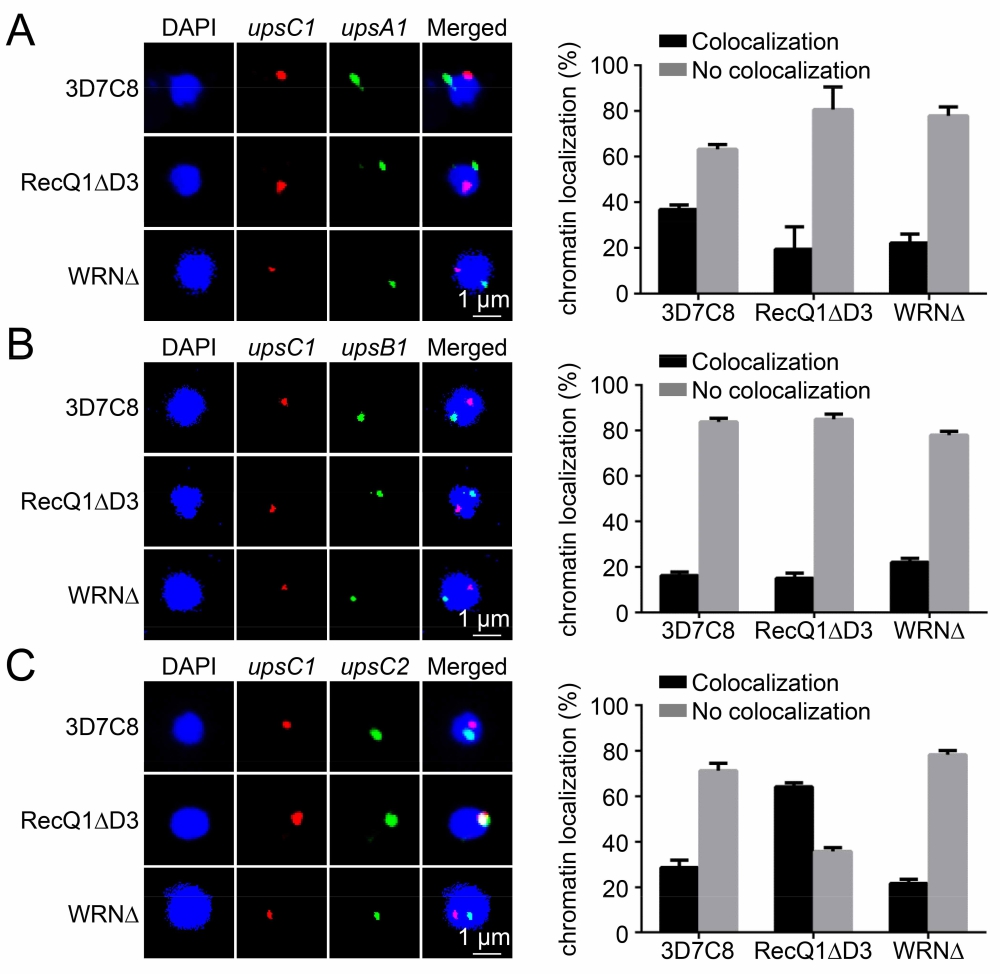
图:当PfRecQ1缺失后,var基因转录状态发生变化,其所在DNA的核周定位发生重排。
来源:中国科学院
原文链接:http://www.cas.cn/syky/201902/t20190215_4679565.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

猫抓老鼠!中科院微生物所高福院士团队揭示恶性疟原虫免疫逃逸分子机制

Cell | 刘诗欣团队揭示真核解旋酶在DNA复制起始和重启中的关键“门控”作用
演化:“最奇怪动物”身份揭秘
“欺诈”与“反欺诈”:高福院士团队揭示恶性疟原虫与人体免疫细胞博弈的“猫鼠游戏”

自然中不存在的蛋白质也能人造了!撼动材料医药界

DNA机器人一小步 癌症治疗一大步
上海有机所等在单分子水平揭示解旋酶通过相分离与DNA互作的新模式

Nature:ATP酶活性依赖的RNA解旋酶调控相分离的发生影响RNA成熟与加工

新研究揭开人类头发曲直的秘密

高福团队揭示恶性疟原虫免疫逃逸分子机制