科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-04-12
来源:CBG资讯
尽管光动力治疗(photodynamic therapy, PDT)作为一种有前景的癌症治疗方法受到科学界广泛应用,但高活性光敏剂和强光照仍有导致治疗过量的风险。然而,外加的诊断治疗探针总是使非原位监测过程变得复杂和滞后。如何实时监控光敏剂的治疗反应,降低其副作用并提高治疗效果,是一个具有挑战性的难题。
香港科技大学唐本忠院士课题组在开发聚集诱导发光(aggregation-induced emission, AIE)材料用于评估治疗反应方面做了一系列开创性工作(Chem. - Asian J. 2013, 8, 1806; J. Am. Chem. Soc. 2014, 136, 2546)。另一方面,他们利用推拉电子效应,构建了一系列红/近红外的AIE光敏剂用于细胞器靶向的光动力癌症治疗(ACS Nano 2018, 12, 8145; Adv. Mater. 2018, 30, 1802105),为开发聚集诱导发光材料用于生物治疗提供了一个新的思路。然而,想要实现其治疗反应的评估,必须加入额外的商用探针,大大增加了体系的复杂程度和操作难度。目前为止,聚集诱导发光领域尚未开发出可实时原位监测自身光动力治疗反应的荧光材料。在前期工作基础上,作者通过电荷调控,开发了一种带四个正电荷的AIE光敏剂,TPE-4EP+,具有极高的单线态氧产生效率,并在其光动力治疗诱导的细胞凋亡过程中经历线粒体到细胞核的易位,从而构建原位监测光动力治疗过程的实时自报告系统(图1, J. Am. Chem. Soc., DOI: 10.1021/jacs.9b00636)。
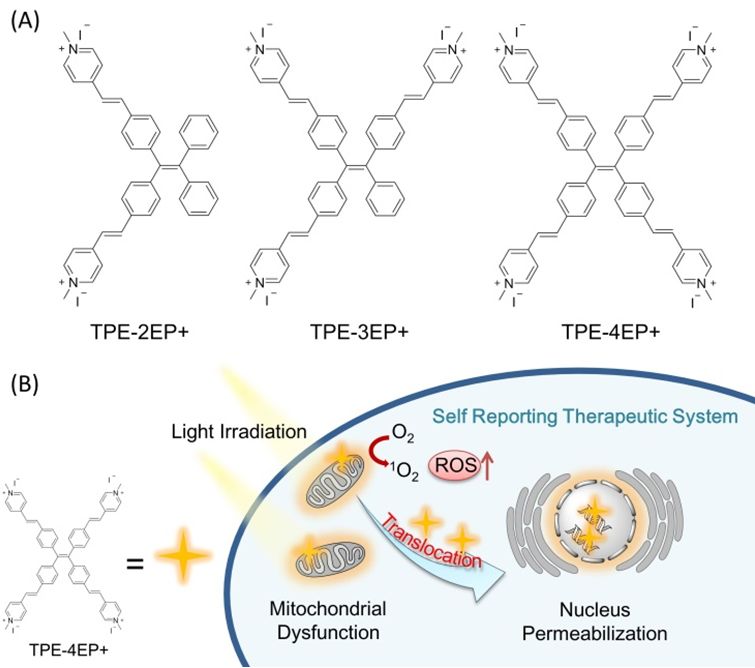
图1. 分子设计及原位监测光动力治疗过程的实时自报告系统示意图
(来源:J. Am. Chem. Soc.)
为了实现AIE材料的电荷调控,作者选用典型AIE分子四苯基乙烯(tetraphenylethylene, TPE)作为核心,不同数目的吡啶盐为正电荷单元连接在TPE转子上,合成了分别带有二、三、四个电荷的AIE材料。因为分子具有较长的共轭结构以及推拉电子效应,三个分子都具有较长波长的发射(610 nm)。
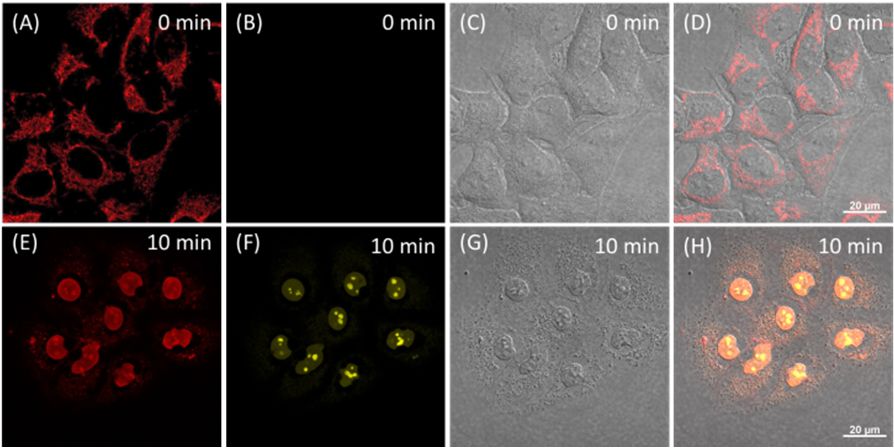
图2. TPE-4EP+在光照下的荧光易位现象
(来源:J. Am. Chem. Soc.)
在其生物应用探究过程中,作者意外地发现带有四个电荷的分子TPE-4EP+在连续光照下,荧光信号会逐渐从线粒体向细胞核区域转移(图2)。同时伴随着细胞体积收缩、胞膜小泡状以及形态学变化等细胞凋亡的典型特征。
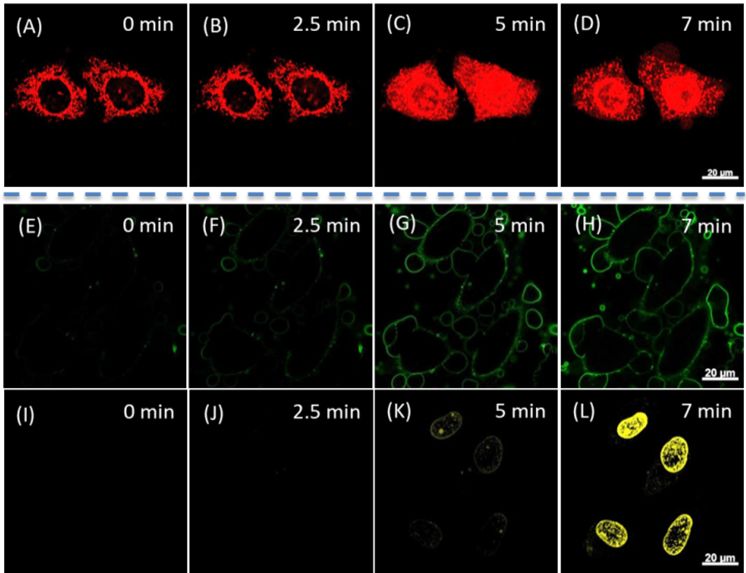
图3. Annexin V/PI联合染色实验
(来源:J. Am. Chem. Soc.)
Annexin V/PI双染色法实验进一步验证了TPE-4EP+由线粒体到细胞核的转移确实发生在细胞凋亡过程中(图3)。更重要的是,TPE-4EP+可以清楚地区分不同的细胞凋亡阶段。
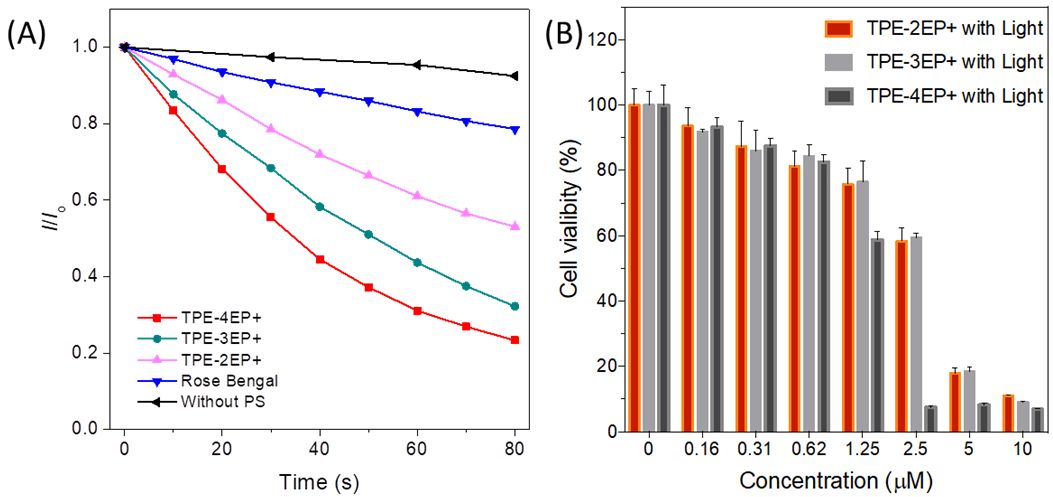
图4. 分子细胞内外的光毒性测试
(来源:J. Am. Chem. Soc.)
紧接着,作者对三个AIE分子进行了细胞内外的光毒性实验测试(图4)。结果表明,三个分子具有极高的单线态氧产生效率,在白光光照下能有效杀死癌细胞。而实验结果也显示,它们的单线态氧产生效率和光毒性与其电荷数目成正比,即TPE-2EP+<TPE-3EP+<TPE-4EP+。
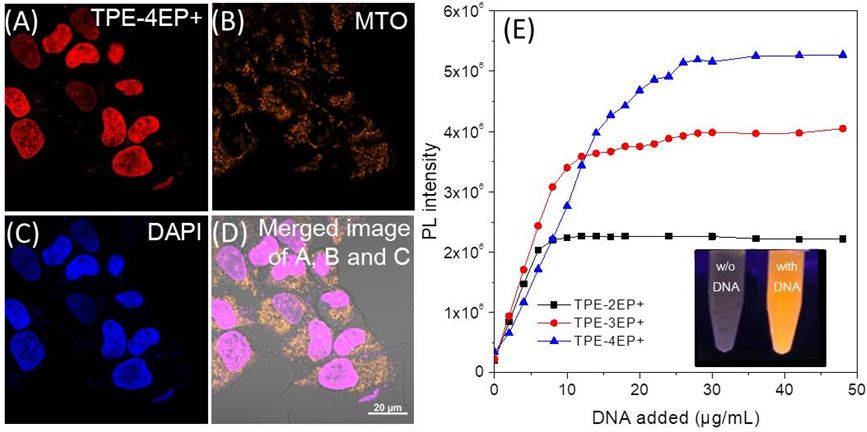
图5. 固定细胞染色实验以及DNA响应测试
(来源:J. Am. Chem. Soc.)
最后,作者进行了固定细胞实验以及DNA响应测试。结果表明,TPE-4EP+能特异性靶向固定细胞的细胞核,并与DNA特异性结合,使荧光增强。基于上述实验,作者对TPE-4EP+在细胞内的荧光转移现象作出了合理解释:在光动力治疗诱导的细胞凋亡过程中,线粒体膜电位丧失,从而使带电荷的TPE-4EP+逐渐脱离与线粒体膜的结合;而又因为核膜通透性在细胞凋亡过程中的扩大,TPE-4EP+由于静电吸附的驱动进入细胞核与核内大量DNA结合并点亮细胞核,从而实现了光动力治疗下荧光信号从线粒体向细胞核区域的转移,构建原位监测光动力治疗过程的实时自报告系统。总结:作者通过电荷调控AIE分子,开辟了一种可视化光动力治疗的新方法,从而实现有效评估治疗反应,控制光毒性以及治疗时间。此外,TPE-4EP的工作原理可为新一代PS的合理设计提供策略。该工作以“In Situ Monitoring Apoptosis Process by a Self-Reporting Photosensitizer”为题发表在J. Am. Chem. Soc.(DOI: 10.1021/jacs.9b00636)上,第一作者为香港科技大学张天富博士生,李媛媛博士为共同第一作者。通讯作者为香港科技大学唐本忠院士(论文作者:Tianfu Zhang, Yuanyuan Li, Zheng Zheng, Ruquan Ye, Yiru Zhang, Ryan T. K. Kwok, Jacky W. Y. Lam, and Ben Zhong Tang)。
来源:Polymer-science 高分子科学前沿
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5NjM5NzA5OA==&mid=2651717311&idx=3&sn=6bf674d8b050d9adcdee2128815bf411&chksm=8b49ecfabc3e65ec5d085f3d9fb1348ea8bf51a2a7c0d6673678eb080f51c70537bdb266b3d9&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
趣味科学:仰卧起坐会导致瘫痪,这是真的吗?
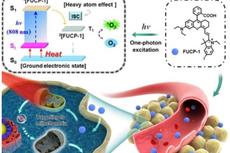
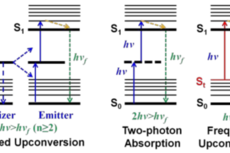
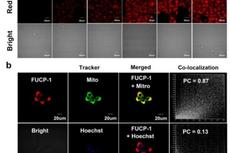
Chem.Sci: 频率上转换光敏剂用于深层肿瘤光动力治疗
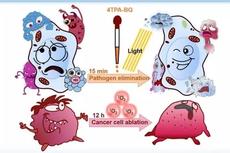
含有Anion-π+相互作用的AIE光敏剂用于多靶向、时间分辨光动力抗菌等。
石远凯的面对面视频

原位监测细胞凋亡过程的自报告光敏剂
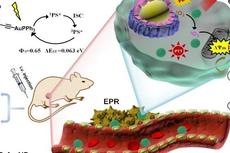
南京工业大学董晓臣教授:新型吡咯并吡咯二酮(DPP)光敏剂的光动力疗法
石远凯:探索抗癌新药
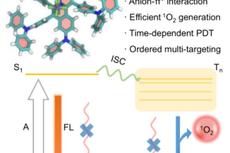
唐本忠王建国团队Angew:聚集诱导发光激活的光敏剂用于时间依赖性光动力治疗
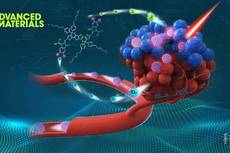
南科大田雷蕾《AM》:在开发用于光动力治疗的有机光敏剂方面取得进展

中科院科学家研究发现脂质体包埋的AIE光敏剂可用于日光下的光动力治疗