科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-26
来源:X一MOL资讯
急性髓性白血病(acute myeloid leukaemia,AML)由血细胞异常增生引起,是成年人最常见的急性白血病,成年和儿童患者的生存率都较差,五年总生存率在27%-65%之间。白血病干细胞(leukaemic stem cells,LSCs)在维持疾病的过程中扮演着关键角色,它的存在导致很多病人死于化疗耐药和疾病复发。目前的化疗药物存在治疗效果差、无法杀伤静息的LSCs以及脱靶效应等缺点,因此开发可以选择性杀伤LSCs而不损伤正常骨髓干细胞(haematopoietic stem cells, HSCs)的药物将有助于改善病人预后并降低全身性副作用。而近日威尔康奈尔医学院的Monica L. Guzman和纪念斯隆-凯特琳癌症中心Jan Grimm等研究者发现已获批用于临床的补铁剂——纳米氧化铁颗粒ferumoxytol(Feraheme)在体内外实验中对铁转运蛋白(ferroportin, FPN)表达低的白血病展现出了较强的抗癌效果,并对其抗癌机理进行了深入研究。相关研究成果发表在Nature Nanotechnology 上。
此前研究表明一些药物可以通过产生活性氧(reactive oxygen species, ROS)使LSCs对治疗更敏感,二价铁离子在过氧化物和氧气存在的条件下也可以通过芬顿反应(Fenton reaction)产生ROS,而铁转运蛋白是已知的唯一一个铁离子外排蛋白,因此在控制细胞内铁含量中发挥关键作用。已有研究发现多种癌细胞的FPN水平失调,多种癌症与周围组织中的FPN下调有关。因此FPN下调对多种癌症而言具有诊断和预后的价值。
作者在以前的研究中发现白血病干细胞和前体细胞对小分子药物产生的ROS敏感,他们猜想FPN下调是可能是这些细胞的致命弱点,因此他们对鼠源和人源的白血病细胞系以及AML病人来源的组织样品的FPN表达进行了分析。结果显示无论是RNA还是蛋白水平,白血病细胞系、白血病干细胞和病人样本都低表达FPN,这意味着这些细胞的铁离子外排功能失调。基于此,作者猜想这些细胞内的铁含量会升高,对ROS的敏感性也更高。通过将ferumoxytol与细胞共同培养,作者发现低表达FPN的细胞中的铁含量确实有所上升,而FPN高表达的细胞则无明显变化,同时ferumoxytol会导致低表达FPN的细胞内ROS的水平升高,从而导致更多细胞死亡。
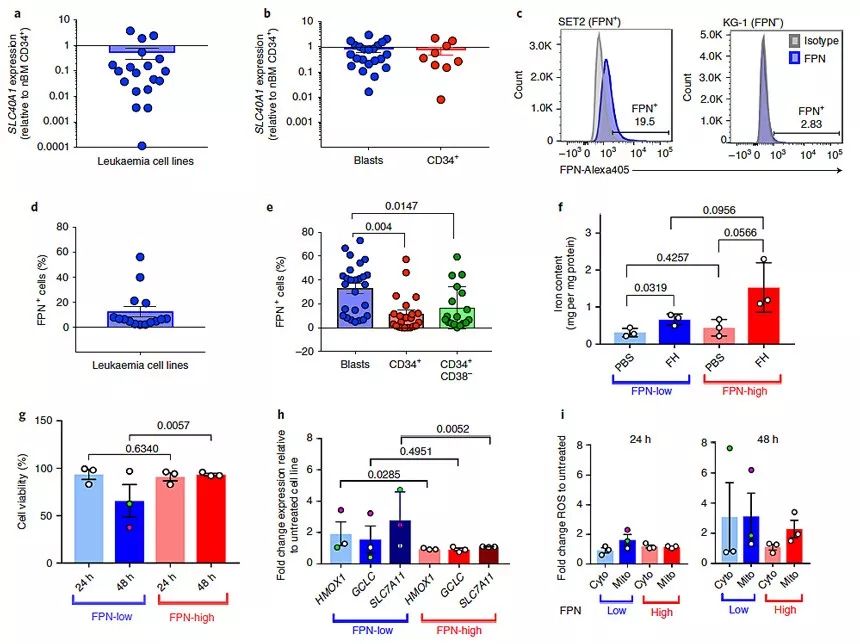
图1. 各种白血病细胞系和人源AML样本低表达FPN,从而导致细胞内铁水平和ROS水平升高。图片来源:Nat. Nanotech.
作者随后利用一种低表达SLC40A1(FPN)的bcCML细胞(同时表达GFP和YFP,GFP+YFP+)引起的白血病细胞系研究了ferumoxytol在体内的抗白血病效应。作者给小鼠注射了白血病细胞,一定时间后注射ferumoxytol进行了治疗,同时用标准的化疗药物阿糖胞苷(ara-C)进行了对比。结果显示无论是静脉注射还是腹腔注射,ferumoxytol(剂量为6 mg/kg)都可以显著降低小鼠外周血、骨髓和脾脏中的白血病细胞数量,降低脾脏的质量指数,延长小鼠的生存期,这意味着6 mg/kg的ferumoxytol具有良好的抗白血病效果。
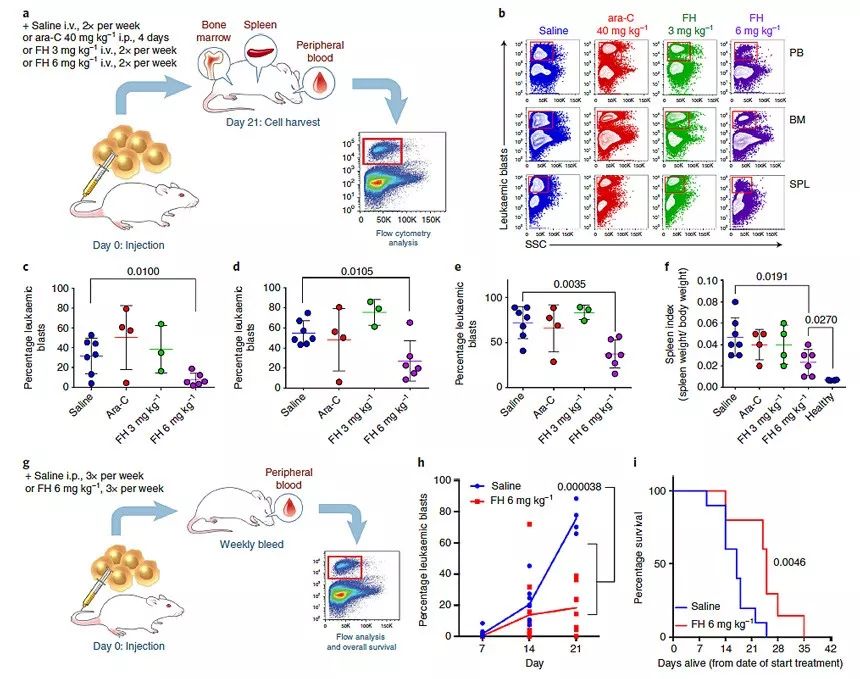
图2. Ferumoxytol抑制鼠源白血病进展,降低癌症负担并延长了小鼠生存期。图片来源:Nat. Nanotech.
接下来,作者利用病人来源的异种移植模型(patient-derived xenografts,PDX)验证了ferumoxytol的抗白血病效果。作者分别利用高表达FPN和低表达FPN的人原代AML细胞造模(AML-PDXs),然后利用ferumoxytol进行治疗。结果显示只有低表达FPN的AML-PDXs的模型的肿瘤负担显著减少,而高表达FPN的AML-PDXs则没有受到明显的影响。这表明ferumoxytol可以选择性的杀伤低表达FPN的AML细胞。通过对病人的样品进行分析,作者发现ferumoxytol治疗会导致病人组织中血红素氧化酶1(haem oxygenase-1,HMOX1)表达上调2-6倍,由于HMOX1代表着铁存在的条件下细胞的抗氧化活性,可以反应细胞的ROS水平,因此这表明ferumoxytol会增加细胞内的ROS水平,也表明这些低表达FPN的细胞对ROS的富集更敏感。
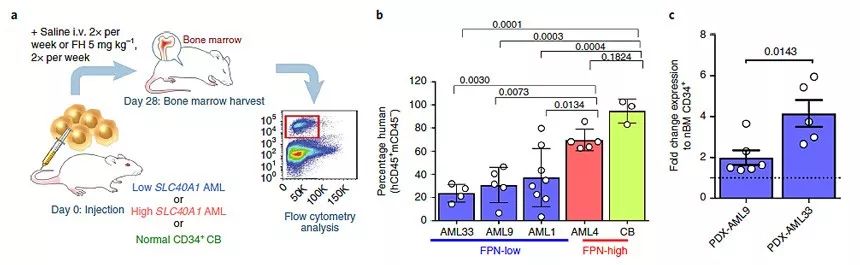
图3. Ferumoxytol抑制AML-PDXs进展。图片来源:Nat. Nanotech.

图4. Ferumoxytol特异性抑制FPN低表达的AML的机制。图片来源:Nat. Nanotech.
综上,本研究首次发现已获得FDA批准临床使用的氧化铁纳米颗粒可以特异性的治疗低表达FPN的白血病,这主要是由于FPN的低表达导致细胞内铁离子更容易富集,导致ROS水平升高,而氧化铁纳米颗粒的摄入直接加剧了这一过程,从而造成了白血病细胞的死亡,作者也在鼠源模型和人源化模型中对这一现象进行了验证。首先,这一成果表明了老药新用的重要性,指导着我们不断挖掘老药的一些新用途。其次,由于这种疗法是特异性针对低表达FPN的癌细胞,因此高表达FPN的骨髓干细胞不会受到影响,从而成功避开了传统药物的毒副作用。当然,本研究仅仅是临床前在动物身上完成的研究,因此在人体内的效果还有待进一步研究确认。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657612273&idx=2&sn=d3da0aa4f5434d2fa822ba9d2e333ff4&chksm=80f7d821b78051371247ff15997485dd3ca1b0d6a383f1786b7afa04f37cd4c1183afe609a9c&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
NEJM:里程碑!挽救急性髓性白血病的药物
胰腺特异性抗原(PaA)
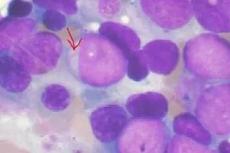
Cancer Cell:科学家在急性髓性白血病疗法开发上获重大突破!

番茄叶绿体发生的组织特异性

Cancer Cell | 老药新用—ERBB2抑制剂有望用于治疗急性髓性白血病

发现ALKBH5在急性髓细胞性白血病的关键作用
中国抗癌协会整合肿瘤学分会成立大会在西安召开




合肥研究院研发出针对急性髓性白血病FLT3-ITD突变选择性的第三代新型抑制剂
胰腺特异性抗原(PaA)

氧化铁纳米颗粒是怎样“炼”成的?