科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-30
来源:药学进展
自身免疫性疾病是一类由于机体自身免疫系统 紊乱而导致的多脏器、多系统损害的慢性疾病,主要 包括系统性红斑狼疮( systemic lupus erythematosus, SLE)、类风湿性关节炎( rheumatoid arthritis, RA)、 干燥综合征( Sjogren's syndrome, SS)、多发性肌炎 与皮肌炎( polymyositis, PM/dermatomyositis, DM)等。 这类疾病通常累及关节、肌肉、骨骼及关节周围的软 组织,患者一经确诊应当及时用药治疗,避免疾病进 一步发展造成肝肾等器官或系统的损害。临床上常用 的糖皮质激素和传统改善病情的抗风湿药物( diseasesmodifying antirheumatic drugs, DMARDs)具有良好的 抗炎、止疼以及改善或延缓病情进展的作用,至今仍 作为临床治疗风湿免疫病的一线选择。然而,针对一 线治疗单一或联用方案反应不佳或无法耐受者,需要 考虑其他具有潜在疗效的治疗方案,如干细胞移植、 生物制剂或新型植物药制剂,以及一些可能调节或抑 制免疫的抗风湿候选药物,以期缓解这类难治性风湿 病患者的病情、改善其生活质量。
1 干细胞移植
干细胞是一类具有高度自我更新能力和多向分化 潜能的细胞,有强大的组织修复和免疫调节能力。干 细胞移植疗法主要指造血干细胞移植和间充质干细胞 ( mesenchymal stem cells, MSCs)移植。前者用于自 身免疫性疾病的治疗,在短期内显示出一定的疗效,但 该方法费用高,且患者经历化疗药物预处理后不良反 应大,长期随访复发率高,目前临床已不推荐使用该 疗法。 MSCs 则由于低免疫原性、无免疫排斥、多 向分化潜能、免疫调节、造血支持等优点,已作为新的 治疗方法应用于难治性和重症自身免疫性疾病的治疗。 MSCs 的免疫调节作用主要通过抑制 T 淋巴细胞、 B 淋巴细胞、自然杀伤细胞( natural killer cells, NKs) 和树突状细胞( dendritic cells, DCs)的增殖与活化来 发挥。关于 MSCs 进一步调节 B、 T 淋巴细胞和巨 噬细胞的机制,可参见本期《间充质干细胞移植在治 疗自身免疫性疾病中的应用进展》一文。目前,国内外 关于 MSCs 移植治疗自身免疫性疾病的研究主要集中 在多发性硬化症,其次是 RA、 SLE 和狼疮性肾炎( lupus nephritis,LN)(数据来源:https://clinicaltrials.gov/, 检索截止日期: 2019 年 2 月)。临床结果显示,在各疾病采用一线治疗后加用 MSCs 疗法,安全且有效, 治疗后患者复发率低。尽管 MSCs 移植在传统方法治 疗无效的免疫性疾病患者中显示出良好的临床疗效, 且未出现严重的不良反应,但考虑到患者的移植疗效 存在个体差异,有关适用对象的选择标准以及临床应 用的给药途径、剂量、频次等均未形成共识或指南, 未来需要进一步大规模的临床试验以指导其应用。
2 生物制剂
生物制剂是一类针对机体免疫、炎症调节分子或 以受体为靶点的单克隆抗体或天然抑制剂的重组产物, 具有良好的免疫调节及抗炎活性。在自身免疫性疾病 中,生物制剂靶向作用于细胞因子和免疫细胞,通过 特异性地针对某一类炎症介质,阻断疾病的炎症进程, 从而改善及控制病情。根据作用的靶点不同,生物制剂 主要分为 3 类: 1)抗细胞因子活化的生物制剂; 2)针 对 B 淋巴细胞的生物制剂; 3)针对 T 淋巴细胞的生物 制剂。此外,还有一些针对辅助性 T 细胞 17( T helper cell 17 , Th17)的生物制剂或合成肽免疫原也进入风湿 免疫疾病的临床试验或临床治疗,具体见表 1。
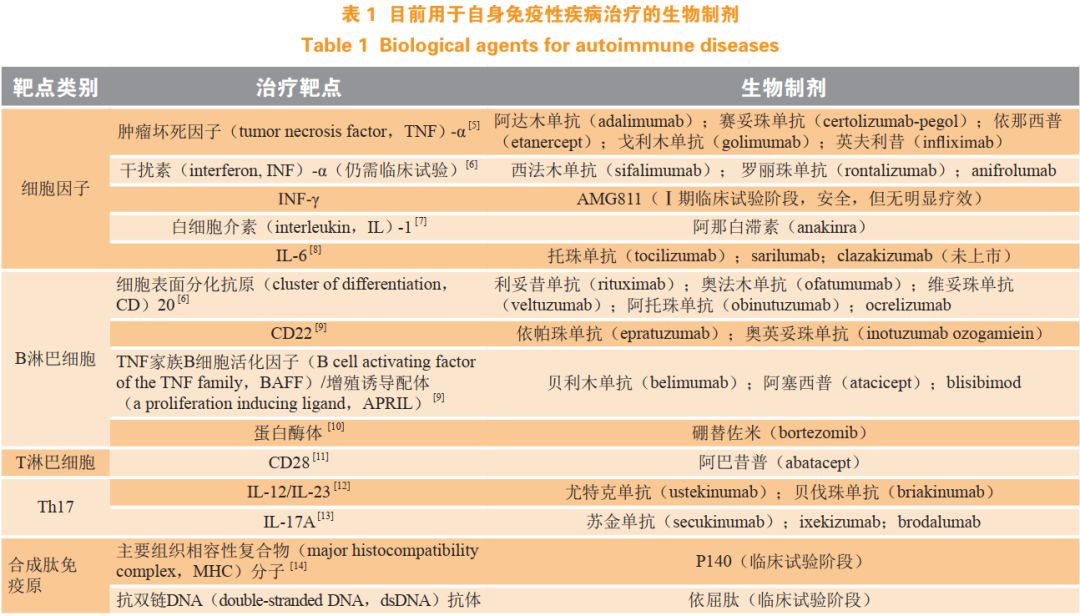
目前,生物制剂在临床上主要用于治疗 RA、银 屑 病 关 节 炎( psoriatic arthritis, PsA)、 强 直 性 脊 柱炎( ankylosing spondylitis, AS) 以 及 SLE。 TNF-α 抑 制剂在 RA、 PsA 和 AS 中的临床使用频率最高。当患者初次使用 TNF-α 抑制剂治疗失败或经历不良事件, 原则上换用另一种 TNF-α 抑制剂,若出现严重副作用 或经历 2 次及以上使用 TNF-α 抑制剂失败,则选用除 TNF-α 抑制剂以外的其他生物制剂。目前 RA 患者在非 TNF-α 抑制剂靶向生物制剂中,会首选利妥昔单抗和托 珠单抗。 SLE 患者常用针对 B 淋巴细胞的生物制剂, 贝利木单抗是首个被美国 FDA 批准用于治疗 SLE 的生 物制剂, 2 项Ⅲ期临床试验( BLISS-52 和 BLISS-76) 均证实其可缓解 SLE 患者症状并改善预后;而利妥昔 单抗对不能耐受或传统疗效不佳或严重脏器受累的难 治性 SLE 疗效较佳。 理论上,表 1 中针对各治疗靶点的生物制剂对自 身免疫性疾病应有一定改善作用,但免疫疾病发病机 制复杂,这些生物制剂的疗效及安全性尚需未来高质 量的临床多中心随机对照试验进行验证。
3 改善病情的抗风湿药物
目前, DMARDs 仍是临床上治疗自身免疫性疾病 的基本药物。鉴于同一治疗方案在不同个体中显示的 疗效和不良反应差异大,研究者们将目光投向遗传药 理学,希望通过基因标志物的测定助推个体化给药。 传 统 DMARDs 主 要 包 括 甲 氨 蝶 呤( methotrexate, MTX)、羟氯喹( hydroxychloroquine, HCQ)、硫唑 嘌呤( azathioprine, AZA)和柳氮磺吡啶( sulfasalazine, SSZ)等。新型 DMARDs 包括环孢素( cyclosporine A, CsA)、 霉 酚 酸 酯( mycophenolate mofetil, MMF)、 来氟米特( leflunomide, LEF)等。其中,有关 MTX、 HCQ、 SSZ 和 LEF 的基因多态性研究已于本期《传统 合成改善病情抗风湿药的遗传药理学研究进展》一文 中详细阐述,现对余下 3 类 DMARDs 的基因多态性研 究进行补充。
3.1 传统改善病情的抗风湿药物的基因多态性研究
AZA 是 巯 基 嘌 呤 的 1-甲 基-4-硝 基 咪 唑-5-基 衍 生物,在免疫性疾病中的应用对象主要是炎症性肠 病( inflammatory bowel disease, IBD) 患 者, 此 外,该药也用于妊娠的 SLE 患者、自身免疫性肝炎 ( autoimmune hepatitis, AIH) 及 SS 等 疾 病 的 患 者。 该药的优势在于其经济性、妊娠安全性及低肝毒性, 但是,仍有约 10% ~ 30% 的患者服药后因 AZA 相关的 不良反应而停药,其中以白细胞减少最为常见,并 且这一严重不良反应在亚洲人群的发生率较高。为了评估患者服用 AZA 发生骨髓抑制的风险, 建议患者用药前进行 AZA 代谢相关酶的基因检测, 包括硫嘌呤甲基转移酶( thiopurine methyltransferase, TPMT)和核苷酸焦磷酸酶 15( nucleotide triphosphate diphosphatase 15, NUDT15)。前者是 FDA 推荐的监 测位点,但在中国人群的突变频率低。一项涉及 87 名在笔者所在医院风湿免疫科就诊并服用 AZA 的 患者的研究结果提示: TPMT*3C 的基因突变频率仅 为 4.6%,而 NUDT15 R139C 的突变频率达到 32.1%, NUDT15 R139C 突变与服用硫唑嘌呤导致白细胞减少 显著相关 。中国 IBD 治疗药物监测专家共识]中 推荐患者用药前进行 NUDT15 基因多态性检测,以预 测用药后骨髓抑制的风险,但研究结果是否适用于其 他免疫性疾病有待多中心的大样本研究。
3.2 新型改善病情的抗风湿药物的基因多态性研究
3.2.1 环孢素 CsA 是一种钙调磷酸酶抑制剂,通过影 响细胞因子的转录从而抑制 T 淋巴细胞活化,发挥免 疫抑制作用。 CsA 体内代谢的肝药酶主要是细胞色素 P450( cytochrome P450, CYP450) 3A4 和 CYP3A5, 经肠道时部分药物还会被 P- 糖蛋白( P-glycoprotein, P-gp) 泵 出 胞 外, 减 少 药 物 的 吸 收。 研 究 表 明 CYP3A5*3 突变型纯合子患者的血药浓度更高, CYP3A4*1B、 *18B 等位基因携带者可能有药物清除率 升高的趋势, CYP3A4*22 携带者则显示出较高的 剂量调整浓度。编码 P-gp 的 ABCB1 基因中的 3 种 多态性,即 C1236T、 G2677T/A 和 C3435T,对 CsA 代 谢及疗效的影响较小,未来研究可以针对单倍型进 行分析。此外,一些参与调节 CYP 活性或 CsA 药理作 用发挥路径中涉及的分子,包括过氧化物酶体增殖剂 激 活 受 体 α( peroxisome proliferators-activated receptor alpha, PPAR-α)、 CYP450 氧化还原酶( cytochrome P450 oxidoreductase , POR)、孕烷 X 受体( pregnane X receptor, PXR)及 甲 酰 肽 受 体 1( formyl peptide receptor 1, FPR1)的基因多态性,也可能对 CsA 的 代谢及疗效产生影响。然而,目前研究多在脏器移植患 者中开展,考虑到 CsA 在风湿免疫疾病中的普遍应用, 未来应以自身免疫性疾病患者为研究对象开展 CsA 基 因多态性的研究。
3.2.2 霉酚酸酯 MMF 口服后快速脱酯化为活性产物霉 酚酸( mycophenolic acid, MPA),作用于次黄嘌呤单 磷酸脱氢酶( inosine-5'-monophosphate dehydrogenaseIMPDH),抑制 T、 B 淋巴细胞增殖,临床上常用于治 疗 SLE、 LN,并能改善硬皮病患者的间质性肺炎 [47]。 MPA 是肝脏尿苷二磷酸葡萄糖醛酸转移酶( uridine diphosphate glucuronosyl transferaseenemy, UGT) 的底 物,可被转化为无活性产物 7-O-葡萄糖苷酸霉酚酸 ( 7-O-MPA-glucuronide, MPAG)和少部分的酰基葡萄 糖苷酸霉酚酸( MPA acyl glucuronide, Ac MPAG), 后者可能与 MPA 不良反应有关。进入血液循环的 MPA 代谢物经肾小管上皮细胞外排,此过程涉及 ATP 结 合 盒 亚 家 族 C2( ATP-binding cassette subfamily C member 2 , ABCC2)及可溶性阴离子转运体( solute carrier organic anion transporter, SLCO)家族。因此, 当前与 MMF 药动学相关的基因多态性研究主要集中在 代谢酶 UGT1A9、 1A8、 2B7亚家族,以 及转运酶 ABCC2 和 SLCO1B1、 1B3亚家族。 而 MMF 的作用靶点 IMPDH的基因多态性也常被研 究与药物药效学相关性。鉴于国外研究的对象主要为器 官移植患者,且国内相关研究缺乏,未来需要从大规模 多中心的临床研究来探索中国人基因多态性与 MMF 药 动学及药效学相关性。
3.3 生物类改善病情的抗风湿药物的基因多态性研究
生物类 DMARDs,即改善病情的抗风湿药物生物 制剂。目前有关生物类 DMARDs 的遗传药理学研究 不多,主要集中于 TNF-α 抑制剂。研究表明:与 RA 易感性相关的遗传变异与 TNF-α 抑制剂治疗的反应无 显著相关性,包括 CD28 基因的 rs1980422 和 CCL21 基因的 rs2812378 等。一项涉及 65 名使用阿达木 单抗/英夫利昔单抗的银屑病患者的研究显示:包括 jagged 2( JAG2)和 adrenoceptor alpha 2A( ADRA2A) 基因在内的 10 个单核苷酸多态性,与抗 TNF-α 药物 的治疗应答相关。依那西普在银屑病中的应答情 况 与 CD84 基 因 多 态 性( rs6427528) 之 间 也 有 强 烈 关联 [61]。尤特克单抗是针对 Th17 的生物制剂,有研 究 证 实 人 类 白 细 胞 抗 原( human leukocyte antigen, HLA) -Cw 6 可 预 测 患 者 对 尤 特 克 单 抗 的 反 应, 而 IL12B rs6887695 GG 基因型表达和 rs3212227 非 AA 基因型表达显著增加了 HLA-Cw6 阳性患者治疗成功 的可能性。
由于生物制剂的疗效和安全性仍待进一步验证, 未来更明确的药理学作用可能有助于确定影响生物制 剂应答的相关基因多态性。
4 植物药制剂
植物药制剂是我国特有的一类传统 DMARDs。该 类药是从传统中药中提取的具有抗炎及免疫调节作用 的活性成分,常见的具有调节免疫功能的中药活性成 分包括苷类、多糖、生物碱及黄酮类。其中,雷公藤 多苷片和白芍总苷片对机体的免疫抑制作用较为典型,
目前在临床上已被广泛应用于自身免疫性疾病的治疗。 研究发现,不同剂量雷公藤总苷可显著抑制小鼠脾淋 巴细胞转化,阻断 T 细胞的活化信号,并抑制外 周血单核细胞 IL-13 的释放。芍药苷可以下调胶原诱 导的关节炎模型小鼠 IL-6 和 IL-12 水平,抑制 DCs 成熟, 从而下调 Th1 和 Th17 细胞数和百分比;白芍总苷对 Th 细胞的这种抑制作用在临床患者中也得到了验证。 目前,还有大量中药经临床前试验证实具有免疫 调节作用,有望成为抗风湿免疫病的候选药物。研究 显示柴胡总苷可抑制刀豆素 A 诱导的小鼠 T 细胞增殖, 并减少其释放 IL-2、 IFN-γ、 TNF-α。丹参多糖则通 过抑制 IFN-α 及 IL-1β mRNA 基因表达发挥免疫抑制作 用。 Xu 等的研究表明钩吻碱可对刀豆素 A 诱导 的 T 淋巴细胞及脂多糖( lipopolysaccharide, LPS)诱 导的 B 淋巴细胞产生抑制增殖作用。维药槌果藤则在 治疗 RA 模型大鼠研究中显示了下调 TNF-α、 IL-17a 水 平的作用,效果与雷公藤相当。此外,雪菊的黄酮类、 苯丙素类、倍半萜类和甾醇类成分展现了良好的抗炎、 抗氧化作用,也为发掘雪菊抗痛风潜力提供药效学 基础。
中医药凝聚了中华民族几千年来的实践经验,是 中国古代科学的瑰宝。但其要在现代科学文明背景下 取得突破并走向世界,必须借助现代技术与试验方法 提取、分离和纯化出有效成分,并明确药效机制。相 信未来更多高质量的科学实验数据将作为支撑,从而 推动将中药作为免疫调节剂的新药研发。
5 具有免疫调节作用的药物
维生素 D 是一种脂溶性维生素,常用于抗佝偻病, 在体内经肝肾代谢为生物作用形式 ——1, 25-二羟基维 生 素 D3[1, 25-dihydroxyvitamin D3, 1, 25(OH)2D3]。 近 来发现 1, 25(OH)2D3 与自身免疫相关,具有多种免疫 调节、抗炎和免疫抑制特性。研究表明: SLE、 RA、 多发性硬化症、克罗恩病和溃疡性结肠炎等自身免疫 性疾病患者的维生素 D 水平较低,并且低维生素 D平与疾病严重程度相关。补充维生素 D 有助于免疫 系统下调 Th1 细胞、上调 Th2 细胞,减少自身免疫反 应的发生。体内外研究发现, 1, 25(OH)2D3 的免疫调节 和免疫抑制效应包括:减少 IL-2、 IL-12 和 IL-6 的产生; 减少 INF-γ 的产生;下调 TNF 水平;上调 IL-4、 IL-5 IL-10 水平;抑制 B 淋巴细胞分泌和产生自身抗体。 此外,考虑到一些研究表明维生素 D3 对抗原呈递细胞、 活化的 T/B 淋巴细胞的作用基于存在于这些细胞中的 维生素 D 受体,未来应关注维生素 D 受体激动剂在开 发辅助自身免疫性疾病治疗方面的潜力。
辅 酶 Q10( coenzyme Q10, CoQ10) 是 一 种 人 体 内合成的脂溶性抗氧化剂,该酶有一定抗炎作用,并 能促进免疫系统功能,是一种常见的膳食补充剂。 Jhun 等的研究结果提示, CoQ10 与二甲双胍联用能改善 小鼠胶原诱导的关节炎以及线粒体功能障碍。对酵母多 糖诱导的关节炎小鼠予以 CoQ10 处理,观察到 CoQ10 减轻关节炎的严重程度并降低了血清免疫球蛋白浓度, 同时减少了 Th17 细胞和破骨细胞的分化,表明 CoQ10 可能是 RA 的潜在治疗物质 [78]。同一研究团队还验证 了益生菌复合物、锌和 CoQ10 的组合对胶原诱导的关 节炎模型小鼠的疗效,结果显示该组合疗法通过抑制 促炎细胞因子的表达、调节 Th17/Treg 平衡改善了自身 免疫性关节炎,可作为 RA 治疗的重要候选物。
6 展望
自身免疫性疾病常用的糖皮质激素、免疫抑制剂等药物,其临床疗效在大多数患者中得到了验证,但 长期用药可能引发一系列不良反应,并且考虑到受累 器官对不同免疫抑制剂的敏感性存在差异,个体化的 药物选择将是一个难题,需要临床医生结合患者的临 床表现类型使用适宜的制剂。以狼疮为例,其治疗方 案的选择可参考本期《免疫抑制药物在重症狼疮中的 应用》一文。新型疗法的开发可为患者提供更多的选择, 尤其对于一些难治性、重症患者而言,采用几种药物 合并治疗的联合疗法值得探究。
目前治疗前景最好的是干细胞移植疗法,临床研 究证实其在多种免疫疾病治疗中安全有效,但其对于 不同自身免疫性疾病的调控机制有待进一步阐明。参 与自身免疫调节相关的药物在临床上已显示出较好的 治疗潜力,但其有效性和治疗方案还需要更多大规模 的临床前、临床研究证实。生物制剂的优势在于其靶 向作用,虽疗效显著,但过敏和严重感染的风险也大, 且有研究报道机体可能再产生针对单抗的抗体,存在 耐药问题和用药安全等隐患,临床需引起关注。此外, 目前生物制剂的价格昂贵。相较之下,中国传统的植物 药制剂的开发空间较大,且原药成本低,其主要发展瓶 颈在于明确有效成分并进行分析和提纯。综上,这些具 有潜力的免疫疗法除需继续确证临床疗效及安全性外, 更重要的是探索其发挥作用的机制,以期为进一步明 确自身免疫性疾病的发病机制、开发类似或有关的可 能疗法提供新思路。
来源:ppsyxjz 药学进展
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5MDY3ODExNQ==&mid=2651305913&idx=1&sn=3ad04c96d8e0c76317f82ede01da7441&chksm=8bf4e1b5bc8368a3e9c8c9b0ca0fdce1e30775dce0bf2373381925c3bf4dae76ea6e5963a812&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

研究发现扁桃体菌群具免疫调节作用
中国被毛孢多糖免疫调节活性研究取得进展

Nature:新研究揭示肠道的免疫调节机制

研究揭示脑损伤后免疫调节机制

JCC: 生物制剂和免疫调节剂联合疗法研究
直播回放来啦 | 纳米材料用于免疫调节

Sci Adv:新研究揭示疱疹病毒免疫逃逸及宿主天然免疫调节的分子机制

生物技术
石远凯的面对面视频

中国被毛孢多糖免疫调节活性研究取得进展