科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-26
来源:X一MOL资讯
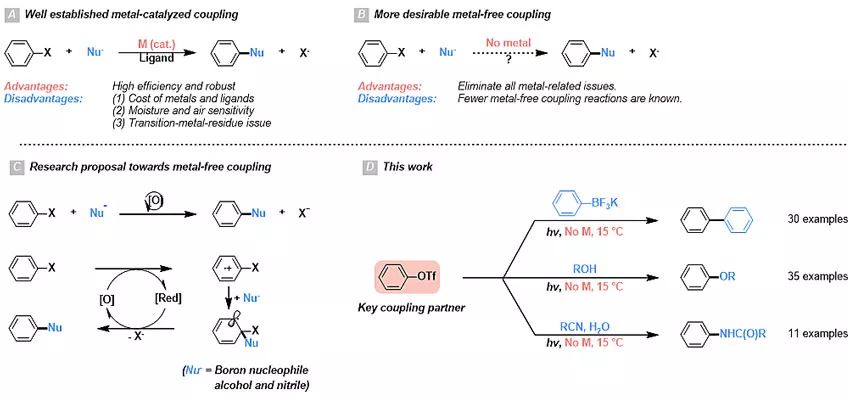
过渡金属催化的芳基卤化物和各种亲核试剂之间的交叉偶联反应在化学科学中具有重要意义。经历了几十年的研究和发展,各种各样的过渡金属催化的偶联反应已成为化学领域中形成碳-碳(C-C)、碳-氧(C-O)和碳-氮(C-N)键必不可少的手段。由于其重要性和高效性,过渡金属催化交叉偶联的发现和发展通常被认为是20世纪最重要的科学突破之一,并于2010年被授予了诺贝尔化学奖。在过渡金属,比如钯、镍和铜的参与下,各种亲核试剂可与芳基亲电试剂进行反应。这些偶联反应的一般都会经历氧化加成-转金属-还原消除的循环,而在这三个关键步骤中,过渡金属催化剂显然是必需的。除过渡金属外,影响这些反应的另一个关键因素则是配体。因此,各种具有不同的电子以及位阻效应的膦、氮和氮杂环卡宾配体(NHC)相继被发现或合成,并且得到了广泛的应用。通过配体调节金属中心的性质能够丰富催化剂的多功能性,实现高效的催化交叉偶联。
然而,金属催化剂的成本一般较高,特别是大规模工业生产过程中需要高催化剂负载的情况下,成本负担尤为沉重。一些金属配合物对水和空气敏感。这不仅使操作复杂化,还会产生安全问题。此外,在制药和电子材料行业中,为了解决“过渡金属残留问题”往往需要一些繁琐的流程和特殊设备,以将金属的含量降低到一定的水平,因而耗尽了额外的资源。由此看来,探索以及发展不依赖于过渡金属和配体的合成方案,提供将芳基卤化物或相关亲电子试剂与亲核试剂偶联的新策略,从而有效地从根源消除与金属催化剂相关问题,就显得尤为重要。
过渡金属将芳基亲电子试剂与亲核试剂偶联的能力主要依赖于它们能够自由切换氧化态的性质。由于这种独特的氧化还原活性,过渡金属可以有效地活化芳基亲电子试剂的碳-卤(C-X)键,实现三步催化循环中的氧化加成。另外一种活化芳基亲电子试剂C-X键的策略则是经历单电子转移(SET)过程,通过电子占据芳基亲电子试剂C-X反键轨道(σ*),产生自由基阴离子从而削弱C-X键。基于这种反应模式(SRN1),李朝军课题组最近报道了在无过渡金属参与的情况下从芳基氯化物,溴化物和三氟甲磺酸酯制备其碘化物的方法。受这些结果的鼓舞,以及出于对Suzuki偶联和Ullmann偶联在构建C-C、C-O以及C-N键的重要性的浓厚兴趣,该课题组开始了对相应的无金属过程的研究和开发。可惜的是,还原性较弱的亲核试剂,比如有机硼试剂和醇在先前建立的条件下并不能与芳基氯化物,溴化物和三氟甲磺酸酯反应。
基于这些结果,该课题组猜测,虽然这些交叉偶联试剂具有亲和性,但在SRN1反应条件中,这些非还原性亲核试剂要比NaI活性低。此外,即使在产生芳基自由基的情况下,它们也可能不会被较弱的亲核试剂有效地捕获。面临这些挑战的过程中,在Fukuzumi、Nicewicz、Wu等人开创性工作的启发下,该课题组设想也许通过氧化途径产生芳基阳离子能够促进这些弱亲核试剂的亲核加成。在这个反应模型的指导下,该课题组实现了无金属催化剂参与的三氟甲磺酸芳基酯与还原亲核试剂(芳基三氟硼酸盐、脂肪醇和腈)的交叉偶联反应。
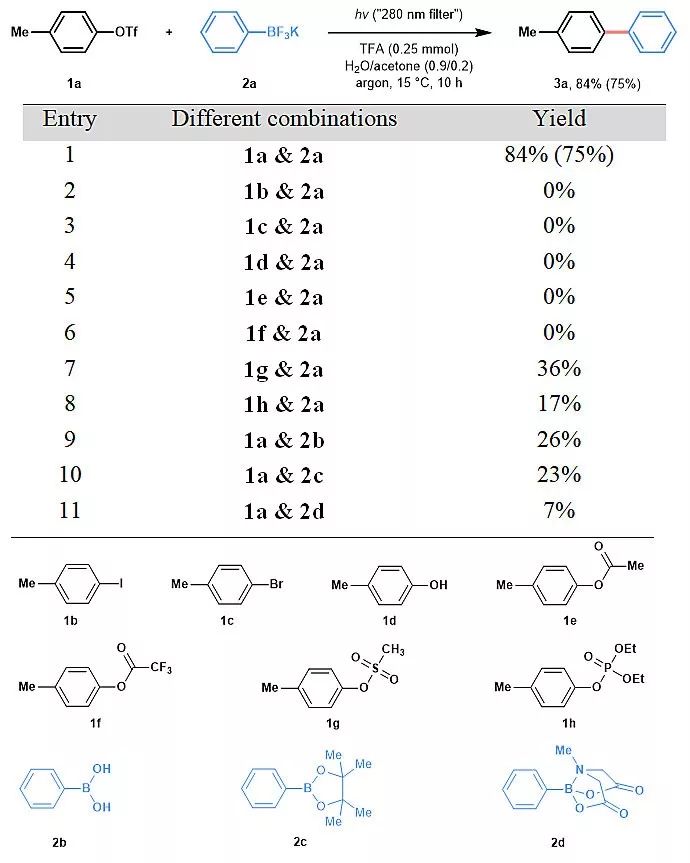
基于之前提到的反应设计,该课题组通过组合各种芳基亲电子试剂和苯基硼试剂作为偶联配偶(coupling partners)进行了研究。经过反应条件优化发现4-甲基苯基三氟甲磺酸酯(1a)可以与苯基三氟硼酸钾(2a)偶联。该反应在没有过渡金属的,光促进的最优条件下可以获得84%的产率。除了丙酮作为共溶剂外,该课题组发现水是这类反应的有效溶剂,可能原因是苯基三氟硼酸钾可以很好地溶解在这种混合溶剂中。此外,尽管水可能与之前提到的芳基阳离子进行亲核反应,该课题组在反应后没有观察到任何苯酚副产物。这表明在最优条件下,苯基三氟硼酸盐是比水更有效的亲核试剂。值得注意的是,芳基碘(1b)、芳基溴(1c)、苯酚(1d)、芳基乙酸酯(1e)和芳基三氟乙酸酯(1f)都不是合适的反应底物。而三氟甲磺酸芳基酯、甲磺酸芳基酯(1g)和磷酸芳基酯(1h)可以以较低的效率生成产物。某些酚衍生物能够参与这种无金属的Suzuki偶联的现象表明苯酚衍生物富含电子的特性可能有助于产生之前提出的芳基阳离子中间体。此外,在可以反应的酚衍生物中,由于三氟甲磺酸酯是更好的离去基团,因此三氟甲磺酸芳基酯是反应活性更高的底物。而硼亲核试剂的反应活性方面,芳基硼酸(2b)、芳基硼酸酯(2c)和氮-甲基亚氨基二乙酸(MIDA)硼酯(2d)都不如芳基三氟硼酸钾(2a)亲核性强。虽然常用的芳基溴和碘化物在该反应中不是可行的底物,但是考虑到三氟甲磺酸芳基酯能够从相应的苯酚制备,该反应相比传统交叉偶联反应还是具有独特的优势。
在确定的最优条件后,该课题组探索了这种无金属Suzuki偶联的底物普适性。各种芳基三氟甲磺酸酯均可与芳基三氟硼酸盐以中等至良好的产率进行偶联。可能是空间效应的影响,在对位和间位有取代基的芳基三氟甲磺酸酯比邻位取代基的底物有更高的收率。富电子的和缺电子芳基三氟甲磺酸酯都是有效的底物,并且富电子的芳基三氟甲磺酸酯能够以更高的产率生成产物。和传统的钯催化的Suzuki偶联有所区别,这种无金属参与的偶联策略在使用带取代基的芳基三氟硼酸盐时会生成区域异构体。这是因为作为一种富电子芳基亲核试剂,芳基三氟硼酸盐具有的多个亲核位点导致了这种区域选择性。
基于这个反应模型,也许其他的亲核试剂也能在类似的条件下实现和芳基三氟硼酸盐的偶联。值得高兴的是,通过稍微改变反应条件,各种脂族醇和腈都能参与反应生成对应的芳基烷基醚以及酰基苯胺,从而实现了无过渡金属参与的Ullmann和Ritter反应。与之前的Suzuki偶联相似,丙酮在这些反应中作为关键促进剂,而且只有芳基三氟甲磺酸酯是有效的偶联反应物,而芳基溴和芳基碘不能产生所需的产物。与其他涉及芳基阳离子的反应不同,在该反应中只有ipso取代的产物可以被检测到。
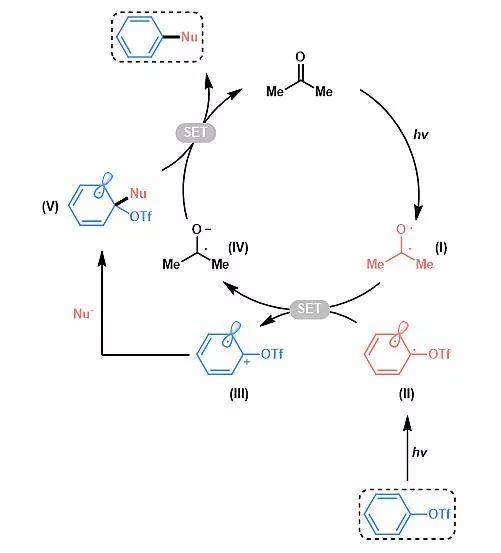
通过进行大量的机理实验,包括了自然布局分析(natural population analysis, NPA)、循环伏安法测定以及紫外-可见光光学实验,该课题组提出了以下的可能机理机制。在光照条件下,丙酮和芳基三氟甲磺酸酯均会被激发至其三重态(I和II)。这些具有高反应性的物种通过发生SET过程以产生自由基阳离子III和自由基阴离子IV。在与亲核试剂反应后,芳基自由基阳离子将转化为自由基中间体V。随后中间体IV和V经历了另一个SET过程,实现了V的归芳化以及将三氟甲磺酸根离子作为离去基团导致产物的生成。
总的来说,该课题组发展了一种无需过渡金属参与的交叉偶联反应。该反应实现了三氟甲磺酸芳基酯与芳基三氟硼酸盐、脂族醇以及腈的偶联。考虑到这些反应的简单性和实用性,该课题组预计这些结果将开辟新的交叉偶联反应的方法。
这一成果近期发表在Journal of the American Chemical Society 上,文章的第一作者是博后刘文博,第二作者为博士研究生李健斌。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657614303&idx=6&sn=167233a29faa316a87a6304b59082fdf&chksm=80f7d00fb7805919c25c3f03e5a9b6cef2922e38bfd4b5cce8f670bc252a952688cea49eb66e&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
过渡金属 试剂 甲磺酸 光反应 氟硼酸 亲核试剂 三氟甲磺酸
JACS:LiCl加速的芳基氯化物与芳基三氟甲磺酸酯之间的交叉偶联



三氟甲磺酸三甲基硅酯
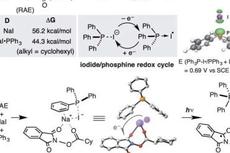
Science述评:光反应的新生力—PPh3&NaI光氧化还原体系
α-羟基-2-吡啶甲磺酸
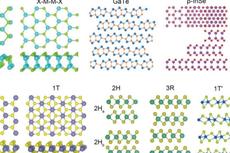
魏钟鸣课题组:综述二维金属硫化物的结构和器件应用

用eg电子占据作为催化活性描述符来指导纳米酶的理性设计
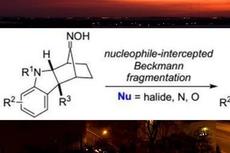
达特茅斯学院Jimmy Wu课题组实现亲核试剂拦截的Beckmann裂解

李朝军综述:无过渡金属参与的芳基亲电试剂取代和偶联光反应

EES: 原子级分散的过渡金属氮碳催化剂-普适性与规模化制备及应用

加州理工学院Reisman课题组在镍催化下将三氟甲磺酸烯醇酯转化为卤代烯