科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-07-04
来源:X一MOL资讯
芳香胺化合物普遍存在于天然产物、药物分子和功能材料中,因此,如何高效精准地构建C-N键是有机合成领域中一个重要的研究方向。其中C-H键的直接胺化反应凭借其原子经济性,得到了研究者的广泛关注。近年来,钌催化的C-H键胺化反应相继被报道,但更多的是构建三级芳香胺,直接得到二级芳香胺的研究成果相对较少。最近,兰州大学的梁永民课题组报道了氮杂环导向的芳环邻位选择性胺化反应。作者采用十二羰基合钌作为金属催化剂,以di-tert-butyldiaziridinone作为胺化试剂,化学专一性的实现了芳环邻位胺化。该方法可直接生成二级芳香胺,并可以进一步转化得到相应的苯胺衍生物(图1)。
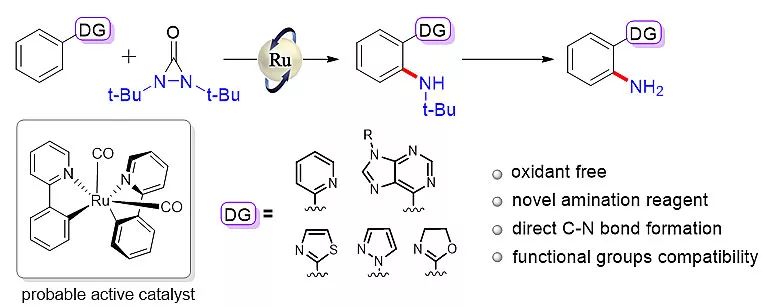
图1. 钌催化芳环邻位选择性胺化
作者在反应条件的优化过程中发现一氧化碳配体在反应过程中起了十分关键的作用,只有含有一氧化碳的Ru催化剂才能使反应顺利的进行。随后,作者发现在标准条件下不加碱时,仍能以34%的分离产率得到目标产物。据此实验结果,作者推测该反应的C-H活化经历了十二羰基合钌协助下的芳环邻位去质子化过程,一氧化碳作为配体可有效促进C-H键活化,密度泛函理论(DFT)计算结果进一步支持了这一推测。在后续的底物拓展中他们发现,该反应对不同电性的官能团如卤代物、硝基、氰基、醛基、三氟甲基等均有很好的兼容性,并能得到理想的产率。当使用含有不同取代基的嘌呤做为引导基团时,以此方法也能够得到相应的目标产物(3ak、3al)。(图2)。
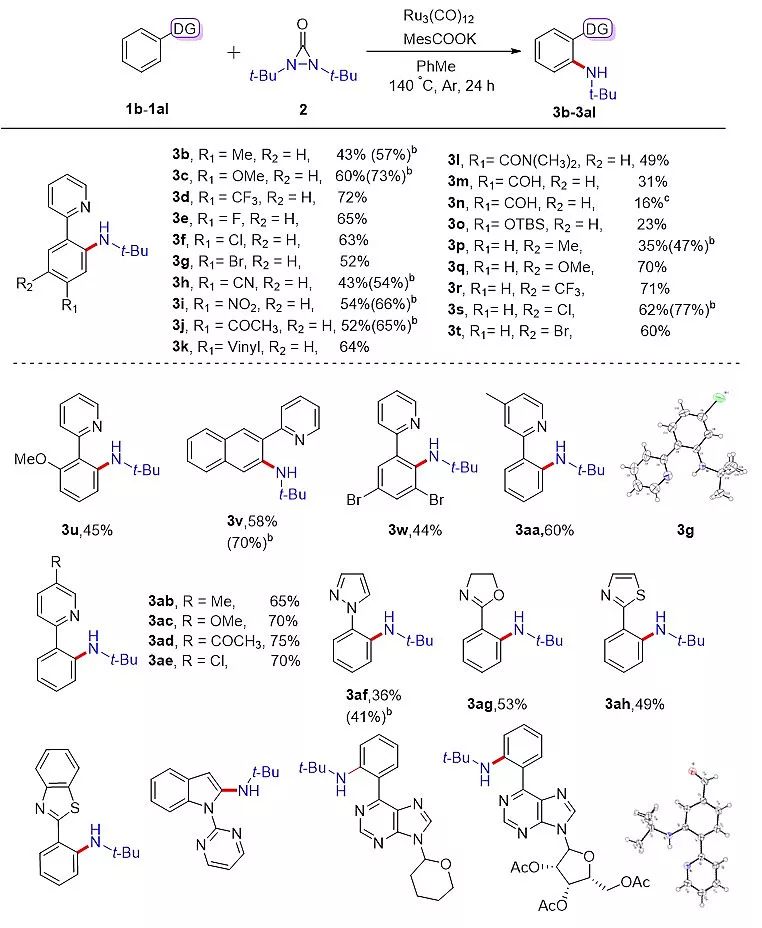
图2. 反应普适性研究
为进一步探究反应的机理,作者进行了一系列机理验证实验。包括氢/氘交换实验、自由基捕获实验、动力学同位素效应(KIE)研究等。随后作者合成了反应过程中可能经历的间体--18电子八面体钌复合物,并通过实验验证了该中间体在此反应中的可行性。最后提出了可能的反应机理(图3)。
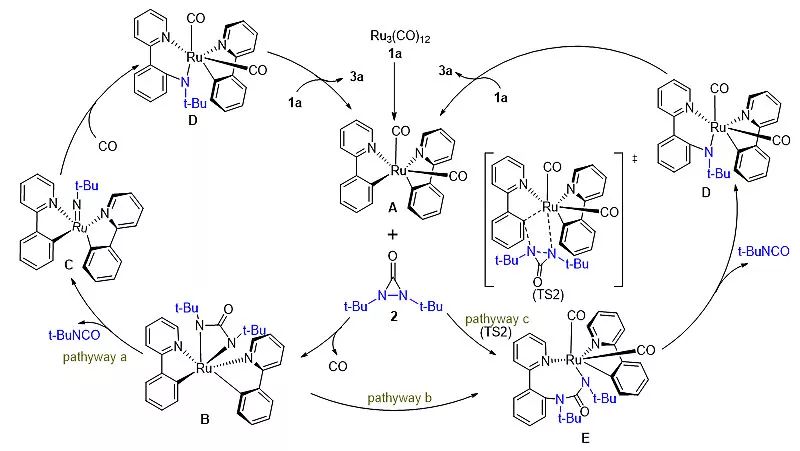
图3. 可能的反应机理
综上所述,作者用di-tert-butyldiaziridinone作为胺化试剂,高效地实现了钌催化的芳烃邻位选择性胺化反应。该反应适用于吡啶、噁唑、噻唑、嘌呤等含氮杂环取代的芳烃底物。机理研究实验证明该反应经历了钌参与的邻位C-H活化过程,并推测催化过程中形成了18电子八面体钌复合物活性中间体。相关成果近期发表在Chem. Commun.上,兰州大学的硕士生苟学亚和香港中文大学的博士生李宇科是该论文的共同第一作者,梁永民教授为通讯作者。
Ruthenium-catalyzed ortho-selective CAr-H amination of heteroaryl arenes with di-tert-butyldiaziridinone
Xue-Ya Gou, Yuke Li, Xin-Gang Wang, Hong-Chao Liu, Bo-Sheng Zhang, Jia-Hui Zhao, Zhao-Zhao Zhou, Yong-Min Liang
Chem. Commun., 2019, 55, 5487-5490, DOI: 10.1039/C9CC02499A
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657614895&idx=6&sn=873c76bef337ffcb247b5e032209f0a1&chksm=80f7d5ffb7805ce917726e510312df6359d0fd3cd48ed37af8b5b83f77bf4f8d549c50fcf5fa&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
苹果WWDC 2017干货亮点全在这里

【前沿】一周科技新闻

中国科技新闻学会倡议书

【前沿】纵览一周科技新闻
动物学: 侦察蚁能够引导搬运食物的同窝蚂蚁回家

2019年“湖南十大科技新闻”揭晓
动物学: 加拉帕格斯群岛的鸟儿喜欢吃花

2020年国内十大科技新闻解读

【纵览】一周科技新闻
2018年国内十大科技新闻解读