科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-09-18
来源:BioArt
随着现代生活水平的提高和过多高热量食物的摄入,肥胖的发病率在过去几十年迅速增加,已成为全世界范围的流行病。肥胖的发病率不断增长,并且被认为是癌症等慢性病和死亡率升高的主要危险因素。大量研究表明肥胖与心血管疾病关系密切,特别是冠心病、心衰和房颤。肥胖也与心肌肥厚、心室功能障碍和舒张顺应性降低的发生发展有关。肥胖患者多发射血分数正常性心衰,而少见严重的左室收缩功能障碍。目前针对肥胖性心肌病缺乏有效的药物治疗手段,寻找有针对性的防治靶点一直是医学界关注的重要课题。
近日,复旦大学中山医院张英梅教授、任骏教授团队在Science Advances发表了题为“FUNDC1 Interacts with FBXL2 to Govern Mitochondrial Integrity and Cardiac Function through an IP3R3-Dependent Manner in Obesity”的研究,报道了线粒体自噬蛋白FUNDC1在调节肥胖性心肌病的新机制,并为肥胖性心肌病的干预提供了新的潜在分子靶标。FUNDC1是一种调控线粒体自噬的关键受体, 既往研究表明FUNDC1是线粒体质量控制的关键线粒体膜蛋白。其功能改变与多种心血管疾病(心肌梗死、缺血性心肌病)密切相关。

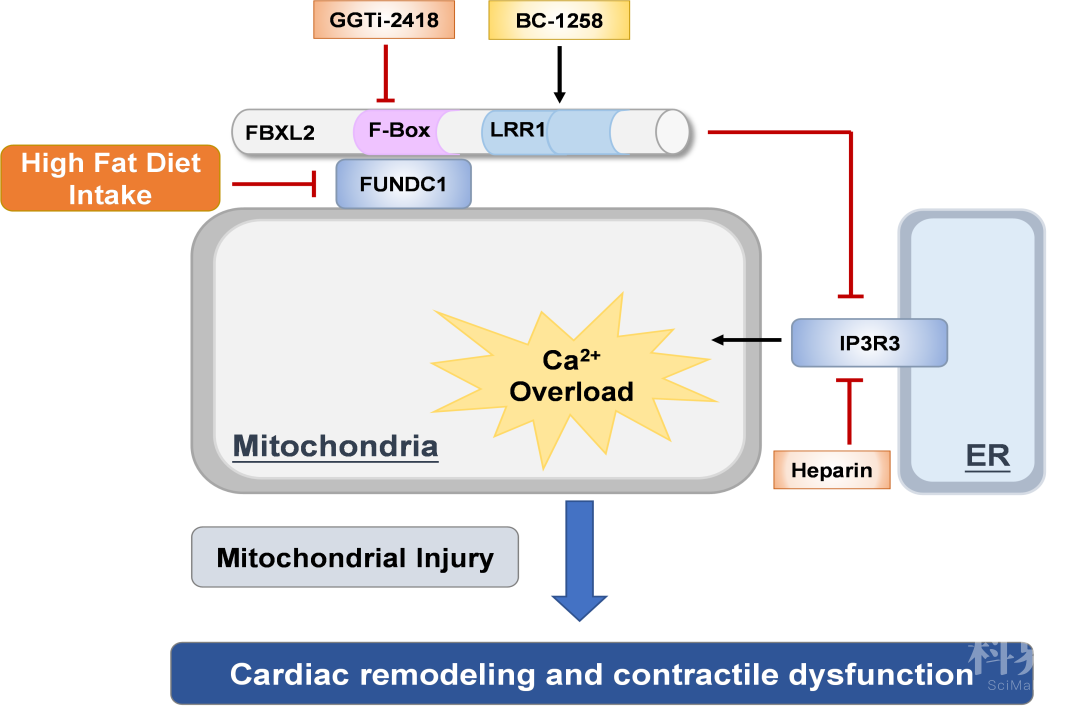
在该项研究中,研究人员发现了线粒体蛋白FUNDC1与人SCF泛素连接酶复合体的受体亚基FBXL2之间存在相互作用,且这两种蛋白的相互作用通过进一步调节IP3R3受体的降解对线粒体钙稳态起到调控作用。该团队构建FUNDC1基因敲除小鼠,发现FUNDC1的缺失加剧了高脂饮食引起的心肌重塑、心肌功能下降、线粒体异常和细胞死亡,同时IP3R3水平升高、心肌细胞内钙超载。通过质谱分析和免疫共沉淀,进一步揭示了FUNDC1和FBXL2通过FBXL2的F-box结构域相互作用。激活或过表达FBXL2或抑制IP3R3可以缓解脂毒性诱导的心脏损害,但破坏FBXL2定位则加重这种心肌损伤。同时,FUNDC1缺失促进了棕榈酸诱导的FBXL2的降解但减少了IP3R3降解,从而对维持线粒体钙稳态和保护心脏功能方面起至关重要的作用。
该研究首次描述了FUNDC1与肥胖型心肌病的关系,并确定FUNDC1及其互作蛋白FBXL2可作为肥胖型心肌病的防治靶点,为肥胖型心肌病的相关药物开发提供了重要科学思路。该研究表明组织特异性地调控FBXL2通路,是下一步糖脂代谢紊乱心血管疾病药物开发的重要方向,能够提高肥胖人群心血管疾病患者的健康效益。
复旦大学中山医院张英梅教授为文章的通讯作者,任骏教授、中山医院心内科孙明明博士后,解放军总医院心内科周浩医生为文章的并列第一作者。此项工作是团队对肥胖症心血管系列研究的又一个延伸,我国学者与国外学者就代谢紊乱中自噬失调进行了大量工作,2018年张英梅教授任骏教授在由艾维Elsevier 出版的Autophagy and cardiometabolic disease (任骏,James R. Sowers, 张英梅主编)以及在 Nature Review Endocrinol 上曾系统总结回顾了自噬失调在代谢紊乱中尤其是肥胖症中多种心血管病的发生与发展,而该工作则提示FUNDC1介导的线粒体自噬可能在自噬钝化导向线粒体损伤中其至关作用。
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652499788&idx=7&sn=4470fced3fb7f9f9689da070f6a54c39&chksm=84e27cf8b395f5eecf356450184ef8c4be4471c02ee772cac12d366e44c64aef7511eacd170d&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

研究显示六至八月出生更易患心血管疾病

超强地磁暴带来极光,会导致头疼、心血管病吗?
“2018中国卒中学会红手环志愿者服务团胆固醇管理月-红五月行动”即将启动

学术发布 | 重视心血管病与糖代谢异常“共病”患者的心血管风险综合管理

新研究:吸烟或提高心血管病与脑卒中风险
《中国心血管病报告》

直播预告|心血管病的预防与养生保健

痛惜!心血管病专家陈灏珠院士逝世

昆明动物所等在百岁老人健康长寿保护机制研究中取得进展----中国科学院

痛惜!我国著名心血管病专家陈灏珠院士逝世