科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-09-11
9月9日,国际学术期刊Cell Research 在线发表了中国科学院上海营养与健康研究所潘巍峻研究组题为Endothelial CDS2 Deficiency Causes VEGFA-mediated Vascular Regression and Tumor Inhibition 的研究论文,该工作首次揭示了VEGFA (Vascular endothelial growth factor-A)信号通路的功能存在两面性,即,VEGFA既可以促进血管新生也可以诱导血管退化,这一过程受CDS2 (CDP-diacylglycerol synthetase-2)控制的磷脂酰肌醇代谢循环调控。内皮细胞CDS2缺失能够将VEGFA信号通路的功能从促进血管新生转变为诱导血管退化,并通过肿瘤自身分泌的VEGFA达到抑制肿瘤生长的目的。
内皮细胞响应信号刺激对血管形态、稳态和功能的调控至关重要。血管内皮生长因子A (VEGFA)自20世纪80年代被鉴定以来,其主要功能之一便是促进血管生长。该研究在斑马鱼中发现,在VEGFA刺激条件下,cds2基因突变胚胎的血管能够发生血管退化。斑马鱼活体成像技术表明,cds2突变体的内皮细胞受VEGFA刺激能够通过逆向迁移和细胞凋亡来诱导血管退化。小鼠视网膜血管和植入肿瘤血管模型进一步证实,内皮细胞CDS2缺失能够诱导VEGFA介导的血管退化。在小鼠肿瘤模型中,内皮细胞CDS2敲除能够抑制肿瘤血管生长,造成缺氧,诱导肿瘤分泌更多VEGFA,这反而能够引起肿瘤血管退化并抑制肿瘤生长。机制研究发现,在CDS2缺失条件下,VEGFA刺激减少了磷脂酰肌醇二磷酸(PIP2)的生成,随后阻断了磷脂酰肌醇三磷酸(PIP3)的产生并引起FOXO1 (Forkhead box protein O1)激活依赖的血管退化。
综上所述,该研究首次发现了VEGFA信号通路能够诱导血管退化,揭示了CDS2依赖的磷脂酰肌醇代谢环路及PIP3/FOXO1信号通路对血管变构的重要性,并表明靶向内皮细胞CDS2是一个有效的抗肿瘤血管策略。
营养与健康所博士研究生赵稳操、曹乐和上海第九人民医院博士应涵汝为该论文第一作者,潘巍峻为通讯作者。该工作得到耶鲁大学教授吴殿青、中科院生物化学与细胞生物学研究所研究员李林、中山大学教授李旭日、浙江大学教授余路阳、上海第九人民医院教授林晓曦、华东师范大学教授钟涛、营养与健康所研究员秦骏和唐芸棋的支持和帮助。
该成果得到科技部、国家自然科学基金委、中科院先导项目和科研设备开发项目等的支持。
论文链接
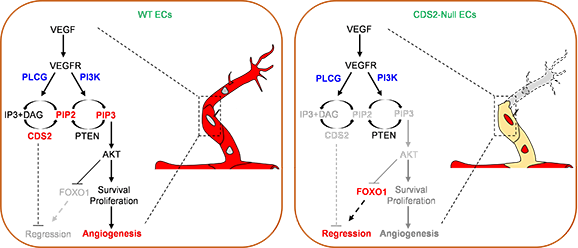
图示:VEGFA诱导CDS2缺失的内皮细胞发生血管退化的机制模式图
鎮ㄤ娇鐢ㄧ殑娴忚鍣ㄤ笉鏀寔鎴栨病鏈夊惎鐢╦avascript, 璇峰惎鐢╦avascript鍚庡啀璁块棶![video:CR新闻稿-动画]
来源:中国科学院
原文链接:http://www.cas.cn/syky/201909/t20190910_4713780.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

研究发现内皮细胞SIRPα信号调控造血祖细胞胸腺归巢和T细胞发育

研究揭示脑血管内皮细胞调控神经前体细胞顺序分化的新机制
朱明昭和王晓群课题组合作鉴定T细胞胸腺迁出调控的关键血管内皮细胞
陈真团队揭示内皮细胞对脂肪组织的调控
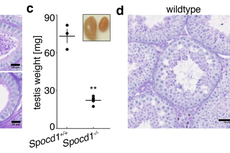
Nature | piRNA信号通路新调控因子

空间蛋白组和磷酸化修饰组联合揭示肝脏内皮细胞全景
中国抗癌协会肿瘤护理专业委员会在津成立



Cell :小鼠内皮细胞单细胞图谱

【学术前沿】 Apln+血管内皮细胞调控造血干细胞和骨髓移植

Apln+血管内皮细胞调控造血干细胞和骨髓移植