科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-09-13
来源:BioArt
非编码RNA是一类不编码蛋白质(少数情况下也有报道编码小肽)而以RNA形式发挥功能的分子。近年来的研究发现非编码RNA,包括miRNA、长链非编码RNA和环状RNA等,在生长发育和疾病,特别是肿瘤的发生发展中发挥了重要作用。也因此,非编码RNA成为分子生物学研究领域的热门。
然而,目前绝大部分研究关注的都是由RNA聚合酶II转录的非编码RNA,而对由其他RNA聚合酶产生的非编码RNA,则关注较少。
事实上,真核生物有三种RNA聚合酶,即RNA聚合酶I,II,III。其中,RNA聚合酶I专门转录rRNA;RNA 聚合酶II转录 mRNA, lncRNA, circRNA以及miRNA,snoRNA等;RNA 聚合酶III则负责转录 5SrRNA、tRNA 以及U6等其他小RNA【1】。rRNA和tRNA的研究较早,它们的结构和功能相对清晰,而由RNA聚合酶III转录的小RNA 的研究,尚有很多空白。
Vault RNAs (vtRNA)是一类由RNA聚合酶III转录的长度为88-100nt的小非编码RNA。它们与蛋白组成核糖蛋白颗粒——Vault,也因此而得名【2】。人类有4个vtRNA变体,分别为vtRNA1-1, vtRNA1-2, vtRNA1-3,vtRNA2-1。虽然每个细胞中有10000到100000个Vault颗粒,并且也发现Vault颗粒与细胞耐药,凋亡等现象相关,但具体的机制一直不明【3】。而研究发现,只有一小部分vtRNA参与Vault颗粒的形成【4】,对于大部分游离的自由的vtRNA在细胞中究竟发挥了什么功能,更是不得而知。
近日,来自德国海德堡的Matthias W. Hentze教授在Cell发表研究:The Small Non-coding Vault RNA1-1 Acts as a Riboregulator of Autophagy,该研究首次将自噬相关蛋白P62定性为RNA结合蛋白,并发现vtRNA可通过抑制P62的寡聚化(Oligomerization),从而影响细胞自噬)。

自噬是指细胞将受损或衰老的蛋白及细胞器运输到溶酶体中消化降解的过程。长期以来,自噬被认为是不具有选择性的,直到能结合特定自噬底物的受体蛋白(autophagic receptors)被发现。P62,也称为SQSTM1,就是这样的自噬受体蛋白。它的C端为泛素相关结构域,可结合被泛素化的蛋白,另外还有一个结合LC3的结构域,将所结合的蛋白带到自噬溶酶体中。P62通过N端PB1结构域发生寡聚化。寡聚化可促进P62的活性,增加与LC3的结合。重要的是,P62的寡聚化异常会引起自噬的改变,而P62寡聚化是如何被调控的,目前知之甚少。
研究者在分析2013年发表的蛋白与RNA结合数据库:RBDmap【5】,意外地发现P62蛋白竟然可以结合RNA。而这之前,P62结合RNA的能力没有被报道过。
那么P62结合什么类型的RNA?RNA的结合对P62的功能有何影响?研究者围绕这2个问题开展了研究。
iCLIP-seq数据分析显示,P62结合最多的RNA是vaultRNA和tRNA。进一步分析显示,vtRNA1-1结合P62的能力最强,远高于其他vtRNA和tRNA等。P62结合vtRNA1-1的生理意义是什么?由于自噬体也可降解RNA【6】,P62结合vtRNA1-1是为了将它带入自噬体降解吗?研究者利用siRNA敲低了P62,发现vtRNA1-1的表达几乎不受影响,这提示P62并不能使vtRNA1-1降解。
那么,vtRNA1-1是否能影响P62的功能?研究者利用LNA敲低vvtRNA1-1后发现LC3B增加,P62与LC3B的共定位增强,这提示vtRNA1-1抑制细胞自噬。
那么,vtRNA是如何抑制P62的功能,从而抑制细胞自噬的呢?研究者发现P62的锌指结构域(zz)负责结合vtRNA,而该结构域非常靠近P62的PB1结构域——负责P62寡聚化和激活P62的结构域。因此,研究者推测,vtRNA可能通过抑制P62的寡聚化,抑制自噬。研究者在饥饿(诱导自噬)和加BafA(抑制自噬)的条件下,将细胞裂解液与32P标记的vtRNA1-1孵育,并通过蛋白互作实验(IP),检测P62结合P62多聚体的情况。确实,突变vtRNA1-1结合结构域的P62变体,RK/A,结合RNA的能力减弱,结合P62多聚体的能力增加。而饥饿条件下,野生型(wt)P62结合vtRNA1-1减少。这说明vtRNA1-1抑制P62寡聚化。
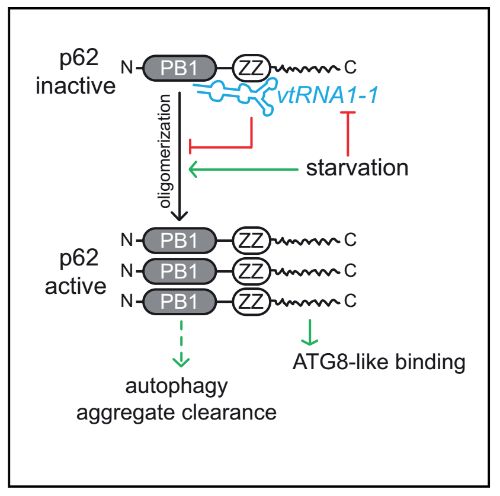
综上所述,该研究首次发现P62,虽然没有经典的RNA结合结构域,但也具有结合RNA的能力,更重要的是,P62的活性受所结合的RNA调控。VtRNA1-1通过抑制P62的寡聚化,控制P62的活性,调控细胞自噬水平。
参考文献
1.VANNINI A, CRAMER P. Conservation between the RNApolymerase I,II,and III transcription initiation machineries [J].Molecular Cell,2012,45( 4) : 439-46.
2. Kedersha, N.L., and Rome, L.H. (1986). Isolation and characterization of anovel ribonucleoprotein particle: large structures contain a single species ofsmall RNA. J. Cell Biol. 103, 699–709
3. Stadler, P.F., Chen, J.J., Hackermu¨ ller, J., Hoffmann, S., Horn, F., Khaitovich,P., Kretzschmar, A.K., Mosig, A., Prohaska, S.J., Qi, X., et al. (2009). Evolutionof vault RNAs. Mol. Biol. Evol. 26, 1975–1991.
4. Kickhoefer, V.A., Rajavel, K.S., Scheffer, G.L., Dalton, W.S., Scheper, R.J., and Rome, L.H. (1998). Vaults are up-regulated in multidrug-resistant cancer cell lines. J. Biol. Chem. 273, 8971–8974
5. Castello, A., Fischer, B., Frese, C.K., Horos, R., Alleaume, A.M., Foehr, S.,Curk, T., Krijgsveld, J., and Hentze, M.W. (2016). Comprehensive identification of RNA-binding domains in human cells. Mol. Cell 63, 696–710.
6. Yin, Z., Pascual, C., and Klionsky, D.J. (2016). Autophagy: machinery andregulation. Microb. Cell 3, 588–596
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652475267&idx=4&sn=d128fabc6e3c76e76fc89bf95d4e7b95&chksm=84e21c37b39595211c37ec41f76254e620de42af16be89703687a5ee8f2c120a4c81ef8875db&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Cell观点:功能性长非编码RNA从“垃圾”转录物演变而来
科研进展|特产所首次揭示长非编码RNA调控肌肉发育机制

生物所揭示非编码RNA协同调控固氮机制

CARPID助力非编码RNA研究

中科大瞿昆团队开发非编码RNA新技术,发现新长非编码RNA

非编码RNA领域遭重创:当年热血回国,如今17篇非编码RNA论文被质疑学术造假
中国科大在长链非编码RNA调控肿瘤形成研究中取得进展

中国科大在长链非编码RNA调控肿瘤形成研究中取得进展

清华大学揭示长链非编码RNA顺式调控基因表达新模式
苹果WWDC 2017干货亮点全在这里