科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-10-22
来源:BioWorld

各种生物体,包括我们人类每天都会受到的紫外线辐射、自由基和其他化学物质的诱变造成体内遗传物质DNA的损伤,即使没有受到外界环境的影响,细胞自身进行分裂时DNA的复制也会产生错误。
然而即便如此,为什么绝大部分生物体仍然可以维持其基因组的稳定性而正常生存呢?
研究发现,机体内拥有一套保卫系统能够时刻监视,一旦发生错误,就立刻启动DNA修复机制。
2015年,三位科学家 Tomas Lindahl(瑞典),Paul Modrich(美国)和Aziz Sancar(土耳其),因对DNA修复机制的贡献,共同荣获2015年诺贝尔化学奖。

2019年10月14日,福州大学化学学院林忠辉研究员、黄明东教授和李金宇教授作为共同通讯作者在国际顶尖学术期刊 Nature 子刊 Nature Chemical Biology 杂志上发表题为:Structural Basis of Sequence-specific Holliday Junction Cleavage by MOC1 的研究论文。在DNA损伤修复分子机制的研究上取得重要进展。

Holliday junction(HJ)是英国分子生物学家 Robin Holliday 于1964年首次发现,是在DNA同源重组损伤修复过程中形成的一种十字叉状的DNA连接体,在噬菌体、细菌、真菌、植物乃至动物细胞中均存在。
在DNA损伤修复完成后,HJ必须在HJ解离酶的作用下解离,从而促使两条同源DNA双链分开重新成为线性DNA。MOC1(monokaryotic chloroplast 1)是一个叶绿体特异的HJ解离酶。
林忠辉研究员研究团队结合了结构生物学、计算生物学和大量的生化数据不仅在原子水平上揭示了HJ解离酶——MOC1的催化机制,而且对RuvC家族悬而未决的底物特异性识别机制也提供了重要的启示。
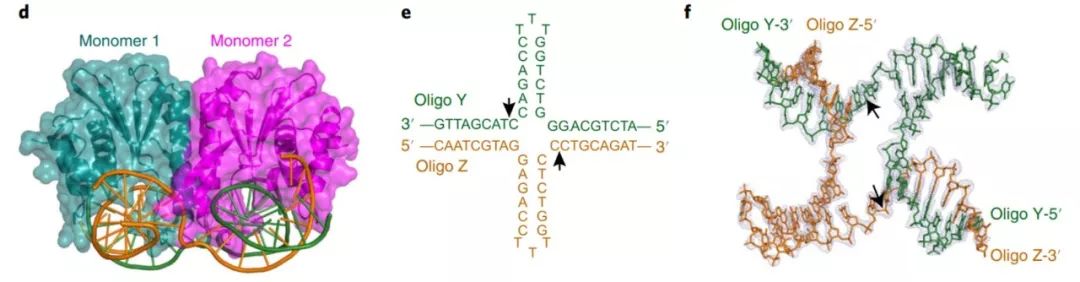
更为重要的是,该研究针对关于核酸酶如何将DNA序列上的微小差异转化成为其催化活性上的巨大不同这一科学问题,创新性地提出了一种双金属离子辅助的DNA序列特异选择性机制。
论文链接:
https://www.nature.com/articles/s41589-019-0377-4
来源:ibioworld BioWorld
原文链接:http://mp.weixin.qq.com/s?__biz=MzU1MzMxMzcyMg==&mid=2247494177&idx=4&sn=ecbbd80597ba4dcbfa5dd6f474489699&chksm=fbf61ef4cc8197e22b8107ba8e6c4bf5626b1f097ec6ca517721931c77c70a9c64f191747262&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
DNA Nature dna复制 dna分子 dna损伤修复
细胞修复DNA损伤新机制揭示

酒精造成DNA损伤的新修复通路
新研究揭示DNA损伤后的组蛋白降解促进DNA修复
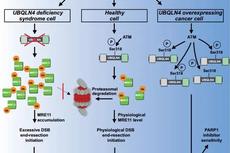
Cell: UBQLN4在DNA损伤修复中的作用

合成生物学: 一个用来控制转基因生物的内置毁灭开关
王艳丽:做研究就像破案

自然中不存在的蛋白质也能人造了!撼动材料医药界

DNA损伤修复蛋白动力学研究获进展

DNA机器人一小步 癌症治疗一大步

华裔女科学家实现天才的想法:发明全自动DNA分子机器人