科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-09
来源:BioArt
在创新药物研发中,一个核心问题是如何快速发现具有理想生物学特性的新化学实体。然而,满足Lipinski's类药性的化学空间所包含的理论分子数可能超过1063【1】,如何更高效地探索这样巨大的多样性空间,找到具有良好的可合成性和成药性的新分子是摆在计算化学家和药物化学家面前的一道难题。针对这一问题,Reymond团队利用穷举法构建重原子数在13到17范围之内的分子结构,建立了包含有166亿个化合物的GDB库【2】;Levré等人从市售的炔烃和叠氮化物出发通过使用Click反应规则构建了Zinclick数据库【3】,该库具有较好的可合成性但结构类型相对单一;此外,也有一些基于人工智能(Artificial Intelligence,AI) 方法,例如Segler等人利用LSTM模型设计集中化合物库【4】,Zhavoronkov等人将基于生成对抗网络 (GANs)的AI技术应用到化学空间探索【5】。虽然方法众多,但这些虚拟化合物库都面临着多样性、可合成性和成药性的多方面问题。
如果将寻找药物新化学实体看做数据科学中的采样问题,那在已知药物结构所代表的数据点附近进行采样无疑是获得类药分子结构的高效策略之一。
近日,中国科学院上海药物研究所蒋华良、郑明月课题组从已批准上市药物出发,采用电子等排体和化学反应转化规则构建了成药性拓展空间数据库DrugSpaceX (https://drugspacex.simm.ac.cn/)。研究结果近期在线发表于Nucleic Acids Research,题为“DrugSpaceX: a large screenable and synthetically tractable database extending drug space” 【6】。中国科学院上海药物研究所药物设计与发现中心 (DDDC)的蒋华良和郑明月研究员为论文通讯作者,第一作者是博士研究生杨天标,博士后李召军为共同第一作者。

目前版本的DrugSpaceX包含超过1亿种可用于虚拟筛选的新分子结构,且在类药性、可合成性和三维化学多样性空间覆盖率方面均具有突出的特点 (图1),为开展虚拟筛选和药物分子设计提供了高质量的资源。此外,DrugSpaceX还提供了几个规模较小的子集,包括10%多样性子集,扩展的类药性子集,类药性子集,先导化合物子集和片段子集等,可供用户免费下载使用。
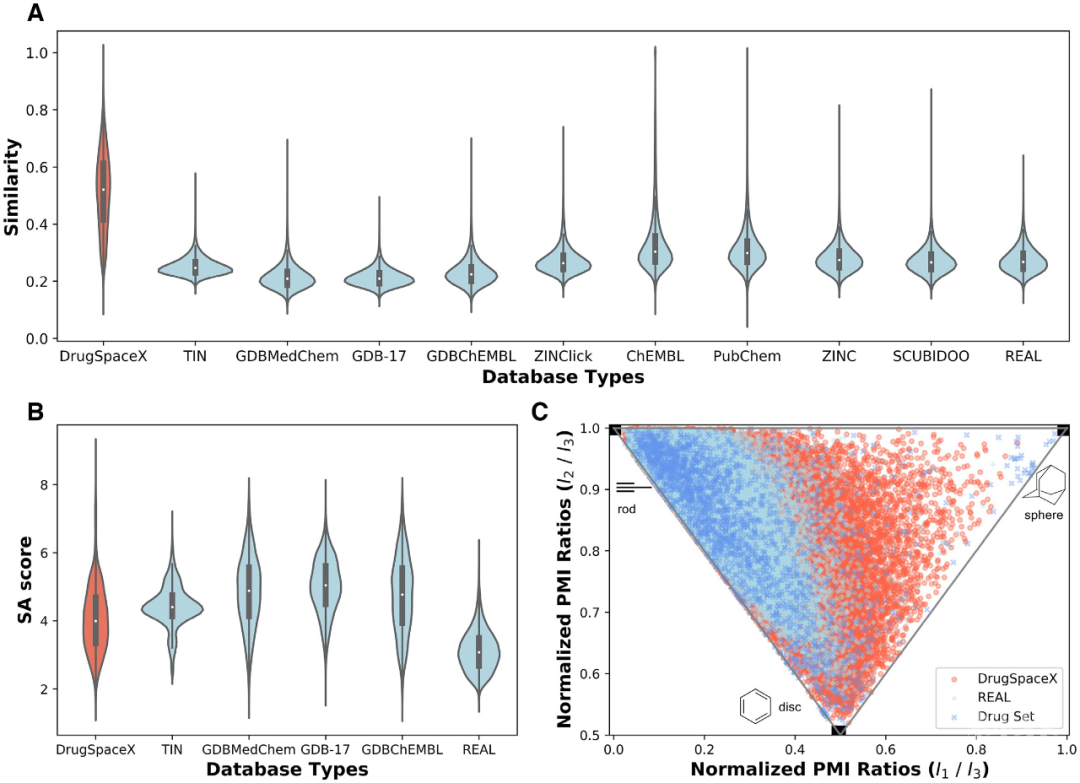
图1 DrugSpaceX数据库在类药性,可合成性和结构多样性上均具有突出的特点
研究团队使用了盘状蛋白结构域受体1 (discoidin domain receptor 1, DDR1) 进行案例研究,展示了如何利用DrugSpaceX快速筛选活性化合物 (图2)。首先,以药物数据集为出发点进行基于结构的虚拟筛选,选择分子对接打分前十的药物分子。通过文献检索可以发现其中Imatinib,Nilotinib,Ponatinib均对DDR1有交叉活性。然后,从DrugSpaceX上检索前十名药物分子第一轮衍生物,再进行第二轮筛选。可以发现,在第一轮衍生物中对接打分前十的化合物主要集中在ponatinib周围(如图2A所示),其中排名第3的化合物DE209841,已被Insilico Medicine最近报道的DDR1抑制剂专利所覆盖(NO. WO2020079652A1)。图2B中显示了DE209841的预测结合模式,与Zhavoronkov等人文章报道的结合模式吻合【5】。进一步解析重构数据集并采用相同筛选流程,可以发现对接打分和配体效率更高的新结构DE50204704。如图2C所示,该分子结构可以视作是老药Ponatinib经过对“tail” 和“linker” 片段进行两轮改造得到的。
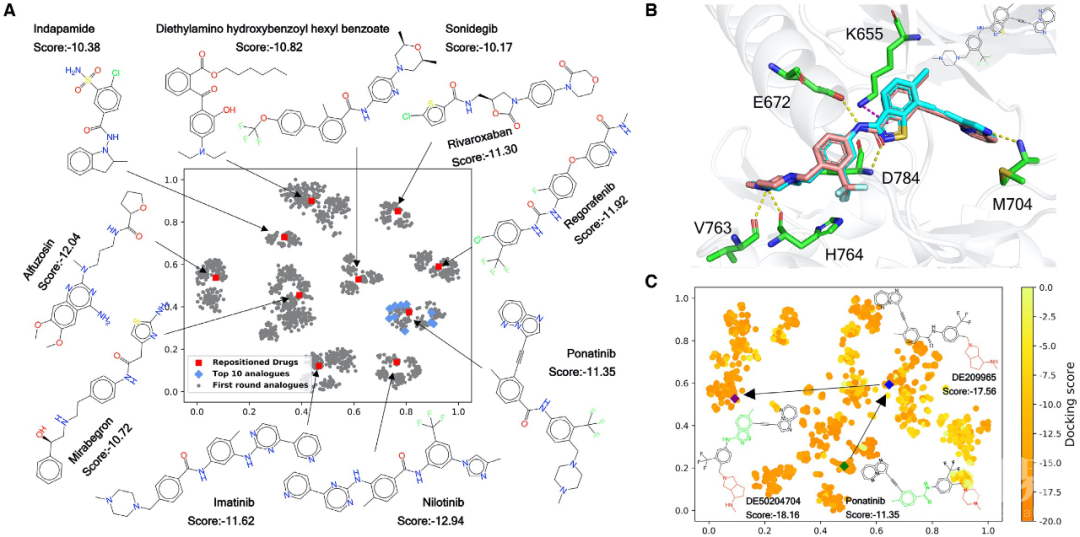
图2 预测DDR1激酶抑制剂
除了帮助药物化学家能够进行快速的骨架跃迁和分子设计, DrugSpacesX为我们提供了一种高效探索类药化学空间的思路。可以发现,通过将专家知识和人工智能相互融合,我们可以在巨大的虚拟化学空间中更容易地找到具有理想生物效应的目标化合物。此外,Christoph Gorgulla等人近期在Nature发表的文章中也指出超大规模虚筛可以提高真阳性率【7】,DrugSpaceX也可以与VirtualFlow等虚拟筛选平台结合使用,通过扩大初始筛选规模和提高筛选库质量两方面来进一步提升效率。目前,研发团队还在对DrugSpaceX进行扩充和完善,期待后续可以推出功能更为强大的版本。
参考文献
1.Reymond, J.L. (2015) The chemical space project. Acc. Chem. Res., 48, 722-730.
2.Ruddigkeit, L., van Deursen, R., Blum, L.C. and Reymond, J.L. (2012) Enumeration of 166 billion organic small molecules in the chemical universe database GDB-17. J. Chem. Inf. Model., 52, 2864-2875.
3.Levré, D., Arcisto, C., Mercalli, V. and Massarotti, A. (2019) ZINClick v.18: Expanding Chemical Space of 1,2,3-Triazoles. J. Chem. Inf. Model., 59, 1697-1702.
4.Segler, M.H.S., Kogej, T., Tyrchan, C. and Waller, M.P. (2018) Generating Focused Molecule Libraries for Drug Discovery with Recurrent Neural Networks. ACS Cent Sci, 4, 120-131.
5.Zhavoronkov, A., Ivanenkov, Y.A., Aliper, A., Veselov, M.S., Aladinskiy, V.A., Aladinskaya, A.V., Terentiev, V.A., Polykovskiy, D.A., Kuznetsov, M.D., Asadulaev, A. et al. (2019) Deep learning enables rapid identification of potent DDR1 kinase inhibitors. Nat. Biotechnol., 37, 1038-1040.
6.Yang, T., Li, Z., Chen, Y., Feng, D., Wang, G., Fu, Z., Ding, X., Tan, X., Zhao, J., Luo, X. et al. (2020) DrugSpaceX: a large screenable and synthetically tractable database extending drug space. Nucleic Acids Research.
7.Gorgulla, C., Boeszoermenyi, A., Wang, Z.F., Fischer, P.D., Coote, P.W., Padmanabha Das, K.M., Malets, Y.S., Radchenko, D.S., Moroz, Y.S., Scott, D.A. et al. (2020) An open-source drug discovery platform enables ultra-large virtual screens. Nature, 580, 663-668.
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652507381&idx=5&sn=9ac219cbba2f427e528dcd7114a67af8&chksm=84e19f41b3961657a875e4c40c6408396ab2cc99fa7cd4d8469b6ddba908a113b31b848a22cd#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
夏季太阳毒,小心“日光性皮炎”!
独家原创|提高活性气体分子的成药性策略

卫健委:做好药品集采中选药品配备使用工作

这些药品降价了!
2015年(第五届)药物毒理学年会在海口市顺利召开



合肥研究院发现成药性良好的第三代FLT3-ITD突变选择性激酶抑制剂
第六届全国药物毒理学年会在重庆成功举办




“2019年创新药物成药性评价高层学术论坛” 第二轮通知

首批鼓励仿制药品目录公布,33种药品入选!

这类药品停产!禁售!