科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-17
头抱菌素衍生物进行合成反应时,通常需将其羧酸基先行酯化予以保护。据报导,头抱菌素酸在酯化时,往往会发生羧基的α-β双键移位,而得到混合物。但随着保护酯本身的结构及合成方法的不同,所得混合物的比例也各异,规律性尚不清楚。
举例Murphy等曾对头抱菌素衍生物在碱存在下,采用酰氯法进行酯化,并对此时所发生的双键移位提出了可能形成烯酮中间体的机理。我们认为采用在碱存在下的混合酸酯法或DCCI缩合法进行醋化,也可能以下列方式生成烯酮中间体,继而发生明显的α-β双键移位。曾用噻孢霉素直接在丙酮中以三乙胺处理,则并无双键移位;而先将噻孢霉素与六甲基二硅亚胺生成噻孢霉素三甲基硅酯后,再用三乙胺处理,继而水解,则所得的噻孢霉素已发生双键移位,其△2:△3为3.5:1,这也符合上述的双键碱催化移位的机理。1
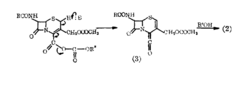
避免方法当用重氮化合物在非极性溶剂中反应时,由于生成了卡宾中间体,而对头抱菌素酸的插入反应,既无碱存在,又无极性溶剂的参与,不可能发生上述α,β-双键移位,故所得的产物均为单一的△3异构体。因此认为用重氮化合物进行头抱菌素酸的酯化是避免发生α,β-双键移位的有效方法。1
本词条内容贡献者为:
李斌 - 副教授 - 西南大学