科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-01-08
坏死性小肠结肠炎(NEC)是一种破坏早产儿肠道黏膜的致命炎症,即使痊愈也极有可能引发严重的脑损伤。但患病的肠道如何“传达”其对新生儿大脑的破坏信号依旧是科学界的未解之谜。
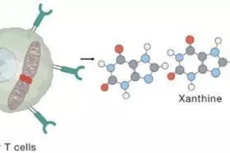
现在,这一谜题的答案呼之欲出。当地时间1月6日,美国约翰霍普金斯医学院和瑞士洛桑大学的研究人员在《科学转化医学》杂志上发表论文称,通过对NEC模型小鼠的研究,他们发现辅助性T细胞(CD4+ T细胞)会从肠道进入大脑,攻击神经细胞,从而引发严重的脑损伤。
在2018年的一项研究中,科学家们发现NEC会产生一种名为TLR4的蛋白质,激活大脑中的免疫细胞——小胶质细胞,导致白质丢失、脑损伤和认知功能下降。但当时科学家们并不清楚这两者是如何相关联的。在最新的研究中,研究人员推测CD4+ T细胞可能与此有关。CD4+ T细胞不仅可以辅助B细胞对外来入侵抗原作出反应,也负责“招募”杀伤性T细胞到炎症区域,清除感染细胞。但如果后者发生的时间和地点有误,就可能误伤健康细胞。
“我们比较了NEC患儿和其他死因婴儿的大脑,发现前者的大脑中CD4+ T细胞增多,小胶质细胞的活动也会增加。我们怀疑这些T细胞可能来自肠道的NEC发炎区域。”研究通讯作者、约翰霍普金斯大学医学院的外科教授David Hackam博士说。
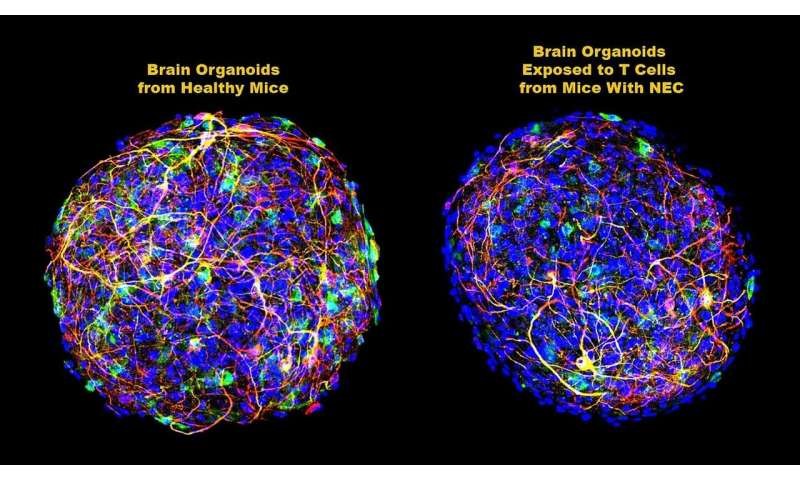
为了证明这个假设,研究人员在幼鼠身上诱导了NEC,结果发现它们大脑中的CD4+ T细胞显著增加,小胶质细胞的活性也相应增加。此外,NEC小鼠的血脑屏障非常薄弱,这也许能解释肠道中的CD4+ T细胞为何可以抵达大脑。随后,研究人员阻断了大脑中CD4+ T细胞,结果发现,小胶质细胞的活动被抑制,白质得以保存。他们也因此确定:CD4+ T细胞的积累是NEC造成脑损伤的原因。
白质是一种被称为髓磷脂的脂肪,它覆盖并保护着大脑中的神经元,促进了神经元之间的交流。为进一步明确不断积累的CD4+ T细胞如何破坏白质,研究人员将NEC小鼠的脑源性CD4+ T细胞添加到大脑类器官中,经过几周的跟踪,他们发现,随着髓磷脂减少,T细胞分泌的干扰素-γ(IFN -γ)会在类器官中积累。若单独将IFN -γ添加到大脑类器官中,则会导致炎症水平增加,髓磷脂减少。这表明,IFN -γ引导了导致NEC相关脑损伤的过程。随后,研究人员又证实了NEC小鼠的肠源性CD4+ T细胞是唯一可能导致脑损伤的细胞。
单独阻断IFN -γ对严重的NEC小鼠脑损伤发展具有显著的保护作用。因此,研究人员指出,相关疗法也许能使患有NEC的早产儿获益。
Hackam说:“我们的研究表明,NEC中的肠源性CD4+ T细胞可以转移到大脑中,造成损伤。我们所用的小鼠模型与人类的情况非常相似,因此,这可能也是患有NEC的人类早产儿的脑损伤发生机制。基于这些发现,或许我们可以通过阻断IFN -γ, 预防这类脑损伤。”
科界原创
编译:花花
审稿:西莫
责编:陈之涵
期刊来源:《科学转化医学》
期刊编号:1946-6234
原文链接:
https://medicalxpress.com/news/2021-01-mouse-link-gut-disease-brain.html
版权声明:本文由科界平台原创编译,中文内容仅供参考,一切内容以英文原版为准。转载请注明来源科技工作者之家—科界App。

研究揭示脑损伤后免疫调节机制
从健康细胞到癌细胞,或许只需要几个突变

大脑“粘合剂”:可修复脑损伤
Nature:当免疫细胞侵入衰老大脑后...

免疫代谢研究进入单细胞时代

逆转关闭的免疫细胞保护大脑老化
新研究让免疫细胞“火力全开”
脑损伤激活胶质细胞产生神经元

华人团队发文《Cell Stem Cell》——帕金森症大脑损伤得以修复
长期压力通过免疫细胞改变大脑,引发焦虑