科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-01-28
来源:植物生物学
1. 实验原理
基因枪法(Gene gun)又称粒子轰击(Particle bombardment)或基因枪轰击技术(Gene gun bombardment),由美国康奈尔大学生物化学系John.C.Sanford等于1983年研发而成。该方法主要适用于单子叶植物的遗传转化,其基本工作原理是利用氦或氮等压缩气体作为动力系统,将表面吸附有DNA的细微金粉射入细胞,最终到达细胞核完成基因转移,因此无需去除细胞壁和细胞膜。
2. 实验材料
玉米优良品系的幼胚或来源于幼胚的胚性愈伤组织
3. 主要试剂
70%酒精,2.5%次氯酸钠,无菌水,LB培养基,质粒提取试剂盒,无水乙醇,0.1mol/L亚精胺,2.5mol/L氯化钙
4. 培养基配方
愈伤诱导培养基:N6 basic salts,1.4g/L L-脯氨酸,0.1 g/L酸水解酪蛋白,2mg/L 2,4-D,10mg/L AgNO3,30g/L蔗糖
高渗培养基:N6 basic salts,0.7 g/L L-脯氨酸,0.1 g/L酸水解酪蛋白,2mg/L2,4-D,0.2M甘露醇,0.2M山梨醇,30 g/L蔗糖
恢复培养基:N6 basic salts,0.7 g/L L-脯氨酸,0.1 g/L酸水解酪蛋白,2mg/L 2,4-D,20 g/L蔗糖
分化培养基:N6 basic salts,1mg/L 6-BA,20 g/L蔗糖
生根培养基:N6 basic salts,0.5mg/L 6-BA,30 g/L蔗糖
5. 仪器设备
PDS-1000/He型基因枪
6. 实验程序
6.1 材料准备
1. 选取授粉后10天左右的玉米果穗,去除苞叶和玉米须,于超净工作台内依次用70%酒精和2.5%的次氯酸钠分别浸泡消毒5min和10min,再用无菌水冲洗4-5遍。用镊子小心剥取大约1.5-2 mm的幼胚,盾片朝上置于愈伤诱导培养基,28℃/黑暗条件下培养诱导愈伤组织。约2-3周后将诱导出的愈伤组织继代培养,每2周继代一次,至得到胚性愈伤组织。
2. 将幼胚或胚性愈伤组织均匀紧凑地置于高渗培养基上,呈直径大约3-4cm的圆形,8-12h后用于基因枪转化。
6.2 质粒的大量提取
提取用于基因枪转化的合格浓度(1µg/µl)的目的载体质粒,(索莱宝质粒大提试剂盒)提取方法如下:
1. 取-80℃保存的目的大肠杆菌菌种,接种于50mL LB液体培养基(含抗生素),37℃,250rpm振荡培养过夜。
2. 将培养物5000rpm,4℃离心3-5min,弃上清。
3. 加入5mL溶液I重悬,旋涡振荡器上剧烈振荡,使沉淀充分悬浮。
4. 加入5mL溶液II,轻轻颠倒混匀,室温放置2-5min。
5. 加入6mL溶液III,轻轻颠倒混匀,冰上放置5min。
6. 11000rpm,4℃离心10min,取上清至吸附柱,11000rpm,离心30-60s,倒掉收集管中的废液,将吸附柱放回收集管(为提高效率,可将收集管中的废液倒入吸附柱再次吸附一次)。
7. 向吸附柱中上加入7ml漂洗液(已加入无水乙醇),11000rpm,离心2min,弃废液,重复该步骤一次。
8. 将吸附柱放入一个干净的离心管中,向吸附膜中央悬空滴加1-2ml经65℃预热的洗脱液,室温放置5min,11000rpm,离心2min,收集质粒溶液用于后续实验(为增加质粒回收效率,可将得到的洗脱液重新加入吸附柱再次洗脱)。
6.3 基因枪微弹的制备
1. 称取金粉20mg(直径1.0μm),放入1.5mL无菌离心管中,加入500μL无水乙醇,剧烈震荡1min,使其悬浮静置5min,<3000 rpm离心1min,去掉上清,重复上述步骤3次。
2. 加入500μL无菌水,剧烈振荡1min,静置1min,<3000rpm离心1min,去上清;重复上述步骤3次。
3. 加入500μL无菌水,悬浮后平均分配到10支1.5mL无菌离心管中,可4℃保存。
4. 向离心管中加4μL质粒(1μg/μL),20μL 0.1mol/L亚精胺和50μL 2.5 mol/L的CaCl2,轻轻吸打混匀,冰浴静置8min。
5. <3000rpm离心1min,去掉上清,加入200μL无水乙醇,重新悬浮,<3000rpm离心1min,重复上述步骤3次。
6. 小心去掉上清,加入50μL无水乙醇,保持悬浮状态备用。
7. 基因枪转化前取10uL点于载体膜中央,使其均匀分布,晾至完全干燥备用。
6.4 基因枪转化步骤
本实验用采用BIO-RAD基因枪PDS-1000/He,方法步骤如下:
1. 打开超净工作台,用70%乙醇擦拭超净工作台和基因枪内部(注意:基因枪门不可用乙醇擦拭,以防损害有机门及封闭圈)。
2. 紫外灯照射杀菌30min。
3. 按前述步骤准备基因枪微弹。
4. 将易裂片、微弹载体、阻拦网及承载微弹载体的铜圈置于70%乙醇中浸泡15min灭菌,之后用滤纸吸干微弹载体表面的乙醇,阻拦网及铜圈在酒精灯上灼烧,置于一个垫有滤纸的无菌培养皿中冷却。
5. 将微载体置于铜圈上,将微弹迅速均匀涂于微载体上,晾干乙醇。
6. 打开压缩气瓶,调节压力至易裂片标准加200psi以上。
7. 将易裂片、阻拦网、微弹载体安装进固定装置中,调整射击参数:Gap distance 20mm;微弹载体飞行距离(Macroprojectile flight distance):10mm;微弹飞行(Particle flight distance):7cm;压力:1350psi;真空度:28.5inches Hg(载体置于第一档)。
8. 将培养皿置于托盘上,使待转化材料集中在托盘中间的圆圈内,将托盘插入基因枪倒数第二档。
9. 打开基因枪电源和真空泵。
10. 关闭基因枪门,按下抽真空键(Vac),当真空表读数达到28.5 inches Hg.时,置于“保持(Hold)”档。
11. 按下射击键(Fire),直到射击结束。
12. 按下放气键,使真空表读数归零。
13. 打开基因枪门,取出培养皿,盖好培养皿盖并用封口膜封好。
14. 重复上述步骤,直至完成转化。
6.5 转化后的组织培养
1. 将转化后的幼胚或愈伤组织继续于高渗培养基上,28℃黑暗培养过夜,转移到恢复培养基上培养1-2周。
2. 将愈伤组织转移到选择培养基(添加有相应抗生素)上,每两周选择一次,共选择三次,期间弃去衰老死亡的愈伤组织。
3. 将选择存活的抗性愈伤移至含相应抗生素的分化培养基上,16h光照/8h黑暗,28℃条件下培养,每两周继代一次。
4. 当植株长到1-2cm高时,转移到生根培养基中继续培养。
5. 3-4叶期且根系发达时,将小苗移入花盆中,并罩塑料袋保温保湿,移入温室栽培5-7d后,去掉塑料袋,一周后移入大田,直至开花结实。
来源:PlantBiotech 植物生物学
原文链接:http://mp.weixin.qq.com/s?__biz=MzI5NTk2MTcyOA==&mid=2247495332&idx=3&sn=c55ee71134cd5c161d8377cbd6a32baf
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
三乙醇铝
2-环己基乙醇
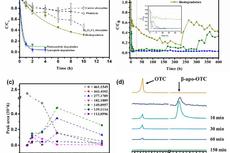
城市环境所在光催化耦合微生物同步降解抗生素及机理分析方面获进展
邻羟基苯乙醇
2-(丙基氨基)乙醇

第三届全国玉米生物学学术研讨会第一轮通知

乙醇促进法可实现秸秆乙醇高效生产
2-环戊烷乙醇
纤维素乙醇
乙醇燃料电池