科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-12-13
来源:BioArt
责编丨兮
2019年12月12日,上海科技大学生命科学与技术学院陈佳教授、免疫化学研究所杨贝副研究员与中国科学院-马普计算生物学伙伴研究所杨力研究员,应邀在Cell上发表题为“One Prime for All Editing”的专评论文(Preview),对哈佛大学David R.Liu教授近期在Nature杂志发表的Search-and-replace genome editing without double-strand breaks or donor DNA(详见BioArt报道:专家点评Nature | David Liu再出重磅基因编辑新工具,可实现碱基随意转换与增删)研究进行了系统性介绍,详细解读了新型基因编辑系统Prime Editing的工作原理,并展望了该领域未来的发展方向。

在该专评论文中,陈佳教授等对Prime Editing系统的设计原理及构建过程进行了解读(图1)。新型Prime Editing系统通过将Cas9切刻酶与逆转录酶融合表达,并利用prime editing guide RNA(pegRNA)最终实现靶位点的基因编辑。其中,pegRNA由3个部分组成,包括single-guide RNA(sgRNA)、引物结合位点(Prime Binding Site,PBS)和储存有靶向位点编辑信息的反转录模板(RT templete with edit,图1A)。Prime Editor(PE)在创建过程中经历了3步关键改进。PE1利用Cas9切刻酶(H840A)和Moloney Murine Leukemia Virus(M-MLV)逆转录酶构成,虽可以精确实现设计的基因组编辑,但在哺乳动物细胞上的编辑效率较低。因此,研究人员构建了PE2,主要是通过在M-MLV逆转录酶中引入5个氨基酸改变进而提高靶向位点的编辑效率。最后,研究人员构建了PE3/PE3b,通过共表达介导非靶向DNA单链切刻(nick)的sgRNA,利用细胞内源性错配修复(mismatch repair)途径保护编辑链的修饰信息,从而进一步提高了prime editing的效率(图1B)。Prime editing具有非常广泛的应用前景,可以实现包括12种碱基替换、小片段碱基插入和缺失等的不同编辑用途(图1C),毋庸置疑地将在基础和临床研究领域获得广泛地应用。在这一专评论文中,陈佳教授等也指出了Prime Editing系统及其应用仍有亟待改进之处:如gRNA依赖性或非依赖性的脱靶效应尚且未知;PE3介导的高碱基插入/缺失率以及PrimeEditing系统在成体动物中的递送等问题。
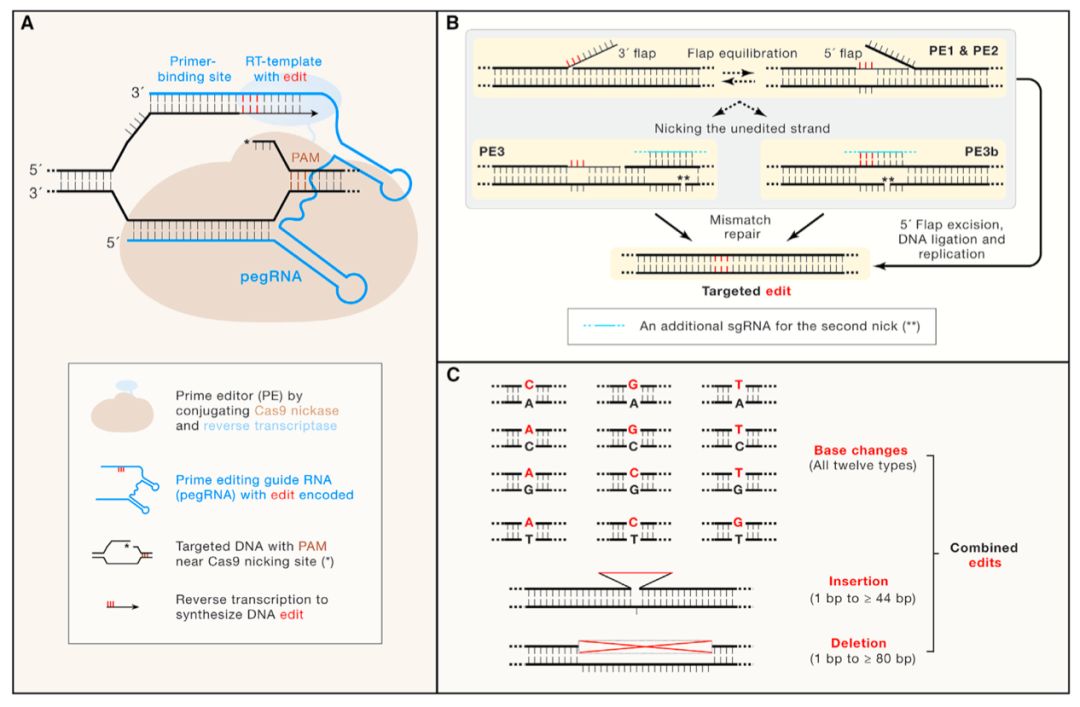
图1:PE系统的创建与应用(A)PE系统示意图(B)PE系统的创建历程(C)PE系统可以介导的编辑类型
陈佳教授长期从事DNA损伤修复机制以及基因编辑相关的研究工作,已阐明APOBEC胞嘧啶脱氨酶在CRISPR/Cas9介导的基因编辑过程中产生突变的分子机制(Lei et al., 2018, Nature Structural& Molecular Biology);在此基础上成功创建多种高效率、高精准型碱基编辑器(Wang et al., 2017, Cell Research; Liet al., 2018, Nature Biotechnology; Wang et al., 2018, NatureBiotechnology; Li et al., 2019, Cell Research);揭示了多种碱基编辑器的效能差异并构建了可编辑致病突变数据库(Wang et al., 2019, Genome Biology),并应邀撰写综述评论等探讨基因编辑领域的进展(Chen et al., 2018, Cell; Chen et al., 2019, NatureBiotechnology; Yang et al., 2019, The CRISPRJournal)。
陈佳教授、杨贝副研究员与杨力研究员为该论文的共同通讯作者。
原文链接:
https://doi.org/10.1016/j.cell.2019.11.030
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652478861&idx=5&sn=a90261f38aff5bf84b8e3414dde7b58d&chksm=84e20e39b395872ff49170bd680d1e7221c800178d0dfbc72f63eed7c3040a2f92c782b2dfba#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
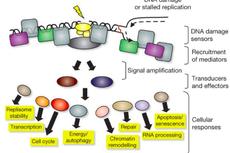
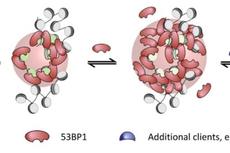
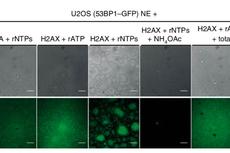
NCB:相分离可调控DNA损伤修复

蚊子怕怕了,利用转基因能破坏它们生育能力,必死无疑

袁健组发现BRD9调控DNA损伤修复新机制
编辑基因创造超人,霍金的担心是不是杞人忧天




基因编辑临床试验10原则出台

细胞修复DNA损伤新机制揭示
同样搞基因编辑,贺建奎 黄军就何以评价两极化



基因编辑有重大新进展!两大突破可高效精准矫正致病的遗传突变
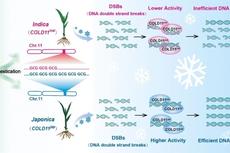
研究发现驯化选择水稻DNA寒害损伤修复机制及优异模块
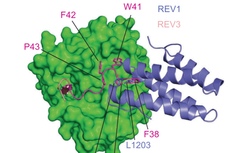
新研究揭示DNA损伤修复关键复合物的组装机制