孙熙宸
加好友
孙熙宸 2019-12-29
来源:肠道君营
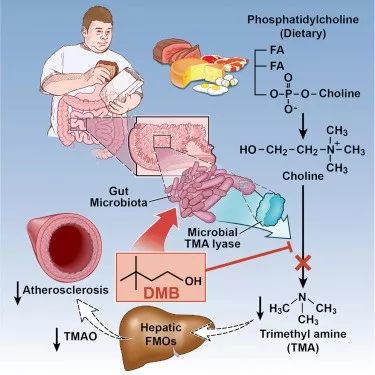
Cell:抑制由肠道微生物途径合成的氧化三甲胺(TMAO)可以有效降低动脉粥样硬化风险
众所周知,动脉粥样硬化是心血管疾病发作的主要因素之一,而高脂饮食又是动脉粥样硬化的罪魁祸首。目前对于高血脂患者而言,为了预防动脉硬化,医生开具的处方一般是他汀类药物,这类药物作用于人体,抑制人体胆固醇的合成。但那些抑制胆固醇合成的药物,毕竟是直接作用于人体的,对人体有一定的副作用。那有没有办法从源头着手呢?
已有研究表明血液中的TMAO(Trimethylamine N-oxide;三甲胺氧化物)水平与动脉粥样硬化有关联,高水平的TMAO会抑制血液中胆固醇的降解,增加动脉粥样硬化的风险。因此,降低血液中TMAO水平会有效降低动脉粥样硬化风险。
人体中TMAO的形成要经过两步:摄入高脂食物之后,食物残渣进入肠道,被肠道微生物转化为TMA(Trimethylamine,三甲胺),TMA通过血液循环进入肝脏,然后被黄素单加氧酶(flavin monooxygenases,FMOs)氧化为TMAO。这个TMAO会抑制血液中胆固醇的降解,胆固醇就不断积累沉淀到动脉血管壁,导致血管壁加厚、硬化,紧接着心脏病就发作了。
最近,来自克利夫兰诊所Stanley L. Hazen研究团队在易患动脉硬化的小鼠模型中发现,给小鼠喂食DMB(苯甲酸二甲基氨基乙酯)后,小鼠肠道中的微生物合成TMA的能力显著降低,紧接着小鼠血液中抑制胆固醇降解的TMAO水平显著降低了,即使天天给小鼠喂食高脂食物。
简而言之,DMB这种药物可以有效降低血液中TMAO水平,达到预防心血管疾病的目的。而DMB本身不是直接作用于人体的药物,而是通过影响肠道微生物,抑制TMAO合成途径,进而降低TMAO在血液中的水平。
欣慰的是,DMB这种物质在自然界中是广泛存在的,例如香脂醋、红酒、橄榄油和葡萄籽油等,其中有些食物的DMB含量竟高达25mM(比研究团队做实验时使用的浓度μM水平,1mM=1000μM还要高),如此看来这些食物可能对动脉粥样硬化有食疗效果。
大家有没有发现,这些食物有个专有名词——地中海饮食(Mediterranean diet),目前已经有大量的研究文章表明,地中海饮食有利于健康。比如2013年发表在国际著名杂志《新英格兰医学》上的研究表明,地中海饮食可以有效降低心脏病的发病风险。
原文:Non-lethal Inhibition of Gut Microbial Trimethylamine Production for the Treatment of Atherosclerosis.
Nature Communications:脂膜包裹细菌可用于增强微生物制剂口服给药和治疗效果
近日,上海交通大学医学院附属仁济医院刘尽尧团队通过生物界面超分子自组装,实现生物相容性脂质体包裹细菌,从而显著提高了肠道生物利用度,并提高细菌对环境的抵抗。
如何实现脂质体包裹细菌呢?研究人员用二油酰基磷脂酸(DOPA)(需钙离子协助)和磷酸钙缓冲液中的胆固醇(起固定作用),DOPA与胆固醇摩尔比率为4:1,隔离包被大肠杆菌Nissle1917(EcN),通过透射电子显微镜可以清晰的分辨包被的细菌和未被包被的细菌。
然后在不同环境下看包被细菌与未包被细菌存活情况。抗生素(氨苄西林和阿普霉素)条件下包被细菌3小时存活率是未包被细菌的50倍;强酸(ph2.0)、强碱(ph11)条件下包被细菌与未包被细菌相比存活细菌数仅下降了50%,存活时间从3小时延长到5小时;乙醇浓度增加到50%,包被细菌与未包被细菌相比存活细菌数增加了2倍;模拟胃液(含有胃蛋白酶ph1.2,和胰蛋白酶ph6.8),包被细菌耐受性显著。
同时也对枯草芽孢杆菌进行了试验研究,证明这种保护作用也可适用于其他益生菌株。
为了评估脂质体包裹细菌是否可作为疾病的预防和治疗方法,研究人员进行了小鼠试验,研究溃疡性结肠炎(鼠伤寒沙门氏菌(STm)引起)。研究发现含有包裹脂质体细菌的小鼠粪便中EcN/STm的比例为25至8000,高出含有未包裹脂质体细菌的小鼠三倍;盲肠中EcN/STm的比率高出3100倍;明显体重减轻,较低水平的IL-6和IFN-血清中的γ,病变中MPO阳性细胞较少等。
试验结果表明:小鼠添加脂质体包裹细菌后,可以显著降低疾病严重程度。以上研究解决了微生物制剂进入人体后的活性问题,为微生物移植在内的临床应用奠定了基础。
原文:Biointerfacialself-assembly generates lipid membrane coated bacteria for enhanced oraldelivery and treatment.
Science:宿主如何应对细菌感染期间的“群体感应”
近日,来自德国马克斯·普朗克感染生物学研究所的科学家们发现,人体具有一个特殊受体,它虽然不能识别细菌本身,但可以很好地监视细菌间的通信,持续监测感染动态,当有大量细菌存在以至于分泌出被称为毒力因子的致病物质时,该受体会向宿主发出调整免疫反应的信号。
就机会致病菌而言,这一感染的关键门槛特别高:只有当以非常大的数量出现和/或形成致病物质时,它们才能让人患病。许多细菌会产生小分子来监视种群密度(丰度),从而调节其集体行为,这一过程称为群体感应。
细菌如何选择合适的时机发动攻击呢?研究发现,它们通过称为“群体感应”的小分子相互交流。只有当机会致病菌达到相对足够的丰度时,它们才会产生引发疾病的物质和粘液分子,这些物质保护它们抵抗抗生素和人体自身免疫系统的攻击。
研究人员发现,我们的身体细胞可以借助芳烃受体(AhR)发现细菌之间的通信。AhR可以检测群体感应分子,直接识别色素沉着的细菌毒力因子,使体细胞能够检测细菌何时准备攻击。
实际上,在细菌达到致病数量之前,该受体就已经在对它们进行监视了,如果检测到群体感应分子处于早期阶段,芳烃受体就会被抑制,从而阻止免疫防御的过早启动。
原文:Host monitoring of quorumsensing during Pseudomonas aeruginosa infection.
nature microbiology:革兰氏阴性菌通过脂多糖抑制效应半胱天冬酶来防止细胞凋亡
近日,来自德国科隆大学的研究人员发现某些细菌通过抑制效应半胱天冬酶的活性来阻止细胞凋亡,从而使其能够在细胞内安营扎寨。
我们知道,人体细胞对“驻扎”在其内的细菌有一种独特的反应模式:程序性细胞死亡,也称为细胞凋亡,可以对被感染细胞的应激情况作出相应反应,导致其迅速地“自杀”。
研究人员在小鼠模型中发现志贺氏菌表面的脂多糖可以与半胱天冬酶结合并阻断其作用进程,半胱天冬酶是启动细胞凋亡的引擎。同时,缺乏完整脂多糖的细菌会引发细胞凋亡,从而阻止其在细胞内繁殖,继而被免疫系统成功消除,不再引起疾病。
细菌的这一特性策略可以防止宿主细胞快速死亡,保护细菌领地。此策略的破解有望在未来减轻抵御及解决细菌感染所造成的恶劣后果。
原文:Cytosolic Gram-negative bacteria prevent apoptosis by inhibition of effector caspases through lipopolysaccharide.
来源:huiguoguoyongjiejie 肠道君营
原文链接:http://mp.weixin.qq.com/s?__biz=MzU4NjQ5OTMxOQ==&mid=2247485730&idx=1&sn=0268192c903eccdb96519b61d8741e04&chksm=fdfb1cbaca8c95accb0c7c2309d8d2006fd47b2471fa9ce011afe87c31439d3fdb0b1a1c963c&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

新工具:追溯肠道细菌起源

你身体里也有病毒基因:存在于众多生命中

肠道细菌吞食大脑化学物质

《Nature Methods》新工具:追溯肠道细菌起源
遗传学: 杀手是怎样炼成的
“第七届植物病原细菌学术研讨会”在南京召开 12月9日,由中国植物病理学会



肠道细菌大脑“安家”

肠道细菌透露真实年龄

肠道细菌打入肿瘤内部,协助抗癌!

肠道细菌打入肿瘤内部,协助抗癌!